
ГОУВПО ПЕНЗЕНСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ
Медицинский институт
Специальность «Фармация»
Итоговый междисциплинарный экзамен
Экзаменационный билет №9
Задача 11
1. Фармацевтическое предприятие для производства препарата «Адонизид» закупило лекарственное растительное сырье - горицвета весеннего трава. Для подтверждения качества сырья был проведен полный фармакопейный анализ.
3. На фармацевтической фабрике полученный препарат « Адонизид» был подвергнут стандартизации согласно НД. Предложите показатели качества, характеризующие данный препарат в соответствии с источниками и способами получения:
-
Охарактеризуйте химическое строение действующих веществ, входящих в препарат «Адонизид».
-
Приведите комплекс испытаний, позволяющих достоверно определять действующие вещества в препарате. Напишите уравнения реакций.
СЕРДЕЧНЫЕ ГЛИКОЗИДЫ
СЕРДЕЧНЫЕ Гликозиды — это группа физиологически активных веществ природного происхождения, в весьма малых дозах оказывающие специфическое действие на сердечную мышцу.
Применение - для компенсации недостаточности сердечной деятельности, многие из них оказывают и диуретический эффект, относятся к списку А.
Сахара (циклические ацетали), где сахарная часть и несахарная (агликон) соединены через полуацетальный гидроксил сахарной части.

.
Несахарная часть гликозидов называется агликоном; агликоны стероидной природы (в сердечных гликозидах) носят также название генины.
Ннеобходимо в виду токсичности соблюдать осторожность при выделении гликозидов из сырья.
Сырье сушат при 40—60 °С или помещают в сосуд с парами спирта, хлороформа — это способствует инактивации ферментов, а гликозиды остаются нерасщепленными.
Строение сердечных гликозидов
группу. Все агликоны содержат ненасыщенное лактонное кольцо. Агликоны сердечных гликозидов содержат 23 или 24 углеродных атома и различаются между собой по степени окисленности. Они содержат не менее 2 гидроксильных групп, некоторые — альдегидную

Общая формула карденолидов
Сердечные гликозиды по характеру заместителя в 10-м положении можно разделить на 2 группы:

Таблица
29. Химический
состав первичных гликозидов наперстянки
2)
подгруппа группу.
Вторичные гликозиды наперстянок состоят из агликонов и сахарной части одинаковой у всех 3 вторичных гликозидов.
Таблица 30. Химический состав вторичных гликозидов наперстянки
|
Вторичный гликозид |
Агликон |
Сахарная часть |
|
Дигитоксин Гитоксин Дигитоксин |
Дигитоксигенин Гитоксигенин Дигоксигенин |
3 молекулы дигитоксозы тоже тоже |
На основе данных табл. 29 и 30, а также сведений о химическом составе агликонов можно вывести формулы первичных и вторичных гликозидов наперстянок.

СНз
Формула дигиланида С (целанида):

Первичный гликозид наперстянки шерстистой — дигиланид С под названием целанид (Celanidum) и вторичный гликозид наперстянки пурпурной — дигитоксин (Digitoxinum) включены в ГФ.
В ГФ включен также препарат строфантин К (Strophanthinum К). Его получают из семян строфанта Комбе. Препарат содержит в основном 2 гликозида, состав которых приведен в табл. 31.
Таблица 31. Химический состав гликозидов строфантина К
|
Гликозид |
Агликон |
Сахарная часть |
|
К-строфантин-р К-строфантозид |
Строфантидин Строфантидин |
Глюкоза, цимароза 2 молекулы глюкозы, цимароза |
К-строфантин-р можно рассматривать как вторичный гликозид К-строфатозида. Последний, теряя молекулу глюкозы, превращается в К-
Сахарная часть гликозидов
Как отмечалось ранее, сахарный компонент может быть моно- и ди-, и трисахаридом и т.д. У Сахаров различают р-формы; D- и L-ряды и оптическую активность (+ или -). D-ряд — это моносахариды, у которых конфигурация атомных групп у последнего ассиметрического атома углерода такая же, как у правовращающего — глицеринового альдегида, L-ряд — соответственно как у L-глицеринового альдегида.
-Форма — это форма сахара, у которого полуацетальный гидроксил направлен в ту же сторону, что и гидроксил у последнего ас-симетрического атома углерода; в р-форме — они направлены в противоположные стороны.
Оптическая активность Сахаров зависит от конфигурации атомных групп у всех ассиметрических атомов углерода.
Сердечные гликозиды могут содержать:
L-глюкозу
D-глюкозу

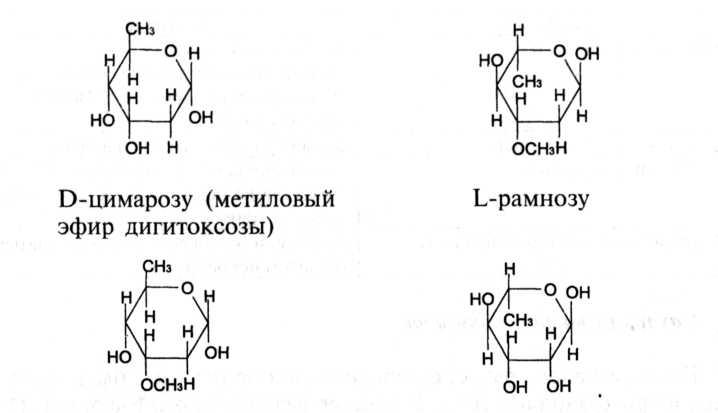
L-олеандрозу
Дигитоксоза, цимароза и олеандроза являются 2,6-дезоксисахарами. Агликоны сердечных гликозидов практически нерастворимы в воде. Сахарный компонент сам по себе неактивный, способствует улучшению растворимости сердечного гликозида, повышает его проницаемость через клеточные мембраны, тем самым усиливая действие агликона.
Методы выделения сердечных гликозидов из растительного сырья
Сердечные гликозиды находятся в растениях в небольших количествах ~ от 0,001 до 0,2 %.
Растительное сырье экстрагируют эфиром для удаления жиров, а затем — спиртом или смесью спирта и хлороформа.
Полученный экстракт выпаривают в вакууме до густой консистенции и экстрагируют теплой водой. Сапонины, осаждают ацетатом свинца, а избыток ацетата свинца удаляют добавлением серной кислоты; как нерастворимый сульфат свинца.
При стоянии из водного раствора выпадает смесь неочищенных гликозидов. Для очистки методы фракционной кристаллизации. В последнее время широко используются адсорбционные методы на различных носителях (силикагеле, кизельгеле и др.).
Физические свойства сердечных гликозидов
Сердечные гликозиды - это твердые, кристаллические, плохо растворимы в воде, оптически активные вещества.
Методы идентификации
, 1.
Сахара, реакциям на углеводы: Фелинга, аммиачный раствор нитрата серебра (после гидролиза),они образуют окрашенные соединения с антроном, п-диметиламинобензальдегидом. Специфическими сахарами сердечных гликозидов являются 2,6-дезоксисахара, для обнаружения которых применяют тест Келлера—Киллиани с антроном. (реакция Пезеца).. Методика основана на образовании фурфурола или его производных из сахарных компонентов под действием концентрированной H2SO4. Фурфурол с антроном затем дает продукт конденсации, окрашенный в зеленый или сине-зеленый цвет:

2. Анализ стероидного цикла
Реакции стероидного цикла Фриделя—Крафтса. При нагревании до 100°С гликозиды в уксусном ангидриде с 20—25 % раствором треххлористой сурьмы дают лиловое окрашивание.
Тест Либермана—Бурхарда. Раствор испытуемого вещества в уксусной кислоте смешивают с 2 мл смеси, состоящей из 50 частей уксусного ангидрида и 1 части концентрированной H2SO4; при этом развивается розовое окрашивание, постепенно переходящее в зеленое или синее. строфантин и его гликозиды в этих условиях окрашиваются в оливково-зеленый цвет, переходящий в желтый.


ральными кислотами; наибольшее распространение получили цветные реакции с серной кислотой.
. Для идентификации карденолидов также используется их способность флюоресцировать в УФ-свете в виде пятен различной окраски при взаимодействии, например с фосфорной кислотой.
3. Реакции на (3,-ненасыщенное лактонное кольцо
.
1. Сердечные гликозиды в присутствии щелочи дают с пикриновой кислотой (тринитрофенолом) оранжевую окраску (реакция Балье):
Несовместимость сердечных гликозидов
-
Карденолиды несовместимы с кислотами и соединениями, ко торые дают кислую реакцию среды. В данном случае происходит гид ролиз по гликозидной связи (отщепление Сахаров). Реакция проходит без видимых внешних изменений (с аскорбиновой кислотой и други ми витаминами кислой реакции среды).
-
Сердечные гликозиды несовместимы со щелочами и соедине ниями, которые дают щелочную реакцию среды (NaHCO3, барби- тал-натрия и др.).
В щелочной среде не происходит гидролиза гликозидной связи, а идет алломеризация с образованием неактивного гликозида (расщепляется лактонное кольцо).
На 1-й стадии происходит расщепление р,-ненасыщенного лак-тонного кольца с образованием соответствующей оксикислоты:

Затем происходит образование полуацеталя:
СНз

СНз

Далее у-кислота способна образовывать внутренний сложный эфир (лактон), что приводит к созданию новой циклической системы (лак-тонизация). Образовавшийся неактивный изоагликон имеет УФ-спектр, который резко отличается от такового нативного гликозида (возможность оценки чистоты методом УФ-спектрометрии).


-
Соли тяжелых металлов осаждают сердечные гликозиды из растворов.
-
Гликозиды несовместимы с дубильными веществами (отвар толокнянки и др.), препаратами валерианы (уменьшение фармако логической активности сердечных гликозидов), производными бар битуровой кислоты (уменьшение амплитуды сердечных сокраще ний), с диуретиками (усиление действия сердечных гликозидов, гипокалиемия).
-
Карденолиды разлагаются при нагревании.
