
ШПОРЫ ПО ФИЗИКИ / Максвелловское распределение частиц по скоростям
.docМаксвелловское распределение частиц по скоростям:
П![]() усть
молекула А имеет скорость
u1,
равную по модулю u
и направленную
вдоль оси ОХ. После упругого столкновения
с другой молекулой, движущейся с такой
же по модулю скоростью
u2
вдоль оси
OZ, молекула
А может получить дополнительную
скорость u2
(рис). В результате такого столкновения
вторая молекула останавливается, а
скорость молекулы А становится равной
u'1=u1+u2,
так что u'1=2u.
Закон
распределения по скоростям теплового
движения молекул газа, находящегося
в состоянии термодинамического
равновесия, впервые был найден Д. К.
Максвеллом (1859) и называется
распределением
Максвелла.
Ход рассуждений Максвелла достаточно
сложен, и приводить его мы не будем, а
ограничимся рассмотрением физического
смысла закона Максвелла и некоторых
его следствий.
усть
молекула А имеет скорость
u1,
равную по модулю u
и направленную
вдоль оси ОХ. После упругого столкновения
с другой молекулой, движущейся с такой
же по модулю скоростью
u2
вдоль оси
OZ, молекула
А может получить дополнительную
скорость u2
(рис). В результате такого столкновения
вторая молекула останавливается, а
скорость молекулы А становится равной
u'1=u1+u2,
так что u'1=2u.
Закон
распределения по скоростям теплового
движения молекул газа, находящегося
в состоянии термодинамического
равновесия, впервые был найден Д. К.
Максвеллом (1859) и называется
распределением
Максвелла.
Ход рассуждений Максвелла достаточно
сложен, и приводить его мы не будем, а
ограничимся рассмотрением физического
смысла закона Максвелла и некоторых
его следствий.
С![]() корости
молекул удобно изображать в виде полярных
векторов в трехмерном пространстве
скоростей,
в котором по взаимно ортогональным
осям координат отложены компоненты
ux,
uy
и uz
скоростей молекул (рис
2). Пусть
dn – число
молекул в единице объема газа, модули
скоростей которых заключены в пределах
от u
до
u+du. Очевидно,
что концы векторов скоростей этих
молекул должны лежать в пространстве
скоростей внутри шарового слоя,
закрашенного на (рис 2). Объем этого слоя
d=4u2du.
При тепловом движении из-за его
беспорядочности все направления
скоростей молекул равновероятны.
Поэтому число
dn должно
быть пропорционально как числу
молекул в единице объема газа, так и
объему
d
шарового слоя. Кроме того, dn должно
зависеть от модуля скорости u. Таким
образом,
корости
молекул удобно изображать в виде полярных
векторов в трехмерном пространстве
скоростей,
в котором по взаимно ортогональным
осям координат отложены компоненты
ux,
uy
и uz
скоростей молекул (рис
2). Пусть
dn – число
молекул в единице объема газа, модули
скоростей которых заключены в пределах
от u
до
u+du. Очевидно,
что концы векторов скоростей этих
молекул должны лежать в пространстве
скоростей внутри шарового слоя,
закрашенного на (рис 2). Объем этого слоя
d=4u2du.
При тепловом движении из-за его
беспорядочности все направления
скоростей молекул равновероятны.
Поэтому число
dn должно
быть пропорционально как числу
молекул в единице объема газа, так и
объему
d
шарового слоя. Кроме того, dn должно
зависеть от модуля скорости u. Таким
образом,
г![]() де
де
![]()
Функция распределения
п![]() редставляет
собой долю молекул, модули скоростей
которых находятся в шаровом слое
единичной толщины. Произведение
редставляет
собой долю молекул, модули скоростей
которых находятся в шаровом слое
единичной толщины. Произведение
F![]() (u)
du=dn/n0
есть вероятность того, что модуль
скорости молекулы заключен между u
и
u+du. Функция
F (u) наз. функцией
распределения молекул газа по модулям
их скоростей.
Закон
распределения молекул по скоростям
(закон Максвелла):
(u)
du=dn/n0
есть вероятность того, что модуль
скорости молекулы заключен между u
и
u+du. Функция
F (u) наз. функцией
распределения молекул газа по модулям
их скоростей.
Закон
распределения молекул по скоростям
(закон Максвелла):
Н![]() аиболее
вероятная скорость:
аиболее
вероятная скорость:
С![]() редняя
арифметическая скорость:
редняя
арифметическая скорость:
Р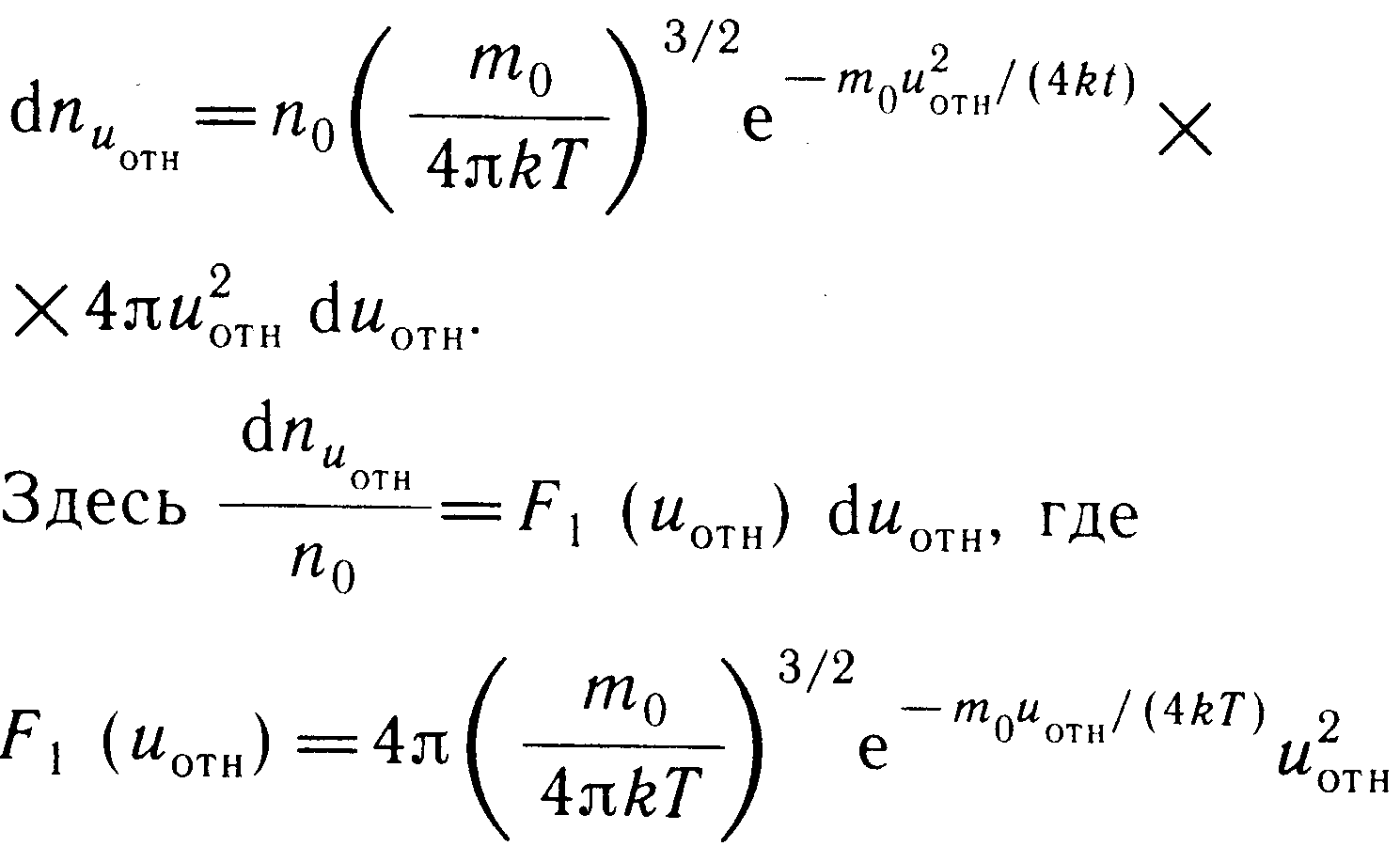 аспределение
молекул по относительным скоростям:
аспределение
молекул по относительным скоростям:
– функция распределения молекул идеального газа по относительным скоростям.
Средняя относительная скорость:
![]()
