
- •ГЕТЕРОЦИКЛИЧЕСКИЕ
- •ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
- •ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
- •ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
- •ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
- •ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
- •ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
- •ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
- •ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
- •ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
- •ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
- •ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
- •ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
- •ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
- •ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
- •ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
- •ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
- •ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
- •ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
- •ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
- •ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
- •ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
- •ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
- •ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
- •ШЕСТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
- •ПИРИДИН
- •ПИРИДИН
- •ПИРИДИН
- •ПИРИДИН
- •ПИРИДИН
- •ПИРИДИН
- •ПИРИДИН
- •ПИРИДИН
- •ПИРИДИН
- •ПИРИДИН
- •ПИРИДИН
- •ПИРИДИН
- •ПИРИДИН
- •ПИРИДИН
- •ХИНОЛИН
- •ХИНОЛИН
- •ХИНОЛИН
- •ХИНОЛИН
- •ХИНОЛИН
- •ХИНОЛИН
- •ХИНОЛИН

ХИНОЛИН
Реакции электрофильного замещения SEAr
Хинолин вступает в реакции электрофильного замещения. При взаимодействии со смесью концентрированных азотной и серной кислот происходит нитрование в положения 5 и 8
|
NO2 |
|
|
|
HNO3, H2SO4 |
+ |
|
|
SEAr |
||
N |
N |
||
N |
|||
|
|
NO2 |
|
|
5-Í èòðî õèí î ëèí |
8-Í èòðî õèí î ëèí |
SO2OH
H2SO4 |
+ |
|

 N
N SEAr
SEAr 
 N
N

 N
N
|
SO2OH |
5-Õèí î ëèí ñóëü- |
8-Õèí î ëèí ñóëü- |
ф о н о вая кисло та |
ф о н о вая кисло та |

ХИНОЛИН
Реакции нуклеофильного замещения SNAr
Хинолин так же, как и пиридин, вступает в реакции нуклеофильного замещения: взаимодействует с амидом натрия и фениллитием
|
NaNH2, NH3 |
|
|
|
|
н агреван ие |
|
+ NaH + NH3 |
|
|
SN |
|
||
N |
N NH2 |
|||
|
||||
|
|
2-Àì èí î õèí î ëèí |
H2+ NaNH2 |
|
|
Li |
|
|
|
н агреван ие |
+ LiH |
|
|
SN |
||
N |
N |
||
|
2-Фен илхин о лин
ХИНОЛИН
Окисление
При окислении перманганатом калия образуется дикарбоновая кислота
|
KMnO4 |
COOH |
|
|
|
|
н агреван ие |
COOH |
N |
N |
2,3-П иридин дикар- бо н о вая кисло та

ХИНОЛИН
Методы получения
Наиболее удобным путем получения хинолина является метод Скраупа: взаимодействие анилина с глицерином и нитробензолом в присутствии серной кислоты и сульфата железа (II)
|
|
+ CH2 |
|
CH |
CH2 |
C6H5NO2, FeSO4, H2SO4, T |
|
|
|
|
||||
|
|
|
|
|
|
|||||||||
|
|
|
|
|
||||||||||
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
N |
|
|
|
OH |
|
OH |
|||||||||
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
84-91% |
|||||||||

ХИНОЛИН
Методы получения
Синтез состоит из следующих стадий.
1. Дегидратация глицерина под действием концентрированной серной кислоты
|
|
|
CH |
|
H2SO4, T |
|
CH C |
O |
||
|
CH2 |
|
|
CH2 |
|
|
CH2 |
+ 2H2O |
||
|
|
|
|
|
||||||
|
|
|
|
|
||||||
|
OH |
|||||||||
|
OH |
|
OH |
|
|
H |
||||
2. Нуклеофильное присоединение анилина к акролеину
|
|
|
H |
|
O |
|
CH C |
O |
+ |
C CH2 |
|
CH2 |
+ |
||||
|
|
H |
AN |
N |
CH2 |
|
|
|
NH2 |
|
|
H
ХИНОЛИН
Методы получения
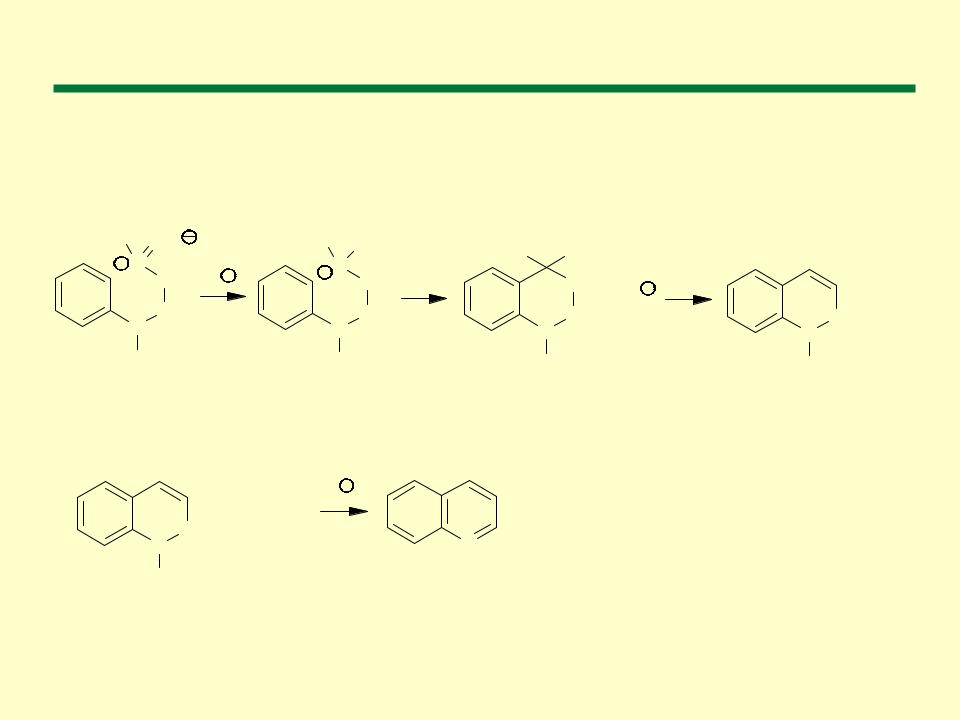
3. Электрофильная атака ароматического кольца электронодефицитным углеродом
H |
|
O |
|
H |
OH |
H |
OH |
|
|
|
|
+ C CH2 H + |
+C |
|
|
|
|
|
|||||
CH2 |
|
CH |
|
H + |
|
|
|||||
|
|
CH2 |
|
CH2 |
|
2 |
+ |
|
|
||
|
N |
N |
N |
CH2 |
-H2O |
N |
CH2 |
||||
|
|
|
|
|
|
|
|
||||
|
H |
|
|
H |
|
H |
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
1,2-Дигидро хин о лин |
|
4. Окисление нитробензолом |
|
|
|
|
|
|
|||||
3 |
|
|
+ C6H5NO2 |
H + |
|
+ C6H5NO2 + 2H2O |
|
|
|||
|
|
N |
CH2 |
|
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
H
Сульфат железа FeSO4 сдерживает бурное течение реакции
