
- •ГЕТЕРОЦИКЛИЧЕСКИЕ
- •ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
- •ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
- •ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
- •ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
- •ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
- •ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
- •ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
- •ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
- •ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
- •ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
- •ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
- •ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
- •ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
- •ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
- •ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
- •ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
- •ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
- •ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
- •ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
- •ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
- •ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
- •ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
- •ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
- •ШЕСТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
- •ПИРИДИН
- •ПИРИДИН
- •ПИРИДИН
- •ПИРИДИН
- •ПИРИДИН
- •ПИРИДИН
- •ПИРИДИН
- •ПИРИДИН
- •ПИРИДИН
- •ПИРИДИН
- •ПИРИДИН
- •ПИРИДИН
- •ПИРИДИН
- •ПИРИДИН
- •ХИНОЛИН
- •ХИНОЛИН
- •ХИНОЛИН
- •ХИНОЛИН
- •ХИНОЛИН
- •ХИНОЛИН
- •ХИНОЛИН

ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
Химические свойства
Пиррол обладает свойствами слабой кислоты и образует соли со щелочными металлами
|
KOH |
|
+ |
|
N |
.. |
_ |
H O |
|
N |
2 |
|||
H |
.. |
|
|
|
K + |
|
|
||
|
|
|
||
Значение рКа пиррола оценивается приближенно как 16,5, следовательно, это более сильная кислота, чем аммиак. Это обусловлено большей степенью s-характера N-H-связи по сравнению с аммиаком. Свободная электронная пара азота, которая обуславливает основные свойства, вовлечена в -облако, и поэтому она не способна к
обобществлению с протонами кислоты

ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
Взаимодействие с сильными кислотами, ацидофобность
Пиррол, фуран и тиофен взаимодейтсвуют с сильными кислотами. В случае пиррола и фурана происходит осмоление (олигомеризация и полимеризация), тиофен в присутствии серной кислоты сульфируется. Т.е. пиррол и фуран являются ацидофобными (боятся кислот). Ацидофобность связана с присоединением протона к -углеродному
атому, разрушением стабилизированной замкнутой сопряженной системы с вытекающим отсюда следствием – дальнейшими превращениями активной диеновой системы
.. |
+ H Y |
H |
о лиго м еризация |
|
H |
п о лим еризация |
|||
X |
X |
|||
|
X = NH, O

ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
Реакции электрофильного замещения
Пиррол, фуран и тиофен, как и другие ароматические соединения, вступают в реакции электрофильного замещения: нитрование, сульфирование, галогенирование, ацилирование по Фриделю-Крафтсу. Пиррол и фуран более реакционноспособные соединения, чем бензол, и сходны с наиболее активными производными бензола: аминами и фенолами. Тиофен менее реакционноспособен, чем пиррол и фуран, но более активен, чем бензол.

ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
Реакции электрофильного замещения
Электрофильное замещение происходит в положение 2
4 |
3 |
+ |
|
|
|
|
E X |
|
|
5 |
2 |
|
Е |
+ HX |
|
N1 |
N |
|
|
|
|
|
||
|
H |
H |
|
|
В реакции электрофильного замещения лимитирующей стадией является стадия образования -комплекса в результате присоединения
электрофильного реагента к атому углерода кольца

ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
Реакции электрофильного замещения
Нитрование и сульфирование пиррола из-за чувствительности к протонным кислотам (происходит полимеризация) проводят в отсутствие протонных кислот. Реакция бромирования и ацилирования по Фриделю-Крафту протекает без участия катализатора
OO
HNO3 + (CH3CO)2O |
|
|
|
|
O N+ O |
|
+ CH3COOH |
|
H C C |
||||||
|
|||||||
|
|
||||||
|
3 |
|
|
|
|
|
|
|
|
ацетилнитрат |
|||||

ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
Реакции электрофильного замещения
CH COONO , 5OC |
|
|
||||
3 |
2 |
|
|
|
+ |
CH3COOH |
Í èòðî âàí èå |
|
|
|
|||
|
N |
NO2 |
||||
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
SO , п иридин , 90OC |
|
|
|
|
||
3 |
|
|
|
|
|
|
Сульф иро ван ие
N Br2, C2H5OH
HÁðî ì èðî âàí èå
(CH3CO)2O, 250OC
Ацилиро ван ие
 N
N SO3H
SO3H
Br H Br
+ HBr
Br N
N Br
Br
H
|
|
+ |
CH3COOH |
|
N |
OCOCH3 |
|||
|
||||
|
|
|
|
|
H |
|
|
||

ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
Реакции электрофильного замещения
Фуран в реакциях электрофильного замещения напоминает пиррол. Как и пиррол является ацидофобным соединением: в присутствии протонных кислот кольцо фурана раскрывается. Хлорирование и бромирование фурана протекает очень бурно и с трудом поддается контролю. Ацилирование требует применения мягкой кислоты Льюиса
|
|
CH3COONO2 |
|
|
+ |
CH3COOH |
||||
|
|
|
||||||||
|
|
Í èòðî âàí èå |
|
|
|
O |
|
NO2 |
||
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
||
|
|
SO3, п иридин |
|
|
|
|
|
|||
O |
|
|
|
|
|
|||||
|
|
|
|
|
||||||
|
Сульф иро ван ие |
O |
|
SO3H |
|
|
||||
|
|
|
|
|
|
|
|
|
||
|
|
(CH3CO)2O, BF3 |
|
|
|
+ |
CH3COOH |
|||
|
|
|
|
|
|
|
|
|
||
|
Ацилиро ван ие |
|
|
|
O |
|
OCOCH3 |
|||
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
||

ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
Реакции электрофильного замещения
Тиофен менее реакционноспособен по сравнению с фураном и пирролом, он может быть просульфирован в условиях высокой кислотности. Бромирование может проводится направленно с образованием 2-бром- или 2,4-дибромтиофена
|
CH3COONO2, (CH3CO)2O |
|
|
|
|
|
|
+ |
CH3COOH |
||||||
|
|
|
|
|
|
|
|||||||||
|
|
Í èòðî âàí èå |
|
|
|
|
|
|
|||||||
|
|
|
|
|
S |
|
NO2 |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
H2SO4 |
|
|
|
|
|
|
+ |
|
H2O |
||
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
Сульф иро ван ие |
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
S |
|
SO3H |
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
S |
|
|
|
Br2, áåí çî ë |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
+ |
|
|
+ HBr |
|||
|
Áðî ì èðî âàí èå |
|
|
|
|
|
|
|
|
||||||
|
Br |
|
|
|
S |
|
Br |
|
S |
Br |
|||||
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
C6H5COCl, SnCl4 |
|
|
|
|
|
|
|
|
+ |
HCl |
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
Ацилиро ван ие |
|
|
S |
|
OCOCH3 |
|||||||||
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||
ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
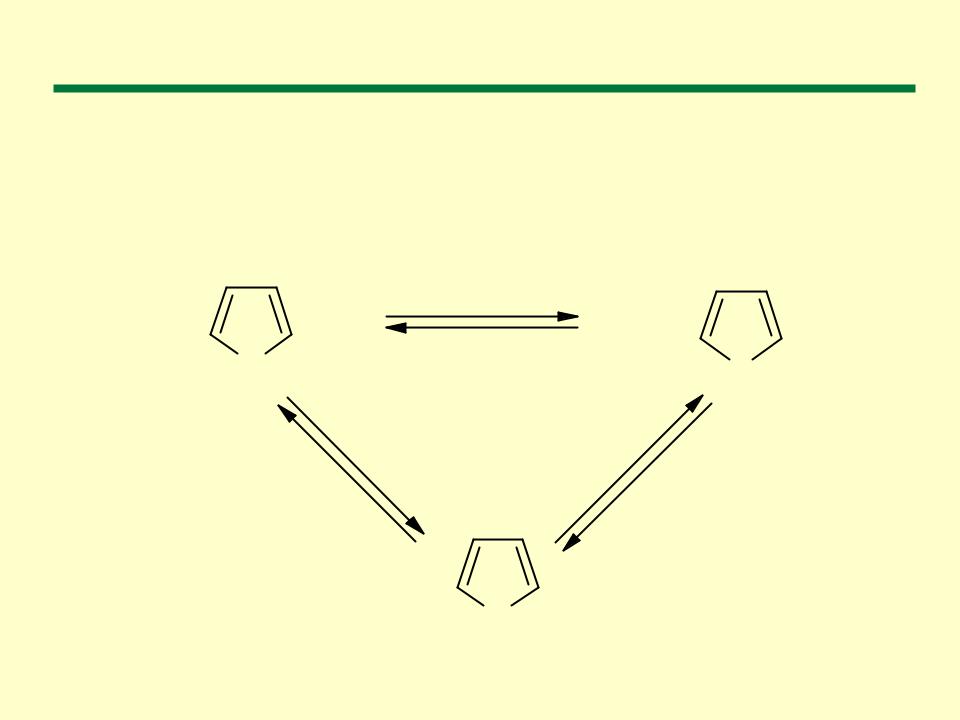
Реакция обмена гетероатомов
Реакция обмена гетероатомов (реакция Юрьева). Фуран, тиофен, пиррол могут взаимно превращаться друг в друга в токе Н2О, Н2S и
NH3 соответственно при температуре 400-500 0С в присутствии Al2O3
H2S
O |
H2O |
S |
|
Al2O3, 400 oC
NH3 H2S
H2O |
NH3 |
N
H

ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ
Реакции присоединения
Фуран, пиррол сравнительно легко гидрируются (тиофен отравляет катализатор)
H2, Ni
O  O
O
Тиофен может восстанавливаться химически (Na, C2H5OH). Гидрированные продукты (тетрагидрофуран, пирролидин и тиофан) используются в качестве растворителей
