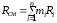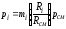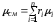- •Содежание.
- •II. Циклы двигателей внутреннего сгорания
- •Результаты расчета примера задания к разделу 2
- •III. Водяной пар. Паросиловые установки
- •Результаты расчета цикла Ренкина (№1)
- •2. Расчет термического к.П.Д. Цикла и удельного расхода пара
- •Результаты расчета цикла Ренкина (№2)
- •Результаты расчета цикла Ренкина (№3)

Содежание.
1)ГАЗОВЫЕ СМЕСИ.ТЕПЛОЕМКОСТЬ ГАЗОВ…………………………………………….
2)ЦИКЛЫ ДВИГАТЕЛЕЙ ВНУТРЕННЕГО СГОРАНИЯ……………………………………
3)ВОДЯНОЙ ПАР. ПАРОСИЛОВЫЕ УСТАНОВКИ………………………………………...
I. ГАЗОВЫЕ СМЕСИ. ТЕПЛОЕМКОСТЬ ГАЗОВ
Для выполнения первого раздела задания необходимо изучить следующие вопросы: параметры состояния рабочего тела, газовые смеси, теплоемкость газов.
Под газовыми смесями понимают механическую смесь нескольких газов, химически между собой не взаимодействующих. Смесь идеальных газов подчиняется всем законам, относящимся к идеальным газам. Состав газовой смеси определяется количеством каждого из газов, входящих в смесь, и может быть задан массовыми mi или объемными ri долями:
mi = Mi / M; ri = Vi / V,
где Mi – масса i-го компонента, Vi – объем i-го компонента, а M и V – масса и объем всей смеси соответственно.
Очевидно, что
М1 + М2 +…+Мn = M;
m1 + m2 +…+mn = 1,
а также
V1 + V2 +…+ Vn = V;
r1 + r2 +…+rn = 1.
Для удобства решения практических задач со смесями газов введено понятие о кажущейся молекулярной массе смеси газов, которая представляет собой среднюю массу из действительных молекулярных масс отдельных компонентов смеси.
Уравнение состояния смеси газов имеет вид:
 .
.
На смеси газов распространяется понятие универсальной газовой постоянной:
 ,
Дж/(кмоль·К).
,
Дж/(кмоль·К).
Связь между давлением газовой смеси р и парциальным давлением отдельных компонентов рi, входящих в смесь, устанавливается законом Дальтона:
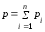 .
.
Если заданы состав газовой смеси, а также характеристики составляющих смесь газов, то можно рассчитать необходимые характеристики смеси по приведенным в табл. 1 формулам.
В теплотехнических расчетах при определении количества теплоты чаще всего пользуются понятием «удельная теплоемкость», хотя называют ее просто «теплоемкость». Под удельной теплоемкостью понимают количество теплоты, которое необходимо сообщить телу, чтобы повысить температуру какой-либо его количественной единицы на 1 К. В зависимости от выбранной количественной единицы различают теплоемкости:
мольную с, кДж/(кмольК);
массовую с, кДж/(кгК);
объемную с/, кДж/(Н·м3К).
Эти теплоемкости связаны между собой следующими соотношениями:
с = с/ ; с/ = с/22,4 ; с/ = сн ,
где н – плотность газа при нормальных условиях.
Таблица 1
|
Задание состава смеси |
Перевод из одного состава в другой |
Плотность и удельный объем смеси, кг/м3, м3/кг. |
Кажущаяся молекулярная масса смеси, кг. |
Газовая постоянная смеси, Дж/(кгК) |
Парциальное давление, Па. |
|
Массовыми долями |
|
|
|
|
|
|
Объемными долями |
|
|
|
|
|
Формулы для расчета газовых смесей
В табл. 1 i – молекулярная масса i-го компонента; 8314 Дж/(кмольК) – значение универсальной газовой постоянной; Ri – газовая постоянная i-го компонента.
1 м3
газа имеет различную массу в зависимости
от давления и температуры. В связи с
этим объемную теплоемкость всегда
относят к массе газа, заключенной в 1 м3
при нормальных условиях (н
= 101325 Па, Tн
= 273 К). При этом объем 1 кмоля различных
газов равен 22,4 м3/кмоль,
а универсальная газовая постоянная –
 Дж/ (кмоль·К). В зависимости от способа
подвода тепла к газу (р
= const
или V
= const)
различают изобарную ср
и изохорную сv
теплоемкости. Отношение этих величин
носит название показателя адиабаты:
Дж/ (кмоль·К). В зависимости от способа
подвода тепла к газу (р
= const
или V
= const)
различают изобарную ср
и изохорную сv
теплоемкости. Отношение этих величин
носит название показателя адиабаты:
k = cp/cv = cp/cv.
Теплоемкости ср и сv связаны также соотношением Майера:
сp - cv = R = 8,314, кДж/(кмольК).
Теплоемкость газов меняется с изменением температуры, причем эта зависимость имеет криволинейный характер. Значения истинных и средних теплоемкостей в интервале от 00 до t берутся непосредственно из таблиц, причем в необходимых случаях производится интерполяция. Количество теплоты, которое необходимо затратить в процессе нагревания 1 кг газа в интервале температур от t1 до t2, определяется по формуле:

где cm1 и cm2 – соответственно средние теплоемкости в пределах 00 – t1 и 00 – t2 .
Если в процессе участвуют М (кг) или Vн (м3) газа, то
QV = M(cvm2 t2 – cvm1t1) = Vн(c/vm2 t2 – c/vm1 t1) , кДж;
QP = M(cpm2 t2 – cpm1 t1) = Vн(c/pm2 t2 – c/pm1 t1) , кДж.
Теплоемкость газовой смеси следует определять по формулам:
массовая
-
 ;
;
объемная
-
 ;
;
мольная
-
 .
.
Расчета первого раздела задания
Для использования теплоты газов, являющихся продуктами сгорания топлива в котельном агрегате, в газоходах последних устанавливаются воздухоподогреватели воздуха, необходимого для горения топлива (рис. 1). Уходящие из котла газы поступают к воздухоподогревателю с температурой t1/ и охлаждаются, отдавая теплоту воздуху, до t1//. В газоходе котельного агрегата под влиянием работы дымососа устанавливается давление несколько ниже атмосферного. Воздух в воздухоподогревателе нагревается от температуры t2/ до температуры t2//.

Рис. 1
При испытании котельного агрегата были получены следующие данные:
-
Температура газов при входе в воздухоподогреватель, t1/ = 300 0С.
-
Температура газов при выходе из воздухоподогревателя, t1// = 120 0С.
-
Температура воздуха при входе в воздухоподогреватель, t2/ = 20 0С.
-
Температура воздуха при выходе из воздухоподогревателя, t2// = 170 0С.
-
Объемный состав дымовых газов – СО2 =20,5%; Н2О =5,4%; О2 =17,3%; N2 =56,8%.
-
Часовой расход газов при t1// составляет 50103 м3/ч.
-
Разряжение в газоходе – 15 мм вод. ст.
-
Барометрическое давление – 760 мм рт. ст.
Определить:
-
Кажущийся молекулярный вес дымовых газов.
-
Газовую постоянную дымовых газов.
-
Весовые (массовые) доли отдельных компонентов, входящих в состав дымовых газов.
-
Парциальные давления компонентов.
-
Часовой расход воздуха.
Принять, что все тепло, отданное газом, воспринято воздухом. Зависимость теплоемкости от температуры считать криволинейной.
Решение:
-
Кажущийся молекулярный вес дымовых газов:

-
Газовая постоянная дымовых газов:
 Дж/(кгК).
Дж/(кгК).
-
Массовые доли компонентов газов:

4. Парциальные давления компонентов:

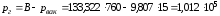 Па.
Па.
Результаты расчета представлены в табл. 2.
Таблица 2
Результаты расчета примера задания к разделу 1
|
Параметры |
СО2 |
Н2О |
О2 |
N2 |
Газовая смесь |
|
ri |
0,14 |
0,09 |
0,162 |
0,608 |
1,000 |
|
i, кг/кмоль |
44 |
18 |
32 |
28 |
29,988 |
|
riI, кг/кмоль |
6,16 |
1,62 |
5,184 |
17,024 |
- |
|
mi |
0,205 |
0,054 |
0,173 |
0,568 |
1,000 |
|
рi10-5, Па |
0,142 |
0,091 |
0,164 |
0,615 |
1,012 |
5. Часовой расход воздуха.
Расход воздуха определяется из уравнения теплового баланса воздухоподогревателя
 .
.
Значения теплоемкостей компонентов дымовых газов и воздуха находим по приложению 1; значения теплоемкостей дымовых газов и воздуха рассчитываем по формулам. Средняя удельная теплоемкость компонентов при p=const в интервале температур 0…300 0С:

· 29,290= 31,691 кДж/(кмольК);
в интервале температур 0…120 0С:
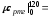 0,1438,5066+0,0933,8214+0,16229,6206+0,60829,0686=
0,1438,5066+0,0933,8214+0,16229,6206+0,60829,0686=
= 30,907 кДж/(кмольК);
в интервале температур 300…120 0С:
 кДж/(кмольК);
кДж/(кмольК);
 кДж/(Н·м3К).
кДж/(Н·м3К).
Средняя теплоемкость воздуха при p=const в интервале температур 20…170 0С:
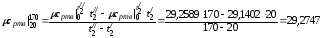 кДж/(кмольК);
кДж/(кмольК);
 кДж/(Н·м3К).
кДж/(Н·м3К).
Объем, занимаемый дымовыми газами, приведенный к нормальным условиям (н.у.):
 нм3/ч.
нм3/ч.
Часовой расход воздуха:
 нм3/ч.
нм3/ч.