
- •Биологическая химия
- •Глава I. Лабораторный практикум
- •Раздел 1 белки
- •1.1. Состав и свойства белков
- •Техника безопасности
- •1. Осаждение белков неорганическими осадителями
- •Техника безопасности
- •1.2.Методы количественного определения белков
- •Раздел 2. Ферменты
- •Раздел 3. Витамины
- •Раздел 4. Химия и обмен углеводов
- •Раздел 5. Химия и обмен липидов
- •Раздел 6. Обмен простых белков и аминокислот
- •Раздел 7. Обмен нуклеотидов
- •Раздел 8. Биохимия крови
- •Раздел 9. Биохимия мочи
- •1. Реакция на хлориды
- •2. Реакции на фосфаты
- •3. Реакции на сульфаты и эфиросерные кислоты
- •4. Реакции на кальций и магний
- •5. Реакция на аммонийные соли
- •1. Реакции на мочевину
- •2. Реакции на мочевую кислоту
- •3. Реакции на креатинин
- •Глава 2. Практические занятия
- •Приложения
- •Вариант 1
- •Вариант 12
- •Глава I. Лабораторный практикум……………………… 6
- •Биологическая химия
- •185910, Петрозаводск, пр. Ленина, 33
4. Реакции на кальций и магний
Кальций и магний выводятся через почки в виде солей в небольшом количестве. Установлено, что с мочой выделяется примерно 30% выводимого из организма кальция и магния. Основная часть этих щелочно-земельных металлов является составной частью кала. В течение суток с мочой здорового человека выводится 0,1-0,25 г (2,5-6,2 ммоль) кальция и 0,1-0,2 г (4,2-8,4 ммоль) магния.
При взаимодействии солей кальция со щавелевокислым аммонием образуется белый кристаллический осадок щавелевокислого кальция, нерастворимый в уксусной кислоте, но растворяющийся в минеральных кислотах:
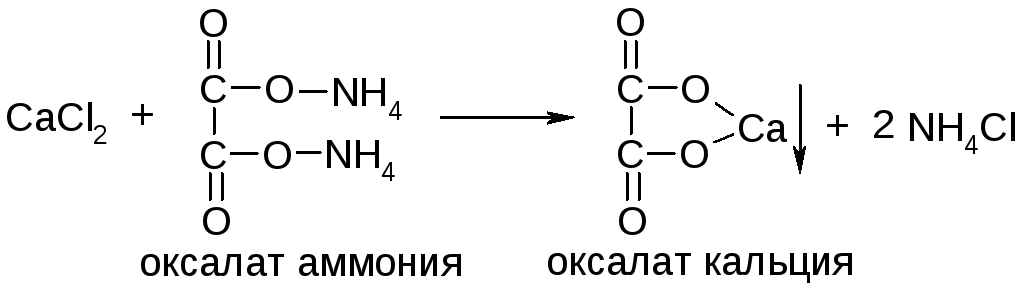
После отделения оксалата кальция фильтрованием соли магния, находящиеся в фильтрате, реагирует с гидроксидом аммония с образованием небольшого осадка двойной аммоний-магниевой соли фосфорной кислоты (фосфорнокислой аммоний-магнезии):
MgНРО4 + NH4OH → Mg(NH4)PO4 + H2O.
Ход работы.К 2 мл мочи прибавляют 4 капли 10%-го раствора уксусной кислоты и 5 капель 5%-го раствора щавелевокислого аммония. Выпадает белый кристаллический осадок оксалата кальция, хорошо заметный при взбалтывании. Жидкость фильтруют и к фильтрату добавляют 7-10 капель 10%-го раствора гидроксида аммония (до щелочной реакции на лакмус). Через 2-3 минуты наблюдается лёгкое помутнение раствора из-за выпадения в осадок фосфорнокислой аммоний-магнезии. Осадок этой соли небольшой, кристаллический, лучше видимый при взбалтывании и рассматривании жидкости в проходящем свете. Кристаллизацию можно ускорить потиранием стеклянной палочкой о внутреннюю стенку пробирки в растворе.
5. Реакция на аммонийные соли
На долю аммонийных солей приходится 4-5% общего количества азота мочи, что соответствует 0,5-1,0 г (36-71 ммоль) аммиака в сутки.
Принцип метода. Аммонийные соли реагируют с гидроксидом кальция с образованием гидроксида аммония, разлагающегося при нагревании с выделением аммиака:
2NH4Cl + Ca(OH)2 → 2NH4OH + CaCl2,
t°С
NH4OH → NH3↑ + H2O.
Ход работы.В пробирку через воронку наливают 1,5-2 мл мочи и 1 мл насыщенного раствора гидроксида кальция (известкового молока). Осторожно вынимают воронку, стараясь не коснуться сливным концом внутренних стенок пробирки. Содержимое пробирки нагревают до кипения и сразу же подносят к отверстию красную лакмусовую бумажку, предварительно смоченную дистиллированной водой. Бумажка синеет вследствие выделения аммиака.
Органические составные части мочи
С мочой взрослого человека в течение суток выделяется около 40 г органических веществ. В моче здорового человека содержатся мочевина, креатинин, мочевая кислота, аминокислоты, гиппуровая кислота, безазотистые компоненты (в основном органические кислоты: щавелевая, молочная, лимонная, янтарная, масляная, валериановая) и другие соединения.
1. Реакции на мочевину
Мочевина – главный конечный продукт азотистого обмена. Количество мочевины, выделяемой с мочой, в норме составляет 20-35 г/сутки (333-583 ммоль/сутки).
Реакция с бромноватистокислым натрием
Принцип метода. Мочевина разлагается бромноватистой щелочью натрия (щелочным раствором бромноватистокислого натрия) с выделением свободного азота:
![]()
Образовавшаяся угольная кислота связывается щелочью натрия:
Н2СО3 + 2NaOH → Na2CO3 + 2H2O.
Ход работы.К 2-3 мл мочи приливают 0,5 мл щелочного раствора бромноватистокислого натрия и наблюдают выделение пузырьков азота.
