
- •Синтез аміаку.
- •Фізико–хімічні основи синтезу аміаку
- •Вплив інертних домішок на рівноважну концентрацію
- •Матеріальний баланс
- •Реактори синтезу аміака.
- •Розрахунок внутрішніх розмірів реакторів синтезу.
- •Газові закони
- •Визначення теплових потоків в реакторі синтезу
- •Коефіцієнт тепловіддачі за умов вільної конвекції.
- •Коефіцієнт тепловіддачі з урахуванням вітру.
- •Визначення об’єму каталізатора в реакторі синтеза.
- •Каталізатори синтезу аміака.
- •Теплообмінні пристрої реактора синтезу.
- •Розрахунок теплообмінників.
- •Конструкції і розрахунок котлів-утилізаторів.
- •Підігрів свіжого газу і розігрів реактора.
- •Розрахунок.
- •Виділення аміаку із газової суміші.
- •Водяні холодильники-конденсатори
- •2. Холодильник – конденсатор змійовикового типу. [ ]
- •Тепловий баланс конденсатора
- •Сепаратори
- •Обладнання для виробництва метилового спирту.
- •Кінетика синтезу
- •Технологічні схеми синтезу метилового спирту
- •Реактори синтезу метилового спирту
- •Розрахунок температурного режиму поличної каталізаторної коробки
- •Об’єм каталізатора і висоташару каталізатора
- •Виробництво карбаміду
- •Схеми виробництва
- •Виділення карбаміду із плаву
- •Принципова схема з розімкненим циклом
- •Принципова схема з частковим рециклом
- •Принципова схема з повнимрециклом
- •Рідинний рецикл суспензії карбаміду в маслі
- •Рідкий рецикл водного розчину амонійних солей
- •Колона синтезу карбаміду
- •Технічна характеристика
- •Розрахунок температурного режиму поличної каталізаторної коробки
- •Об’єм каталізатора і висоташару каталізатора
- •Футерована колона синтезу карбаміду
Кінетика синтезу

Максимальна
швидкість реакції згідно з графіком
буде компенсуватися
![]() .
.
Час
контакту (величина, зворотна об’ємній
швидкості
![]() )
)
![]()
Оптимальна
швидкість приймається
![]() ,
(
,
(![]() ).
).
Технологічні схеми синтезу метилового спирту
Технологічні схеми синтезу метилового спирту поділяються на:
з суміщеною насадкою;
з несуміщеною насадкою.
Агрегат з суміщеною насадкою

1 – компресор, який стискає синтез-газ до 80 МПа;
2 – масляний фільтр;
3 – вугільний фільтр;
8 – доочищувач, в якому змішується свіжий і циркуляційний гази;
4 – реактор синтезу (особливість: значна кількість тепла виділяється, потік розділяється на два потоки);
5 – водяний холодильник-конденсатор;
6 – сепаратор;
7 – циркуляційний компресор, в якому газ дотискається до 30 МПа.
Витрати тиску по схемі – 1,5 МПа.
Продувка застосовується для того, щоб запобігти накопиченню інертних газів.
Агрегат з несуміщеною насадкою

1 – компресор, який стискає синтез-газ до 80 МПа;
2 – масляний фільтр;
3 – вугільний фільтр;
4 – реактор синтезу;
5 – виносний теплообмінник, в якому охолоджується газ;
6 – водяний холодильник-конденсатор;
7 – сепаратор;
8 – циркуляційний компресор;
9 – доочищувач.
Реактори синтезу метилового спирту
Реактори синтезу метилового спирту аналогічні реакторам синтезу аміаку:
трубчаті (в шарі каталізатора знаходяться теплообмінні пристрої);
поличні.
За допомогою теплообмінних пристроїв відводиться теплота і регулюється температура.
Трубчатий реактор синтезу метилового спирту

1 – корпус реактора;
2 – насадка (каталізаторна коробка та ТО);
3 – шар каталізатора;
4 – теплообмінні труби;
5 – центральна труба;
6 – теплообмінник.
Схема поличного реактора

1 – корпус реактора;
2 – насадка;
3 – полиця з каталізатором;
4 – байпасні труби;
5 - центральна труба;
6 - теплообмінник.
Обладнання виробництва метилового спирту (метанол)
CH3OH M=32
tпл=-97,1°С
tкип=64,8°С
ρ=796кг/м3
с=2500 Дж/кг
r=1103 кДж/кг
qзгор.=22518 кДж/кг (теплота згорання)
Пружність пари
|
t, °C |
20 |
30 |
40 |
50 |
64,8 |
|
P, МПа |
0,0127 |
0,0212 |
0,0344 |
0,0525 |
0,1 |
Безбарвна прозора рідина, з водою змішується в будь-яких співвідношеннях та з багатьма органічними розчинниками.
Метанол – отрута. Не відрізняється смаком та запахом від етилового спирту. Вживання всередину: 5-10 мл – тяжке отруєння, 30 мл – летальна (смертельна) доза.
Межі вибухонебезпечності з повітрям 6-34,7% (спирту).
Використання
Сировина для виробництва:
формальдегіду (CH2O) (смоли, пластмаси);
барвників;
оцтового ангідриду;
мурашиної кислоти;
вінілацетату;
етиленгліколю;
біосинтезу білків;
енергетична сировина.
Значна потреба сільського господарства у оцтовій та мурашиній кислотах як консервантах, та білково-вітамінних концентратів для кормів, які отримуються мікробіологічним синтезом.
Метанол – альтернативний енергоносій ( q=22518 кДж/кг, нафтопродукти q=44000кДж/кг), та альтернативна сировина для органічного синтезу. Зараз альтернативою нафті та газу (в Україні) є вугілля. Його можливе використання:
газифікація з отриманням СО+Н2 = метанол;
гідрогенізація з отриманням різних палив.
Метанол може бути домішкою до моторних палив (3-5%), що зменшує викиди СО та тетаетиленсвинцю.
Потужність установки 750 000т/рік.
Історична довідка
Дюма Жан Батіст 1835р виділив СН3ОН з продуктів сухої перегонки деревини.
В природі СН3ОН зустрічається у соках деяких рослин.
До 1923р. основний спосіб отримання з продуктів сухої перегонки деревини.
Сабатьє (кінець ХІХ ст.) робив спробу синтезувати з СО та Н2 в присутності каталізаторів, але при низькому тиску в той час як
СО + 2Н2=СН3ОН + Q (Q=90000 кДж/кмоль)
Сабатьє при низькому тиску отримував СН4.
З 3-х об’ємів вихідних речовин отримується 1 об’єм метанолу, а отже необхідно підвищувати тиск та зменшувати температуру.
В 1913р. фірма BASF розпочала роботи по синтезу з каталізатором.
1921р. Патар – патент на каталізатори для синтезу під тиском (каталізатор ZnO + Cr2O3).
1923р. (BASF) отримано метанол у промислових масштабах.
Сьогодні навіть країни багаті на ліси (Бразилія) виробляють синтетично СН3ОН.
Фізико-хімічні основи синтезу СН3ОН
СО + 2Н2=СН3ОН + Q (Q=90000 кДж/кмоль)
Побічні реакції:
СО + Н2 = СН4 + Н2О + Q1 (Сабатьє)
2СО + 2Н2 = СН4 +СО2 + Q2
2CO + 4H2 = CH3O + H2O + Q2 (CH3O – діметиловий ефір)
4СО + 8Н2 = С4Н9ОН + 3Н2О + Q4 (С4Н9ОН – ізобутиловий спирт)
В результаті склад метанолу сирцю:
СН3ОН – 92-93,5%
Вода – 3,5-6%
Діметиловий ефір – 1-1,6%
Ізобутанол – 0,5-1,2%
Для видалення домішок необхідна багатостадійна ректифікація.
Параметри технологічного процесу
Р=25-30 МПа
t=340-390°C при нормальних температурах швидкість реакції прямує до нуля, що пов’язано з каталізатором.

З підвищенням температури вище 390° прискорюються побічні реакції. Співвідношення СО:Н2 = 1:2, але на практиці для зміщення реакції в сторону СН3ОН беруть співвідношення СО:Н2 = 1:4.
Рівновага реакції

Кp=k2/k1 – константа рівноваги.
k1 – константа швидкості прямої реакції.
k2 - константа швидкості зворотної реакції.
![]()
![]()
Формула Тьомкіна М.І. – Чередніченко В.М.
Формула Нернста
![]()
ν – зміна кількості молів, в реакції ν =2
с – хімічні константи:
с=1,6 для Н2
с=3,5 для СО
с=3,5 для СН3ОН
Кінетика синтезу

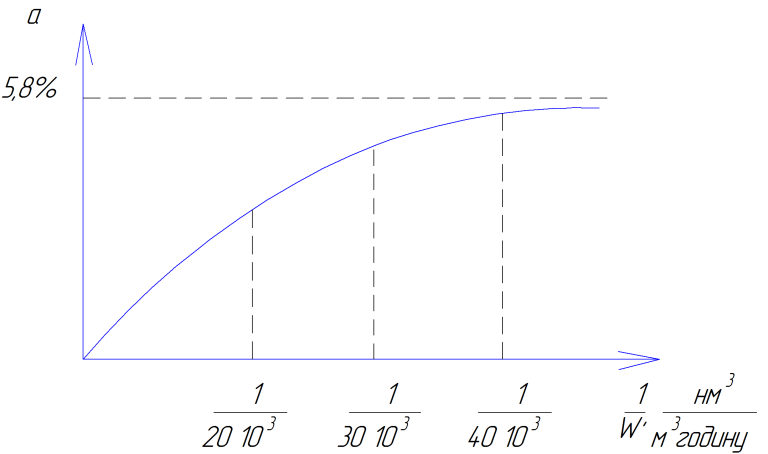
На практиці швидкість приймають на рівні 20·103 - 40·103 нм3/м3кат

Каталізатори
Поділяють на:
високотемпературні (цинк-хромелеві, з домішками t=340-390°C);
низькотемпературні(цинк-мідь-алюміній t=230-275°C).
Для всіх каталізаторів небажаними домішками є залізо, нікель, СО оскільки вони прискорюють побічні реакції в т.ч. метанування та підвищують температуру.
Домішки лужних елементів стимулюють утворення спиртів. Сірка та хлор – отруюють каталізатор.
Найбільше розповсюдження мають цинк-хромелеві каталізатори:
ZnO – 67%
Cr2O3 – 18%
CrO – 8%
Власне каталізатором є ZnO, Cr2O3 – збільшує активність каталізатора, CrO – зменшує чутливість до каталізаторних отрут.
Каталізатор у вигляді гранул:
Таблетки 9х9 мм, 5х5 мм або, що рідше, кульки діаметром 6-7мм.
Отрутою для каталізатора є пентакарбоніл заліза Fe(CO)5.
Вихід СН3ОН на цинк-хромовому каталізаторі:
|
t, °C |
Вихід г/см3годину |
% об. |
|
340 |
2,3 |
4,0 |
|
360 |
3,2 |
5,6 |
|
380 |
3,3 |
5,8 |
|
400 |
3,0 |
5,3 |
Карбонільна корозія
В умовах синтезу СН3ОН спостерігається специфічна корозія – карбонільна.
Fe + 5CO = Fe(CO)5
В результаті якого утворюється пароподібний пентакарбоніл заліза. При низьких температурах t<150°C корозія не відбувається, тому вся холодна апаратура виготовляється з вуглецевих сталей.
При t=150-300°C корозія інтенсивна, при t=330-350°C припиняється. Тому деталі каталізаторних коробок, теплообмінників, трубопроводів та інших апаратів і деталей виготовляють з Х18Н10Т або з матеріалів на основі міді. Поверхні корпусів, кришок, фланців футерують листовою міддю або сталлю Х18Н10Т, товщина листів 2-3мм.
Швидкість карбонільної корозії (мм/рік).
|
Матеріал |
t, °C | ||
|
210 |
260 |
310 | |
|
Сталь 10 |
11,5 |
14,0 |
2,5 |
|
12Х3М |
2,6 |
2,7 |
1,2 |
|
Х18Н9Т |
0,05 |
0,08 |
0,02 |
|
Латунь ЛЖМу 59-1-5 |
0,01 |
0,01 |
0,02 |
Схеми установок синтезу:
з несуміщеною насадкою
з суміщеною насадкою
Схема синтезу СН3ОН з несуміщеною насадкою
1 – масляний фільтр
2 – вугільний фільтр
3 – реактор
4 – виносний теплообмінник
5 – конденсатор (водяний)
6 – сепаратор
7 – циркуляційний насос
8 – пусковий підігрівач
Реактор Ø800мм, Н=12м, Vкат.= 3,5м3, Nнагр.= 1200Вт
Агрегат з суміщеною насадкою
Свіжий газ з температурою 35 0С стискається компресором з тиску 0,9 МПа до 30 МПа проходить послідовно маслянку 2 та вугільний фільтр 3 та направляється у відокремлював 9 вугільного пилу та вологи, у який подається також газ із циркуляційного компресора 8. У відокремлювані потоки свіжого та циркуляційного газу змішуються і далі потрапляють в колону 4. В колону газ поступає кількома потоками (основний та байпасні).
З колони конвертувальний газ поступає у водяний холодильник конденсатор, де охолоджується приблизно до 40 0С, далі поступає в сепаратор 6, 7, в яких відокремлюється метанол –сирець. Після чого газ направляється в циркуляційний турбокомпресор 9, де дотискається до тиску реакції.
Варіант схеми – схема з поршневим циркуляційним компресором. В цьому випадку після нього встановлюють масляний фільтр.
Агрегат з суміщеною насадкою колони має наступні переваги:
Відсутність довгих трубопроводів з температурою вище 200 0С, а отже більш проста та надійна експлуатація апарата, а також низький гідравлічний опір.
Малі втрати тепла в оточуюче середовище в результаті низької температури колони, що обдувається зсередини холодним газом.
Зменшення кількості апаратів високого тиску.


Існують також агрегати з використанням тепла реакції для отримання водяної пари по двоконтурній схемі (колони з полицями).

С интез
метанолу протікає з більш інтенсивним
виділенням тепла, ніж синтез аміаку. (
90 кДж/моль в порівнянні з 52 кДж/моль).
Крім того найбільш оптимальним режимом
є режим в каталізаторній коробці і
достатньо вузький інтервал температур
реакції.
интез
метанолу протікає з більш інтенсивним
виділенням тепла, ніж синтез аміаку. (
90 кДж/моль в порівнянні з 52 кДж/моль).
Крім того найбільш оптимальним режимом
є режим в каталізаторній коробці і
достатньо вузький інтервал температур
реакції.
Ці особливості вимагають підвищенні вимоги до теплообмінного обладнання в колоні та за її межами (схема з не суміщеною насадкою).
Процес близький до ізотермічного вдається створити в каталізаторних коробках трубчатого типу шляхом підвищення об’ємної швидкості до 40000 1/час та більше. Це забезпечує високу продуктивність агрегату при низькому об’ємі метанолу ( ΔZ % СН3ОН) та низькій Δt реакції.
В насадку колони входить нижній теплообмінник та каталізаторна коробка.
Насадка розбірна.
В центральній трубі розташовується пусковий електропідігрівач (N~500кВт). Підігрівач омивається газом з великою швидкістю (малий переріз для газу) завдяки чому зменшується осадження на спіралі нагару, карбонілів заліза та сажі. Зникає небезпека перегріву та замикання спіралі підігрівача. Температурний режим в трубчастій каталізаторній коробці регулюється включенням нижнього холодного байпасу.
Але коробки з одинарними протиточними трубами не забезпечують достатнього відводу тепла реакції з верхньої частини каталі заторної зони, де реакція протікає найбільш інтенсивно.
Подальшим розвитком цієї конструкції являється насадка з двома холодними байпасами. Для цього знизу каталі заторної коробки розміщується двоярусний газовий колектор. Верхня частина колектора слугує для розподілення по трубам основного потоку, а нижній – байпасного. Трубки холодного байпасу 11 рівномірно розміщуються між трубами, по яким рухається основний потік газу.
Для посилення відводу тепла з верхньої частини каталі заторної зони – низ теплообмінних труб ізолюють (! Зверніть увагу, такий прийом не часто зустрічається в теплообмінних пристроях). При цьому ізольована частина трубок основного потоку складає 1/3 -1/2 їх довжини, а потоку байпасного газу 2/3-3/4 довжини.
Полочні колони синтезу метанолу.
Полочні каталізаторні коробки можуть продуктивно та стабільно працювати без перегріву каталізатора при меншій об’ємній швидкості, ніж каталізаторні коробки з протиточними трубками, а отже при більш високому об’ємі метанолу ( ΔZ % СН3ОН), якщо є досить велика кількість полок. Проте в полочних колонах повинен знаходитись попередній теплообмінник, з більшою поверхнею, ніж в колонах з трубчатою каталізаторною коробкою. Це необхідно для забезпечення необхідної температури газу на вході в реакційну зону (335-350 0С).
Нижній холодний бай пас в колоні при її нормальній роботі не використовується. Він вмикається тільки для різкого охолодження каталізатора в разі виникнення реакції метанування, що супроводжується швидким зростанням температури.


Розрахунок (схема)
Склад газу на вході:
CO = 17%
H2 = 68,5%
CH4 = 4,67%
N2 = 8,8%
CO2 = 1,08%
CH3OH = 0,5%
Продуктивність реактора:
![]()
![]()
![]()
![]()
![]()
Ρc=1,39кг/м3 (газ)
Масова частка:
![]()
Кількість утвореного метану:
![]()
![]() - зміна
температури (без втрати тепла);
- зміна
температури (без втрати тепла);
![]() -
теплоємність
суміші;
-
теплоємність
суміші;
![]() - тепловий ефект реакції.
- тепловий ефект реакції.
![]() =90 кДж/кг
=90 кДж/кг
За графіком визначається об’ємна швидкість газу
Графік!
![]()
![]()
![]() –
площа поперечного перерізу.
–
площа поперечного перерізу.
