
- •Одноатомные фенолы (аренолы) Ar-oh
- •Двухатомные фенолы (арендиолы)
- •3. Получение фенола из кумола (кумольный способ)
- •4. Гидроксилирование аренов
- •5. Окислительное декарбоксилирование карбоновых кислот
- •6. Получение из солей диазония
- •Электронное строение фенола
- •1. Реакции по гидроксильной группе
- •1. Кислотные свойства
- •2. Образование фенолятов
- •3. Образование простых эфиров
- •4. Образование сложных эфиров
- •2. Нуклеофильное замещение гидроксильной группы
- •1. Замещение фенольного гидроксила галогеном
- •2. Взаимодействие с аммиаком
- •3) Реакции сульфирования
- •Механизм реакции
- •Конденсация с ароматическими альдегидами
- •2. Окисление фенолов
- •3. Гидрирование фенолов
3) Реакции сульфирования
Фенол легко сульфируется при комнатной температуре концентрированной серной кислотой с образованием орто-изомера, который при температурах выше 1000С перегруппировывается в пара-изомер:

4) Реакции алкилирования
Фенолы легко вступают а реакции алкилирования.
В качестве алкилирующих агентов используют галогеналканы, алканолы и алкены в присутствии протонных кислот (H2SO4, H3PO4) или кислот Льюиса (AlCl3, BF3):

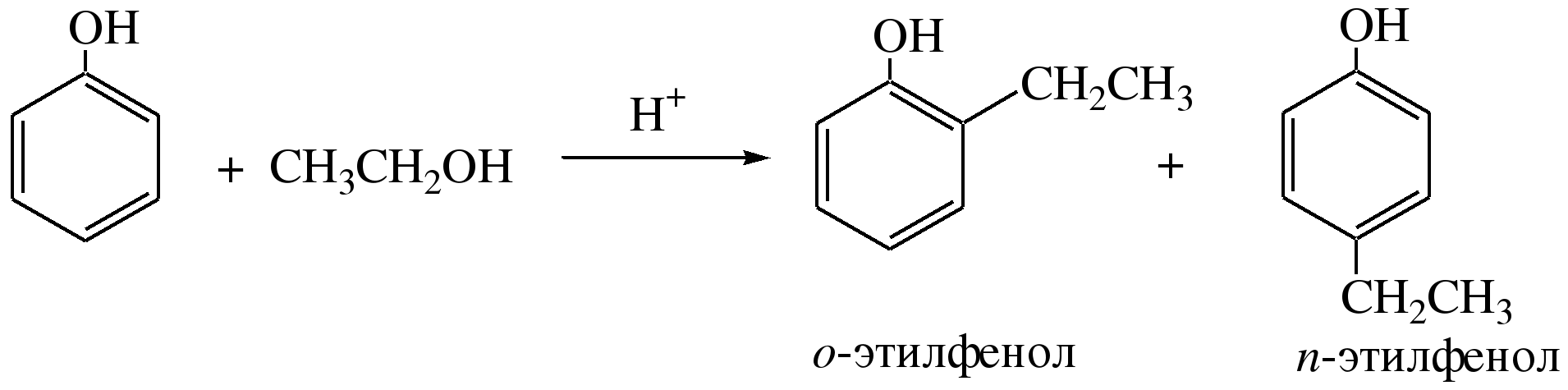
5) Реакции ацилирования
Легко происходит ацилирование фенолов под действием галоген-ангидридов или ангидридов карбоновых кислот в присутствии кислот Льюиса:

6) Реакции нитрозирования
Нитрозофенолы получают прямым нитрозированием фенолов:

пара-крезол орто-нитрозо-пара-крезол
7) Реакции азосочетания
Сочетание с фенолами ведут в слабощелочной среде, так как фенолят-ион значительно активнее, чем сам фенол:
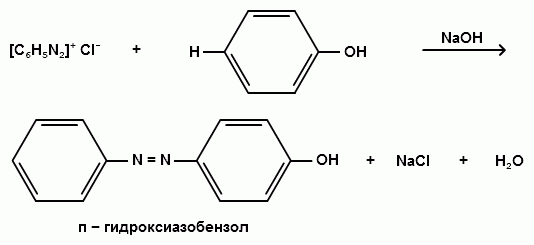
8) Реакции конденсации
Фенолы являются столь активными компонентами в реакциях электрофильного замещения, что вступают во взаимодействие с весьма слабыми электрофилами – альдегидами и кетонами в присутствии кислот и оснований.
Конденсация с формальдегидом
Наиболее легко вступает в реакции конденсации формальдегид.
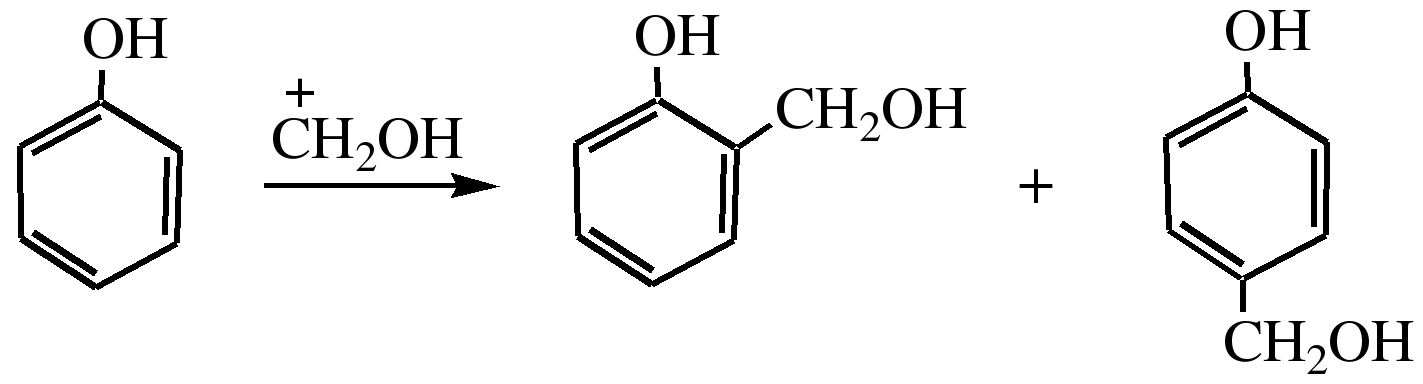
Если реакцию конденсации фенола с формальдегидом проводить в мягких условиях, то удается выделить орто- и пара-гидроксиметилфенолы:
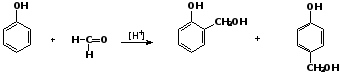
орто-гидрокси- пара-гидрокси-
метилфенол метилфенол
В этой реакции электрофильным реагентом является гидроксиметил-катион, который образуется при протонировании формальдегида:

При избытке формальдегида можно получить ди- и тригидрокси-метилфенолы:

2,6-дигидроксиметилфенол 2,4-дигидроксиметилфенол

2,4,6-тригидроксиметилфенол
Образовавшиеся гидроксиметилфенолы в присутствии кислот могут реагировать с фенолом с получением дигидроксидифенилметана:

2,2-дигидроксидифенилметан
В более жестких условиях фенол с формальдегидом образует высокомолекулярные продукты поликонденсации – фенол-формальдегидные смолы (фенопласты):


Механизм реакции
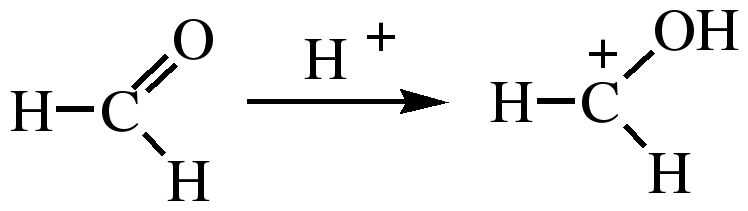

Конденсация с кетонами
При конденсации фенола с ацетоном в присутствии катализатора образуется дигидроксидифенилпропан (торговое название – бисфенол А), который используют для производства эпоксидных смол:


4,4-дигидроксидифенилпропан
бисфенол А
Конденсация с ароматическими альдегидами
Конденсация фенолов с ароматическими альдегидами лежит в основе получения некоторых важных красителей трифенилметанового ряда:

