
- •Фенолы – органические соединения, содержащие в молекуле гидроксильную группу, связанную непосредственно с бензольным
- •НОМЕНКЛАТУРА
- •ИЗОМЕРИЯ
- •Изомерия двухатомных фенолов
- •2. Получение из хлорбензола.
- •3. Получение из солей сульфокислот.
- •Физические свойства
- •Химические свойства
- •Введение в бензольное кольцо электроноакцепторных заместителей (нитрогруппы, галогенов и др.)
- •2. Взаимодействие со щелочами.
- •4. Гидрирование.
- •Нитрование фенола
- •Взаимодействие фенола с серной кислотой
- •Галогенирование фенола
- •Качественная реакция на фенол - взаимодействие с FeCl3
- •Анилин – первичный ароматический амин
- •Изомерия
- •Получение
- •Химические свойства
- •Образование солей.
- •Реакции электрофильного замещения.
- •Cульфирование анилина
- •МНОГОЯДЕРНЫЕ (ПОЛИЦИКЛИЧЕСКИЕ) АРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ
- •Трифенилметан
- •СОЕДИНЕНИЯ С КОНДЕНСИРОВАННЫМИ БЕНЗОЛЬНЫМИ ЯДРАМИ
- •Реакции замещения
- •Антрацен
- •Антрацен вступает в реакции присоединения и окисления. При этом положения 9 и 10
- •При окислении антрацена образуется антрахинон
- •Самым первым и известным красителем этого ряда был 1,2 – дигидроксиантрахинон – ализарин:
- •Фенантрен

Фенолы – органические соединения, содержащие в молекуле гидроксильную группу, связанную непосредственно с бензольным ядром:
OH
НОМЕНКЛАТУРА
Фенолы называют тривиальными названиями:
фенол С6H5OH, крезол H3C – C6H4 – OH
Или по систематической номенклатуре, добавляя суффикс – ол к названию арена
OH
ã è ä ð î ê ñ è á å í ç î ë è ë è ô å í î ë

ИЗОМЕРИЯ
Метильному гомологу фенола соответствуют 3 изомера:
OH |
OH |
OH |
|
CH3 |
|
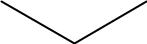
 CH3
CH3
CH3
о-крезол |
м-крезол |
n-крезол |
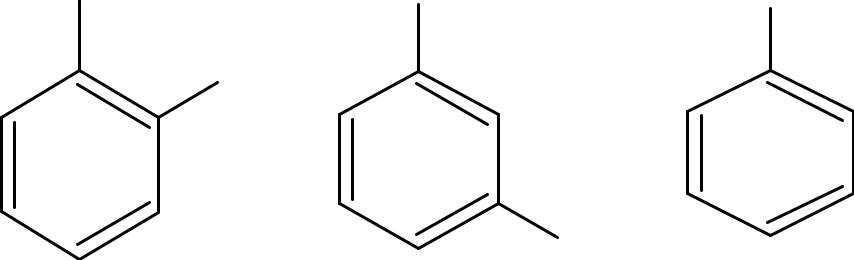
Изомерия двухатомных фенолов
OH |
OH |
OH |
|
OH |
|
|
|
OH |
|
|
|
|
|
||
|
|
|
|
|
пирокатехин |
резорцин |
OH |
||
гидрохинон |
||||
1,2- |
1,3- |
1,4- |
|
|
дигидроксибензол |
дигидроксибензол |
дигидроксибензол |
||
(бензендиол-1,2) |
(бензендиол-1,3) |
(бензендиол-1,4) |
||
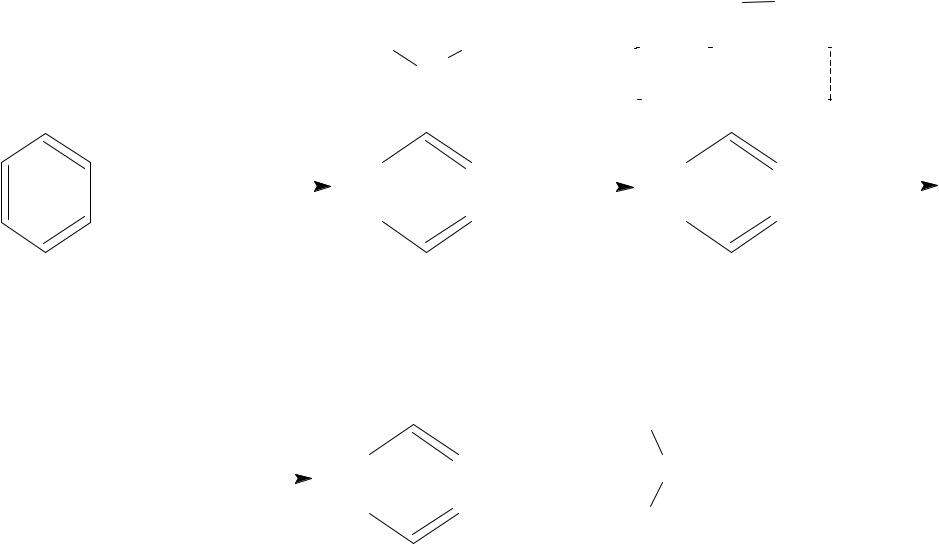
ие
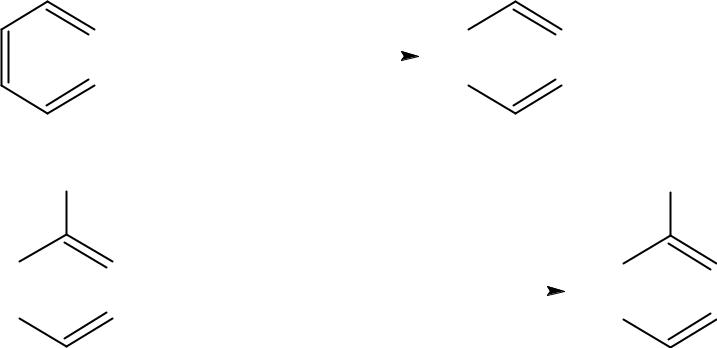
1. Получение из бензола и пропилена (П.Г. Сергеев и др., 1947).
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
||||||||||||
H3C |
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
CH |
|
|
|
|
|
H3C |
|
|
|
|
|
|
|
|
|
C |
|
|
|
|
|
|
|
|
|
CH3 |
||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Ñ H 3 |
|
C H |
|
|
C H 2 |
|
|
|
|
|
|
|
[ O ] |
|
|
|
|
|
|
|
|
H 2 S O 4 |
|||||
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
A l C l 3 , T , p |
|
|
|
|
|
|
|
|
|
|
|
1 1 0 - 1 3 0 0 C |
|
|
|
|
|
|
|
7 0 0 C |
||||||
|
ê ó ì î ë |
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
ã è ä ð î ï å ð î ê ñ è ä |
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ê ó ì î ë à |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H3C |
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
|
O |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
+ |
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H3C |
|
|
|
|
|
|
||||
|
|
|
|
|
|
ô å í î ë |
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
à ö å ò î í |
|
|
|
|
|
|
||||||||||||

2. Получение из хлорбензола.
Реакцию замены хлора на гидроксильную группу проводят в жестких условиях (300°С, давление 200 МПа):
Cl |
OH |
+ |
N a O H |
|
|
|
|
+ |
N a C l |
|
|
|
|
||||
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3. Получение из солей сульфокислот.
Соли сульфокислот сплавляют со щелочами при 320-3500C:
|
|
SO3Na |
|
ONa |
|
|
|||
|
|
|
|
|
|
+ |
N a O H |
|
|
|
|
+ |
N a 2 S O 3 + |
H 2 O |
|
|
|
|
|
|||||
|
|
|
|
ô å í î ë ÿ ò í à ò ð è ÿ |
|
|
|||
ONa |
|
|
|
|
|
|
OH |
|
|
2 |
|
|
+ |
S O 2 |
+ |
H 2 O |
|
2 |
|
|
+ |
N a 2 S O 3 |
|
|
|
|
|
||||||||
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
Физические свойства
Фенол – кристаллическое вещество, трудно растворимое в воде.
С увеличением числа гидроксильных групп
растворимость некоторых фенолов в воде
увеличивается.
Фенолы – ядовитые вещества.
Обычный фенол (карболовая кислота)
– сильный антисептик.
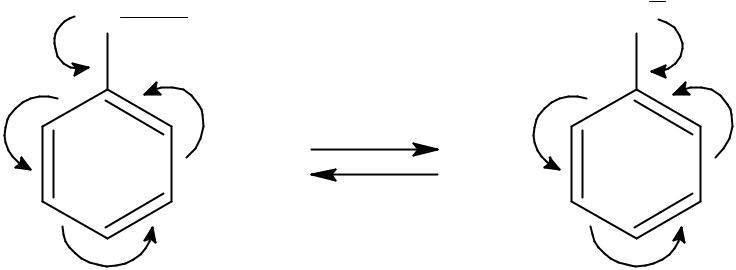
Химические свойства
1. Кислотные свойства.
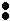 O
O H O
H O
+ |
H + |
Фенолы – слабые кислоты, но превосходят по кислотности спирты.
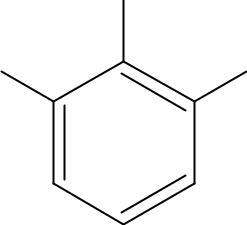
Введение в бензольное кольцо электроноакцепторных заместителей (нитрогруппы, галогенов и др.)
вызывает усиление кислотных свойств фенола. Тринитрофенол (пикриновая кислота) является сильной кислотой
OH
O2N |
NO2 |
|
|
|
|
|
|
NO2 |
|
2 |
, 4 , 6 |
- ò ð è í è ò ð î ô å í î ë |
|
2 - ã è ä ð î |
ê ñ è |
- 1 , 3 , 5 - ò ð è í è ò ð î á å í ç î ë |
|
