
- •Основы биологической химии предисловие
- •Введение Предмет и задачи биохимии
- •Основные признаки живой материи
- •Глава 1. Химический состав организмов
- •Глава 2. Структура и свойства белков
- •2.1. Роль и определение белков.
- •2.2. Функции белков в организме
- •2.3. Элементный состав белков. Содержание белков в органах и тканях
- •2.4. Аминокислотный состав белков
- •2.5. Кислотно-основные свойства аминокислот
- •2.6. Стереохимия аминокислот
- •2.7. Строение белков
- •2.8. Уровни структурной организации белков
- •Первичная структура
- •Вторичная структура белков
- •Третичная структура белков
- •Четвертичная структура белков
- •2.9. Физико-химические свойства белков
- •Кислотно-основные свойства белков
- •Растворимость белков
- •Денатурация и ренатурация
- •2.10. Классификация белков
- •2.11. Методы выделения и очистки белков
- •Очистка белков
- •Глава 3. Углеводы
- •3.1. Понятие об углеводах и их классификация
- •3.2. Моносахариды
- •Оптические свойства моносахаридов
- •Структура моносахаридов
- •3.3. Химические свойства моносахаридов Реакции с участием карбонильной группы
- •Реакции с участием гидроксильных групп
- •3.4. Сложные углеводы
- •Олигосахариды
- •Полисахариды
- •Гомополисахариды
- •Гетерополисахариды
- •3.5. Биологические функции углеводов
- •Глава 4. Нуклеиновые кислоты
- •4.1. Общая характеристика нуклеиновых кислот
- •4.2. Химический состав и строение нуклеиновых кислот
- •4.3. Уровни структурной организации нуклеиновых кислот
- •Первичная структура нуклеиновых кислот
- •Вторичная структура днк
- •Вторичная структура рнк
- •Третичная структура рнк и днк
- •Глава 5. Липиды
- •5.1. Общая характеристика и классификация липидов
- •5.2. Липидные мономеры
- •5.3. Многокомпонентные липиды
- •5.4. Биологические функции липидов
- •Глава 6. Ферменты
- •6.2. Химическая природа и структура ферментов
- •6.3. Кофакторы ферментов Ионы металлов как кофакторы ферментов
- •Коферменты
- •6.4. Механизм действия ферментов
- •6.5. Свойства ферментов
- •6.6. Специфичность действия ферментов
- •6.7. Факторы, влияющие на скорость ферментативного катализа
- •Влияние температуры на активность ферментов
- •Влияние рН на активность ферментов
- •Влияние концентраций субстрата и фермента на скорость ферментативной реакции
- •Зависимость скорости реакции от времени
- •6.8. Регуляция активности ферментов
- •Активация ферментов
- •Ингибирование ферментов
- •Аллостерическая регуляций действия ферментов
- •6.9. Определение активности ферментов
- •6.10. Номенклатура и классификация ферментов
- •6.11. Локализация ферментов в организме и клетке
- •6.12. Применение ферментов
- •Глава 7. Витамины
- •7.1.Понятие о витаминах
- •7.2. Классификация витаминов
- •7.3. Жирорастворимые витамины
- •7.4. Водорастворимые витамины
- •7.5. Витаминоподобные вещества
- •Глава 8. Общие закономерности обмена веществ и энергии в организме
- •8.1. Обмен веществ
- •8.2. Обмен энергии
- •Глава 9. Биологическое окисление
- •9.2. Дыхательная цепь
- •9.3. Окислительное фосфорилирование
- •Глава 10. Обмен углеводов
- •10.1. Переваривание углеводов
- •10.2. Метаболизм глюкозы
- •10.3. Биосинтез гликогена
- •10.4. Распад гликогена
- •10.5. Анаэробный гликолиз
- •10.6. Аэробный распад глюкозы
- •Аэробный распад глюкозы в мозге
- •10.7. Пентозофосфатный цикл
- •10.8. Биосинтез глюкозы (глюконеогенез)
- •10.10. Регуляция обмена углеводов
- •Глава 11. Обмен липидов
- •11.1. Переваривание липидов
- •11.2. Метаболизм глицерина
- •11.3. Метаболизм жирных кислот
- •11.4. Биосинтез жиров
- •11.5. Регуляция обмена липидов
- •Глава 12. Обмен нуклеиновых кислот
- •12.1. Пути распада рнк и днк
- •12.2. Распад пуриновых и пиримидиновых оснований
- •12.3. Биосинтез нуклеотидов
- •Биосинтез пурииовых нуклеотидов
- •Биосинтез пиримидиновых нуклеотидов
- •Биосинтез дезоксирибонуклеотидов
- •12.4. Биосинтез нуклеиновых кислот
- •Биосинтез днк (репликация)
- •Биосинтез рнк (транскрипция)
- •Безматричный синтез рнк
- •12.5. Путь информации от генотипа к фенотипу
- •Глава 13. Обмен белков
- •13.1. Понятие об обмене белков
- •13.2. Переваривание белков пищи и распад белков тканей Переваривание белков
- •Распад белков в тканях
- •13.3. Метаболизм аминокислот
- •Трансаминирование аминокислот
- •Дезамииирование аминокислот
- •Превращение углеродных скелетов аминокислот. Реакции декарбоксилирования
- •13.4. Удаление аммиака из организма. Орнитиновый цикл
- •13.5. Синтез аминокислот
- •13.6. Биосинтез белков (трансляция)
- •Глава 14. Водно-солевой и минеральный обмен
- •14.1. Водно-солевой обмен Содержание воды в организме и клетке
- •Роль и функции воды в процессе жизнедеятельности
- •14.2. Регуляция водно-солевого обмена
- •Регуляция рН
- •14.3. Минеральный обмен Минеральные вещества
- •Функции минеральных веществ
- •Минеральные вещества и обмен нуклеиновых кислот
- •Минеральные вещества и обмен белков
- •Минеральные вещества и обмен углеводов и липидов
- •14.4. Регуляция минерального обмена
- •Глава 15. Взаимосвязь обмена белков, жиров, углеводов и нуклеиновых кислот
- •Глава 16. Гормоны, нервно-гормональная регуляция обмена веществ
- •16.1. Понятие о гормонах. Основные принципы регуляции обмена веществ
- •16.2. Классификация гормонов
- •16.3. Общие представления о действии гормонов
- •16.4. Гормоны щитовидной и паращитовидных желез Гормоны щитовидной железы
- •Гормоны паращитовидных желез
- •16.5. Гормоны поджелудочной железы
- •16.6. Гормоны надпочечников
- •16.7. Гормоны половых желез
- •16.8. Гормоны гипоталамо-гипофизарной системы
- •16.9. Гормоны тимуса и эпифиза
- •16.10. Простагландины
- •16.11. Биохимическая адаптация
- •Рекомендуемая литература
- •Оглавление
10.5. Анаэробный гликолиз
Анаэробный гликолиз - сложный ферментативный процесс последовательных превращений глюкозы, протекающий в тканях человека и животных без потребления кислорода (рис.28).
Обратимое превращение пировиноградной кислоты в молочную катализируется лактатдегидрогеназой:
![]()
-
Пировиноградная кислота
Молочная кислота
Суммарный результат гликолиза выражается следующим уравнением: С6Н12О6 + 2Н3РО4 + 2АДФ = 2С3Н6О3 + 2АТФ + 2Н2О
-
Глюкоза
Молочная кислота
Таким образом, чистый выход АТФ при анаэробном гликолизе - 2 моль АТФ на 1 моль глюкозы. Именно благодаря анаэробному гликолизу организм человека и животных может определенный период времени осуществлять ряд физиологических функций в условиях недостаточности кислорода.
Данный процесс у бактерий называют молочнокислым брожением: он лежит в основе приготовления кисломолочных продуктов. Анаэробный гликолиз протекает в цитозоле клеток, где содержатся все необходимые для этого ферменты, и не нуждается в митохондриальной дыхательной цепи. АТФ в процессе анаэробного гликолиза образуется за счет реакций субстратного фосфорилирования.
У дрожжей в анаэробных условиях происходит сходный процесс - спиртовое брожение, в этом случае пировиноградная кислота декарбоксилируется с образованием уксусного альдегида, который затем восстанавливается в этиловый спирт:
СН3-СО-СООН → СН3-СНО + СО2;
СН3-СНО + НАД.Н+Н+ → СН3-СН2-ОН + НАД+.
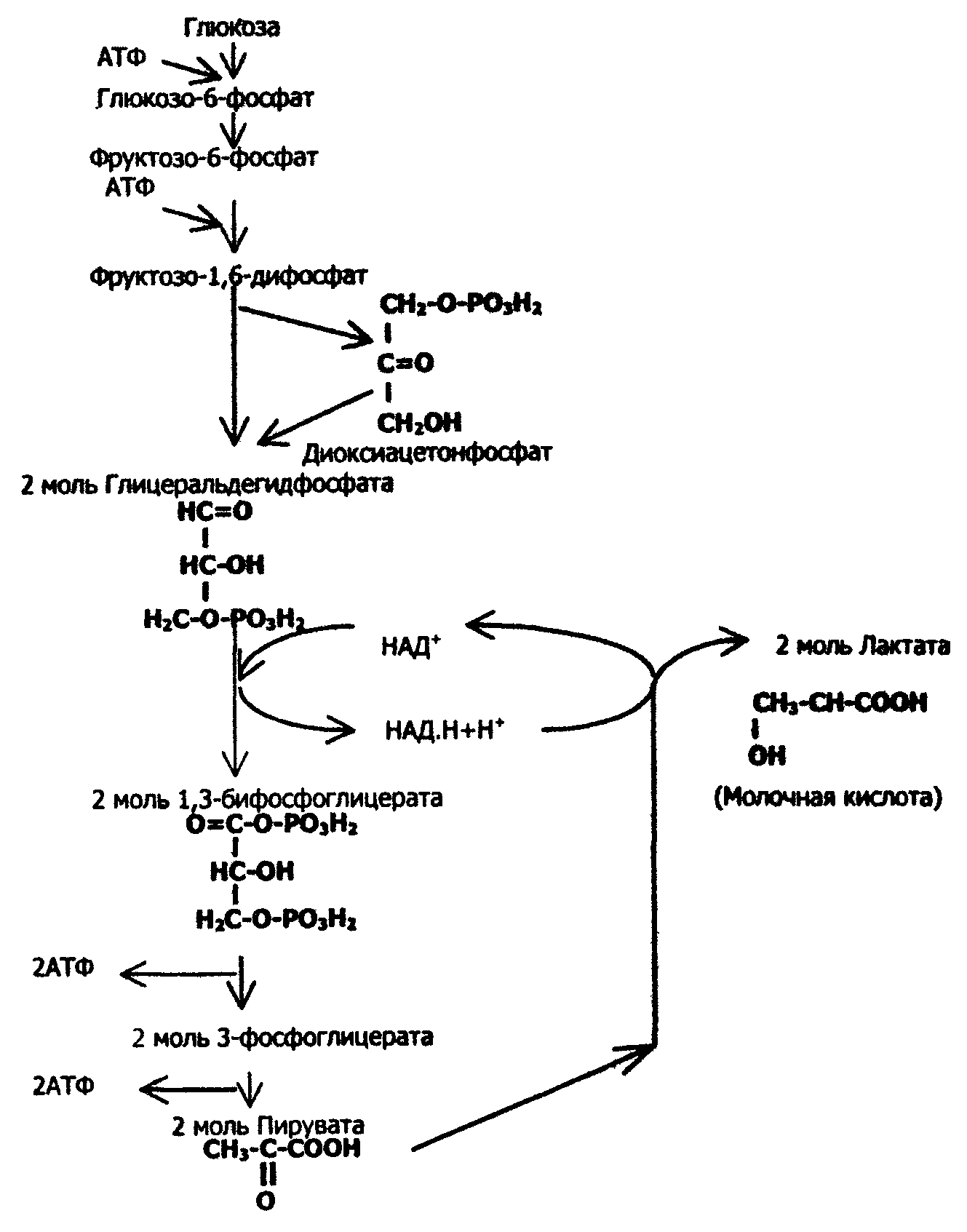
Рис.28. Схема анаэробного гликолиза глюкозы
10.6. Аэробный распад глюкозы
Аэробный распад глюкозы включает в себя три стадии:
1) превращение глюкозы до пировиноградной кислоты (пирувата) - аэробный гликолиз. Эта часть аналогична рассмотренному выше процессу анаэробного гликолиза, за исключением его последней стадии (превращение пирувата в молочную кислоту);
2) общий путь катаболизма;
3) митохондриальная цепь переноса электронов - процесс тканевого дыхания.
Общий путь катаболизма
Общий путь катаболизма сострит из двух этапов.
1-й этап - окислительное декарбоксилирование пировиноградной кислоты. Это сложный многостадийный процесс, катализируемый мультиферментной системой - пируватдегидрогеназным комплексом; локализуется в митохондриях (внутренняя мембрана и матрикс) и может быть выражен суммарной общей схемой:
СН3-СО-СООН + HS-KoA + НАД+ → CH3-CO-SkoA + НАД.Н+Н+ + СО2.
|
пируват |
коэнзим А |
ацетил-КоА |
2-й этап - цикл Кребса (цитратный цикл, или цикл трикарбоновых и дикарбоновых кислот) (рис. 29); локализуется в митохондриях (в матриксе). В этом цикле ацетильный остаток, входящий в ацетил-КоА, образует ряд первичных доноров водорода. Далее водород при участии дегидрогеназ поступает в дыхательную цепь. В результате сопряженного действия цитратного цикла и дыхательной цепи ацетильный остаток окисляется до СО2 и Н2О. Суммарное уравнение всей последовательности превращений глюкозы в ходе аэробного распада следующее:
С6Н12О2 + 6О2 → 6СО2 + 6Н2О
Энергетический эффект аэробного распада - синтез 38 молекул АТФ при расщеплении 1 молекулы глюкозы. Таким образом, в энергетическом отношении полное окисление глюкозы до углекислого газа и воды является более эффективным процессом, чем анаэробный гликолиз. Кислород тормозит анаэробный гликолиз, поэтому в присутствии избытка кислорода наблюдается переход в растительных и животных тканях от анаэробного гликолиза (брожения) к дыханию (аэробный гликолиз), т.е. переключение клеток на более эффективный и экономичный путь получения энергии (эффект Пастера). Роль анаэробного гликолиза в обеспечении организма энергией особенно велика при кратковременной интенсивной работе, когда мощности механизма транспорта кислорода к митохондриям недостаточно для обеспечения аэробного гликолиза. Так, бег в течение ~ 30 секунд (на 200 м) полностью обеспечивается анаэробным гликолизом, при этом скорость анаэробного гликолиза с учащением дыхания уменьшается, а скорость аэробного распада увеличивается. Через 4-5 мин. бега (1,5 км) - половину энергии дает анаэробный, половину аэробный процесс. Через 30 мин. (10 км бега) - энергия поставляется почти целиком аэробным процессом.
Эритроциты вообще не имеют митохондрий, и их потребность в АТФ полностью удовлетворяется за счет анаэробного гликолиза.
