
- •Федеральное агентство по образованию
- •Биохимия
- •В.В. Шапкарин, а.П. Королев, с.Б. Гридина, е.П. Зинкевич
- •Оглавление
- •Глава 1. Методы исследования в биохимии………………………………….…4
- •Глава 2. Белки и аминокислоты…………………………………………………8
- •Глава 3. Ферменты………………………………………………………………..35
- •Глава 4. Углеводы и их обмен…………………………………………………...56
- •Глава 5. Белки и их обмен ……………………………………………………….62
- •Глава 6. Липиды и их обмен ……………………………………………………..63
- •Глава 7. Витамины ………………………………………………………………..71
- •Введение
- •Глава 1. Методы исследования в биохимии
- •1.1. Указания к выполнению лабораторных работ
- •Глава 2. Белки и аминокислоты
- •2.1. Цветные реакции на белки и аминокислоты
- •Цветные реакции на белки и аминокислоты
- •2.2. Методы количественного определения белка
- •Определение белкового азота методом кьельдаля
- •Разведение стандартного раствора белка
- •2.3. Выделение белков из биологических объектов
- •2.4. Реакции осаждения белков
- •Осаждение белков при нагревании
- •Осаждение белков при нагревании
- •Осаждение белков минеральными кислотами
- •Осаждение белков солями тяжелых металлов
- •2.5. Разделение смеси аминокислот методом хроматографии на бумаге
- •Глава 3. Ферменты
- •3.1. Выделение ферментов и обнаружение их действия
- •Продукты гидролиза крахмала
- •Выделение амилаз из солода
- •Выделение сахаразы из дрожжей
- •3.2.Специфичность действия ферментов
- •3.3. Сравнение действия неорганических катализаторов и ферментов
- •3.4. Факторы, влияющие на скорость ферментативных реакций (на активность ферментов)
- •3.5. Выделение α- и β- амилаз из солода и определение их активности
- •3.6. Определение активности амилаз по Вольгемуту
- •3.7. Влияние активаторов и ингибиторов на активность ферментов
- •3.8. Определение активности каталазы (по а.Н. Баху и а.И. Опарину)
- •Глава 4. Углеводы и их обмен
- •4.1 Действие амилазы на сырой и вареный крахмал
- •4.2. Анаэробное окисление углеводов
- •Глюкоза
- •О алкогольдегидрогеназа
- •Глава 5. Белки и их обмен
- •5.1. Определение активности протеаз (по методу Ансона)
- •Глава 6. Липиды и их обмен
- •6.1. Определение йодного числа жира (методом Гануса)
- •6.2.Определение кислотного числа жира
- •6.3. Определение активности липазы клещевины
- •Глава 7. Витамины
- •7.1. Качественные реакции на витамин а
- •7.2. Качественные реакции на витамин д
- •7.3. Качественная реакция на витамин в1 (с диазореактивом)
- •7.4. Качественная реакция на витамин в2
- •7.5. Качественная реакция на витамин (в5) рр
- •7.6. Качественная реакция на витамин с
- •7.7. Количественное определение витамина с
- •Библиографический список
- •Биохимия
- •650056, Г. Кемерово, б-р Строителей, 47
- •650010, Г. Кемерово, ул. Красноармейская, 52
7.2. Качественные реакции на витамин д
Витамин Д – группа соединений, принимающих участие в регуляции форфорно-кальциевого обмена и процесса образования костей. Не растворим в воде, растворяется в жирах и органических растворителях.
Этот витамин можно рассматривать как производное циклических спиртов – эргостерола и 7-дегидростерола, являющихся его провитаминами. Превращение названных провитаминов в витамин Д происходит под действием ультрафиолетовых лучей.
Источниками витамина Д для человека служат: рыбий жир, печень, молоко, сливочное масло, желток яиц.
7.2.1.РЕАКЦИЯ С АНИЛИНОМ. В сухой пробирке смешивают 4 капли рыбьего жира или раствора витамина Д в масле с 20 каплями хлороформа, добавляют при помешивании 10 капель смеси анилина с концентрированной соляной кислотой. Пробирку ставят на кипящую водяную баню на 30-60 секунд. При нагревании содержимое пробирки приобретает красную окраску.
7.2.2. РЕАКЦИЯ С БРОМОМ. В сухую пробирку вносят 5 капель рыбьего жира или раствора витамина Д в масле, добавляют 5 капель раствора брома в хлороформе и перемешивают. Смесь в пробирке постепенно окрашивается в зелено-голубой цвет.
РЕАКТИВЫ. Рыбий жир или раствор витамина А в масле; раствор витамина Д в масле; хлороформ; концентрированная серная кислота; уксусная кислота ледяная; сульфат железа (II); 1 % раствор хлорного железа; смесь анилина с концентрированной соляной кислотой (15:1 по объему); раствор брома в хлороформе (1:60 по объему); насыщенный раствор сульфата меди в ледяной уксусной кислоте.
КОНТРОЛЬНЫЕ ВОПРОСЫ.
1. Общая характеристика роли витаминов.
2. Источники витаминов для человека и животных.
3. Классификация витаминов.
4. Биологическая роль водорастворимых витаминов.
5. Биологическая роль жирорастворимых витаминов.
6. Что происходит в организме человека при отсутствии или недостатке витаминов в пище?
7. Использование витаминов в пищевой промышленности.
8. Качественные реакции на витамин А.
9. Качественные реакции на витамин Д.
10. Источники витаминов А и Д. Провитамины.
7.3. Качественная реакция на витамин в1 (с диазореактивом)
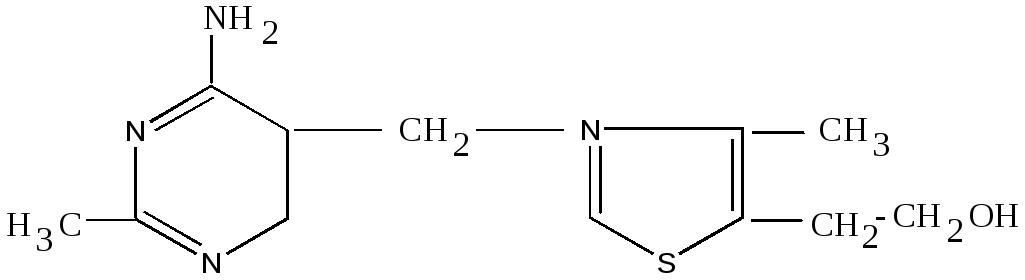
Пиримидиновый Тиазоловый
цикл цикл
В связи с наличием в молекуле атома серы и аминогруппы этому витамину было дано химическое название тиамин. Тиамин в форме тиаминпирофосфата выполняет коферментные функции в реакциях декарбоксилирования -кетокислот и в транскетолазной реакции.
Источником тиамина для человека служат, главным образом, хлеб и крупы, но в тех случаях, когда в процессе переработки зерна не происходит удаление зародышей и оболочек, которые в основном и содержат этот витамин. Очень много тиамина в пекарских и пивных дрожжах. В щелочной среде тиамин легко превращается в тиамин-тиол, который с диазореактивом образует сложное комплексное соединение красного или розово-оранжевого цвета.
Реакция не специфична, так как подобную окраску с диазореактивом дают вещества, имеющие в своей структуре фенольные, имидазольные, пиррольные, тиазольные группы (адреналин, карнозин, желчные пигменты, гистамин и др.).
РЕАКТИВЫ. Вода дистиллированная; тиамин (порошок или свежий раствор с массовой долей тиамина 0,1 %); молоко цельное свежее; раствор сульфаниловой кислоты (в мерную колбу вместимостью 100 мл вносят 1 г сульфаниловой кислоты, 4,6 мл концентрированной соляной кислоты и, растворяя, добавляют воду до метки); свежие растворы с массовыми долями: нитрита натрия 5 %, карбоната натрия 10 %.
