
899-materialovedenie-560kb
.pdfЛабораторная работа 3
ТИПИЧНЫЕ МИКРОСТРУКТУРЫ СПЛАВОВ ДВОЙНЫХ СИСТЕМ
(2 часа)
Цель работы – получение навыков металлографического анализа сплавов – твердых растворов и систем эвтектического типа с использованием диаграмм состояния.
3.1. Теоретическое введение
Микроструктура сплава формируется в процессах кристаллизации расплава, фазовых превращений и структурных изменений в твердом состоянии, происходящих при литье, обработке давлением и термической обработке.
Несмотря на многообразие факторов, влияющих на формирование микроструктуры сплава, важнейшие ее особенности можно предсказать, используя диаграмму состояния, так как именно диаграмма состояния дает сведения о характере фазовых превращений и их последовательности при нагревании и охлаждении сплава. Вместе с тем, следует твердо помнить, что диаграмма состояния описывает фазовое состояние в равновесных условиях, а реальная структура сплава складывается в неравновесных условиях. Поэтому с помощью диаграмм состояния можно анализировать формирование структуры только в медленно охлажденных или отожженных сплавах, в которых отклонения от фазовых равновесий невелики.
Сплавы – твердые растворы
Закономерности формирования микроструктуры однофазного сплава – твердого раствора в условиях равновесной кристаллизации – проанализируем, используя диаграмму состояния двойной системы с неограниченной растворимостью компонентов в жидком и твердом состояниях (рис. 3.1).
Сплав n1 на кривой охлаждения имеет две критические точки. Выше температуры Т1 сплав представляет из себя ненасыщенный жидкий раствор. Процесс кристаллизации необходимо рассматривать с температуры, превышающей Т1. До температуры Т1 происходит охлаждение
30

жидкости состава сплава n1. При понижении температуры до Т1 происходит насыщение жидкости относительно α-кристаллов, и складываются все условия для начала кристаллизации α-фазы. При переохлаждении ниже Т1 из жидкости состава 1 выделяются α-кристаллы состава 2. По своему химическому составу первые α-кристаллы (состава 2) отличаются от исходной жидкости и обогащены атомами компонента А, повышающего температуру солидуса. Следовательно, началу кристаллизации предшествует разделительная диффузия в жидкой фазе, т.е. перераспределение атомов компонентов на фронте кристаллизации, и эта разница в составах жидкости и α-кристаллов существует во всем интервале кристаллизации.
|
|
|
|
|
|
|
|
|
|
A |
T |
|
|
|
|
|
|
|
T n1 |
|
L |
|
|
|
|
|
|
|
|
L + A |
||
A |
|
|
|
|
|
|
|
TA ’ |
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
L |
|
|
|
L |
A |
T1 |
|
1 |
|
|
|
T1 |
|
|||
2 |
|
n |
3 |
|
|
L + |
|
|||
T2 |
|
|
|
|
|
|
||||
|
4 |
|
|
|
|
|
|
|
||
T3 |
|
|
|
5 |
|
|
T3 |
|
|
|
|
|
|
|
|
|
|
B |
|||
|
6 |
|
|
|
|
|
||||
|
|
|
L + |
|
|
|
|
|||
|
|
|
|
|
|
|
|
L |
||
|
|
|
|
|
|
|
B |
TB’ |
|
L + B |
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
B |
A |
|
y n1 |
x |
B |
|
|
|
|
||
|
|
|
|
|
B, % |
|
|
|
б |
|
|
|
|
a |
|
|
|
|
|||
|
|
|
|
|
|
|
|
|||
Рис. 3.1. Диаграмма состояния системы с неограниченной растворимостью (а) и кривые охлаждения (б)
Поскольку из жидкости выделяются кристаллы, обогащенные компонентом А, то жидкость при охлаждении должна обогащаться вторым компонентом В. По мере понижения температуры в интервале кристаллизации состав жидкости будет все больше отличаться от состава исходного сплава, а состав α-кристаллов, существенно отличаясь от состава исходной жидкости в первые моменты кристаллизации, наоборот, будет все больше приближаться к составу исходного сплава.
31

В сплаве n1 в интервале кристаллизации Т1 – Т3 из жидкого раствора, состав которого изменяется по линии ликвидуса от точки 1 до точки 5, выделяются кристаллы α-раствора, состав которых изменяется по линии солидуса от точки 2 до точки 6:
−
L1−5 T1 T3 →α2−6.
Такое изменение составов жидкости и α-кристаллов (одновременное обогащение компонентом В) в интервале кристаллизации возможно только за счет изменения их количеств – уменьшения доли жидкости и, наоборот, увеличения доли α-кристаллов, что подчиняется правилу рычага.
При охлаждении от температуры солидуса Т3 до комнатной в сплаве не происходит никаких фазовых превращений, и идет физическое охлаждение α-твердого раствора.
Возвращаясь к сплаву n1, отметим, что на его кривой охлаждения (в координатах температура – время) видны две критические точки (перегибы), отвечающие температурам начала и конца кристаллизации (рис. 3.1, б). На кривых охлаждения компонентов А и В выявляется по одной критической точке в виде горизонтальной площадки (остановки) при температурах их плавления (кристаллизации). Различия в кривых охлаждения сплава n1 и компонентов А и В легко объяснимы с помощью правила фаз. Такое равновесие возможно только при постоянной температуре. Поэтому на кривых охлаждения компонентов А и В температурам их плавления (кристаллизации) отвечают остановки. Аналогичное равновесие L α в сплаве n1 моновариантно (в = к – ф + 1 = 2 – 2 + 1 = 1) и реализуется в интервале температур. Поэтому на кривой охлаждения сплава n1 нет остановки, а имеются два перегиба.
После равновесной кристаллизации структура сплава n1 состоит из кристаллов твердого раствора α, химический состав которых одинаков с составом сплава (рис. 3.2).
Рис. 3.2. Микроструктура сплава n1
32
Качественно аналогичную структуру имеют все однофазные сплавы, а также чистые компоненты. Поэтому по структуре однофазного материала после равновесной кристаллизации нельзя определить, что это – сплавраствор или чистый металл. Форма и размеры зерен не являются специфическими для того или иного сплава, а зависят от условий кристаллизации.
Сплавы двойных систем эвтектического типа
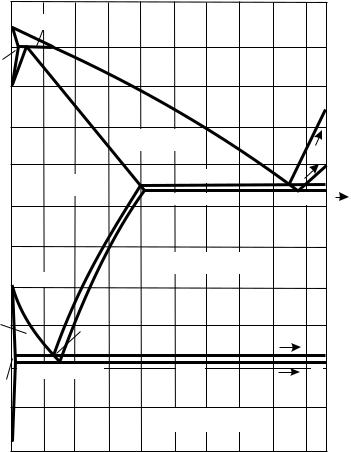
Сплавы участков А – а1 и b1 – В кристаллизуются так же, как и сплавы системы с непрерывными рядами жидких и твердых растворов. На кривых охлаждения эти сплавы имеют по две критические точки (перегибы), отвечающие соответственно температурам начала и конца кристаллизации. Более сложные превращения протекают в сплавах участка а1 – b1 (рис. 3.3).
T |
|
|
|
|
|
|
|
|
|
T |
|
|
|
|
|
A |
L + |
|
|
|
|
|
|
|
|
m |
c |
n1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
T1 |
|
1 |
|
|
|
|
L |
|
|
L |
L |
|
e1 |
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
T1 |
|
L |
|
|
|||
T2 |
2 |
3 |
|
|
|
|
|
|
B T2 |
L + |
|
|
|||
5 |
|
|
|
|
|
|
L |
|
|||||||
T3 |
4 |
|
|
|
L + |
|
|
T3 |
|
L + |
L + |
|
|||
6 |
|
|
|
|
|
|
|
Le a |
b |
||||||
Te |
a |
|
n |
e |
b |
Te |
Le a b |
||||||||
7 |
|
|
|
|
|
|
|
||||||||
T4 |
|
|
8 |
T4 |
|
|
|
|
|
||||||
|
|
|
|
|
+ |
|
|
|
+ |
+ |
|
||||
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
d b1 |
|
|
|
|
|
|
||
A |
a1 m c n1 |
e1 |
|
|
|
|
|
||||||||
|
|
|
|
B, % |
|
|
B |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
||||||
|
|
a |
|
|
|
|
|
б |
|
|
|
|
|||
Рис. 3.3. Диаграмма состояния системы эвтектического типа (а) и кривые охлаждения (б)
В интервале температур (Т1 – Т3) сплав m кристаллизуется как граничный α-раствор (L1–5 α2–6) и при охлаждении до температуры Т4 в нем не протекают фазовые превращения.
При температуре Т4 α-кристаллы состава точки 7 становятся насыщенными относительно β-кристаллов состава точки 8. Поэтому при дальнейшем понижений температуры из первичных α-кристаллов, изменяющих состав по кривой сольвуса аа1 в направлении от точки 7 к точке а1, выделятся вторичные β-кристаллы, состав которых будет изменяться по второй кривой сольвуса bb1 в направлении от точки
−
8 к точке b1, т.е. α7−a1 T4 Tкомн →β8−b1. При комнатной температуре αa1-кристаллы окажутся в равновесии с βb1-кристаллами.
33
На кривой охлаждения сплав m имеет три критические точки (см. рис. 3.3, б): две верхние точки отвечают температурам начала и конца первичной кристаллизации α-раствора, а третья (нижняя) точка – соответственно температуре начала выделения вторичных β-кристаллов из первичных α-кристаллов. Под микроскопом в структуре этого сплава (рис. 3.4) при средних увеличениях можно увидеть две структурные составляющие – первичные α- и вторичные β-кристаллы.
п
вт
Рис. 3.4. Микроструктура сплава m
Обычно вторичные выделения имеют пластинчатую (или игольчатую) форму и в пределах каждого зерна α-фазы кристаллографически ориентированы.
Аналогичные превращения протекают в сплавах участка d – b1 с той только разницей, что в них из жидкости выделяются первичные β-кристаллы, из которых ниже кривой сольвуса bb1 – вторичные α-кристаллы.
В отличие от сплава m кристаллизация сплава с заканчивает-
−
ся при эвтектической температуре ( L3−e T2 Te →α4−a ), когда все первичные α-кристаллы принимают состав точки а, а исчезающая жидкость – соответственно точки e. Поэтому эвтектическая реакция Lе → αa + βb в этом сплаве не протекает.
В момент окончания кристаллизации первичные αа-кристаллы оказываются насыщенными относительно βb-кристаллов, богатых компонентом В. Поэтому при понижении температуры ниже Тe в сплаве с сразу начинается вторичная кристаллизация: из первичных α-кристаллов, изменяющих свой состав по кривой сольвуса aa1 в направлении от точки а к точке а1, выделяются вторичные β-кристаллы, состав которых
изменяется по второй кривой сольвуса bb1 в направлении от точки b к
точке b , т.е. e − комн . При комнатной температуре в этом
1 αa−a1 T T →βb−b1
сплаве в равновесии оказываются αa1- и βb1-кристаллы.
34
На кривой охлаждения сплава с видны две критические точки (см. рис. 3.3, б): верхняя точка отвечает температуре начала, а нижняя (при Тe) – одновременно температурам конца первичной кристаллизации и начала распада α-раствора с выделением из него вторичных кристаллов β-раствора. По структуре этот сплав от предыдущего сплава m будет отличаться только тем, что в нем будет несколько больше вторичных β- и соответственно меньше первичных α-кристаллов.
Вдо- и заэвтектических сплавах помимо первичных α- или β-кристаллов выделяется эвтектика (α + β), а при охлаждении в твердом состоянии – соответственно вторичные β- и α-кристаллы из α- и β-кристаллов разного происхождения.
Вчастности, процесс первичной кристаллизации доэвтектического
−
сплава n1 можно записать как L5−e T3 Te →α6−a . При температуре Тe доли первичных α-кристаллов и оставшейся жидкости Le определятся отношениями отрезков ne/ае и аn/ае. Кристаллизация этого сплава закончится при температуре Тe по эвтектической реакции Lе → αa + βb. По окончании кристаллизации эвтектики сплав n1 оказывается состоящим из первичных α-кристаллов и эвтектики (αa + βb).
Из-за уменьшения взаимной растворимости компонентов в твердом состоянии при понижении температуры из αа- и βb-кристаллов, насыщенных друг относительно друга, начиная с эвтектической температуры Тe, будут выделяться вторичные β- и α-кристаллы.
На кривой охлаждения сплава n1 видны две критические точки (см. рис. 3.3, б): верхняя точка (перегиб) отвечает температуре начала кристаллизации α-раствора, а нижняя (горизонтальная площадка при Те) – температуре кристаллизации эвтектики (α + β) и начала выделения вторичных β- и α-кристаллов из α- и β-кристаллов разного происхождения.
Под микроскопом в структуре этого сплава можно увидеть главным образом три структурные составляющие (рис. 3.5): первичные α-кристаллы, эвтектику (α + β) и выделения вторичных β-кристаллов внутри первичных α-кристаллов.
Аналогично сплаву n1 кристаллизуются другие доэвтектические, а также заэвтектические сплавы.
В эвтектическом сплаве е1 отсутствуют выделения первичных α- или β-кристаллов. Этот сплав кристаллизуется при постоянной температуре Тe в эвтектику, т.е. Lе → αa + βb. При охлаждении до комнатной температуры в сплаве протекает вторичная кристаллизация:
−
αa − a1 ←Te Tкомн →βb −b1.
35

Э( )
п
вт
Рис. 3.5. Микроструктура сплава n1
На кривой охлаждения сплав е1 имеет одну критическую точку – горизонтальную площадку – при температуре Тe (см. рис. 3.3, б), а в структуре – главным образом одну структурную составляющую – эвтектику (α + β) (рис. 3.6).
Э( )
Рис. 3.6. Микроструктура сплава e1
Определение химического состава сплава по его микроструктуре
Если сплав находится в равновесном (отожженном) состоянии и содержит две структурные составляющие, химический состав которых известен из диаграммы состояния, то по микроструктуре можно определить химический состав сплава в целом. Состав однофазного сплава определить по микроструктуре нельзя.
Определим химический состав доэвтектического сплава системы на рис. 3.3. Если плотности первичных кристаллов и эвтектики близки, то соотношение площадей, занимаемых в поле зрения микроскопа структурными составляющими, примерно равно соотношению их масс.
Количество компонента В в доэвтектическом сплаве определится следующим соотношением (% масс.):
36
XB = Fα · a + Fэ · e,
где а и е – концентрация (% масс.) компонента В в первичных кристаллах и эвтектике;
Fα и Fэ – площади первичных кристаллов и эвтектики, выраженные в долях от площади всего поля зрения, принимаемой за единицу. Эти площади оценивают на глаз.
3.2. Порядок проведения работы
Просмотреть шлифы из технического железа и сплавы системы Pb – Sb с эвтектикой при различных увеличениях и схематично зарисовать их микроструктуру при одном увеличении.
3.3. Требования к отчету
Зарисовать микроструктуру технического железа и двойных сплавов системы Pb–Sb. Указать увеличение и структурные составляющие.
Литература
Металловедение / И.И. Новиков, В.С. Золоторевский и др. М.: Изд. дом МИСиС, 2009. Т. 1. С. 79–80, 82–84, 90–92, 96–99, 102–106, 109–113.
Контрольные вопросы
1.Опишите процесс первичной кристаллизации в сплавах – твердых растворах.
2.Какова микроструктура однофазного сплава после равновесной кристаллизации?
3.Как определить долю эвтектики и первичных кристаллов по диаграмме состояния эвтектического типа?
4.Какие структурные составляющие имеют до- и заэвтектические сплавы?
5.Какую структуру может иметь сплав, в котором мало эвтектической жидкости?
6.Можно ли по микроструктуре однофазного сплава определить его химический состав?
7.Опишите изменение составов жидкой и твердой фаз в процессе
охлаждения сплава n1 с температуры выше ликвидуса данного сплава до Ткомн (см. рис. 3.3). Каким компонентом обогащается расплав в процессе первичной кристаллизации?
37
Лабораторная работа 4
МИКРОСТРУКТУРЫ ОТОЖЖЕННЫХ УГЛЕРОДИСТЫХ СТАЛЕЙ И ЧУГУНОВ
(2 часа)
Цель работы – получение навыков металлографического анализа промышленных углеродистых сталей и чугунов в отожженном состоянии.
4.1. Теоретическое введение
При проведении металлографического анализа микроструктуры отожженных сталей и чугунов используют диаграмму состояния железо – углерод (рис. 4.1).
На рис. 4.1 изображены две диаграммы состояния. Одна (сплошные линии) относится к метастабильному равновесию фаз с участием цементита (FезС), другая (пунктирные линии) – к стабильному равновесию фаз с участием графита.
Углерод образует твердые растворы внедрения на базе полиморфных модификаций железа. Твердый раствор углерода в α-Fe называют ферритом (от лат. ferrum – железо) и обозначают (α-Fe). Твердый раствор в δ-Fe называют дельта-ферритом и обозначают (δ-Fe). Феррит и δ-феррит имеют ОЦК решетку. Твердый раствор углерода в γ-Fe называют аустенитом и обозначают (γ-Fe). Аустенит имеет ГЦК решетку.
Предельная растворимость углерода в γ-Fe (2,14 %) на два порядка больше, чем в α-Fe (0,02 %). В ОЦК α-Fe при комнатной температуре растворимость углерода не превышает 0,00005 %.
Карбид железа Fe3C (6,67 % С) имеет ромбическую решетку. Графит имеет гексагональную решетку.
Фазы системы Fe–Fe3C часто обозначают первыми заглавными буквами их названия: L – жидкий раствор, А – аустенит, Ф – феррит, Ц – цементит.
Точка предельной растворимости углерода в γ-Fe при эвтектической температуре E (2,14 % С) – является концентрационной границей, подразделяющей все сплавы системы Fe–С на стали (левее точки E) и белые чугуны (правее точки E). Во всех белых чугунах протекает эвтектическая кристаллизация:
38
T, °C |
|
|
|
|
|
|
|
|
|
|
1539 |
1493° |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1500 |
|
|
|
|
|
|
|
|
|
|
( -Fe) |
J |
|
|
|
|
|
L |
|
|
|
N 1392° |
|
|
|
|
|
|
|
|
|
|
1300 |
|
|
|
|
|
|
|
|
|
D |
|
|
L+( -Fe) |
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
С |
D |
|
|
( -Fe) |
|
E |
|
1153° |
|
|
|||
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
||
1100 |
|
|
|
E 2,14 |
1147° |
С 4,3 |
F |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
( -Fe) + Fe3C |
|
|
|
||
900 G 911° |
|
|
|
|
|
|
|
|
|
|
( -Fe) |
|
S |
|
|
|
|
|
|
|
|
+( -Fe) |
P |
|
|
738° |
|
|
K |
|
||
|
|
|
|
|
|
|
||||
700 |
P0,02 S 0,80 |
|
|
727° |
|
|
K |
|
||
( -Fe) |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
( -Fe) + Fe C |
|
|
|
||
|
|
|
|
|
|
|
3 |
|
|
|
Q |
|
|
|
|
|
|
|
|
|
|
500 0 |
0,5 |
1,0 |
1,5 |
2,0 |
2,5 |
3,0 |
3,5 |
4,0 |
4,5 |
|
Fe |
|
|
|
|
|
C, % масс. |
|
|||
Рис. 4.1. Диаграмма состояния системы железо – углерод |
|
|
||||||||
LC →1147 °C (γ-Fe)E + Fе3СF.
Эвтектоидная точка – S (0,8 % С).
Эвтектоидное превращение протекает во всех сталях и чугунах:
(γ-Fe)S →727 °C (α-Fe)P + Fе3С.
Оно не должно проходить только в очень чистом железе (при содержании углерода менее 0,02 %).
39
