
- •Глава 18. Основы физики атома. Модели атома Томсона и Резерфорда
- •Линейчатый спектр атома водорода
- •Постулаты Бора
- •Спектр атома водорода по Бору
- •Элементы современной (квантовой) физики атомов и молекул Атом водорода в квантовой механике
- •Энергия электрона в водородоподобном атоме
- •Квантовые числа
- •Спектр атома водорода
- •Cпин электрона. Спиновое квантовое число
- •Принцип неразличимости тождественных частиц. Фермионы и бозоны
- •Принцип Паули. Распределение электронов в атоме по состояниям
- •Рентгеновские спектры.
- •Контрольные вопросы.
Спектр атома водорода по Бору
Постулаты Бора позволили рассчитать спектр атома водорода и водородоподобных систем. Водородоподобными называют системы, состоящие из ядра с зарядом Ze и одного электрона (например, ионы He+ , Li2+), где Z – порядковый номер атома в периодической системе электронов.
Решая совместно уравнения для момента импульса электрона
![]() ,
(1)
,
(1)
и
второго закона Ньютона для электрона
массой
![]() и зарядоме,
движущегося по окружности радиуса
и зарядоме,
движущегося по окружности радиуса
![]() под действием кулоновской силы
под действием кулоновской силы
 (2)
(2)
получим
выражение для радиуса
![]() электрона наn-й
орбите
электрона наn-й
орбите
 ;
;  ;
;
 n2
(n
= 1, 2, 3, …). (3)
n2
(n
= 1, 2, 3, …). (3)
Из формулы (1) видно, что радиусы орбит пропорциональны n2 , т.е. квантуются. Для атома водорода (z = 1) радиус первой орбиты электрона называется первым боровским радиусом и равен:
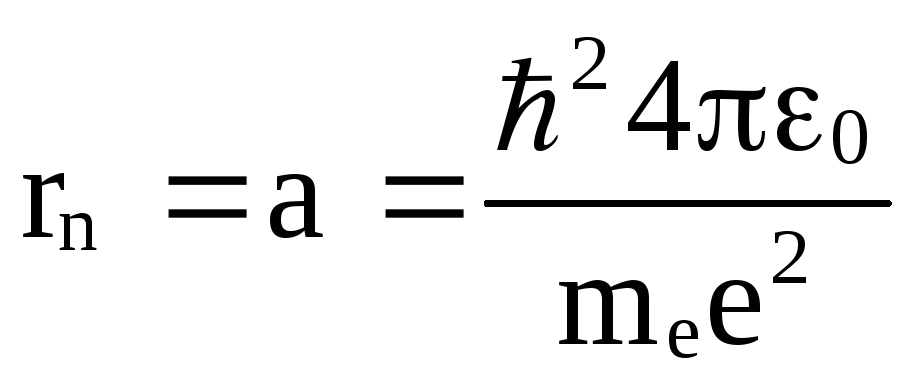 = 0,53 10-10
м
= 0,53 10-10
м
Полная
энергия электрона Е
складывается из его кинетической энергии
(mev2/2)
и потенциальной энергии в электростатическом
поле ядра (![]() ).
).
Е =
![]()
![]() .
.
Из
выражения (1):
![]() =
=![]() . Тогда
Е =
. Тогда
Е =
![]() +
+
![]()
Е
= -![]() .
.
Подставляя квантованные радиусы rn из (3), получим:
 (4)
(4)
Здесь знак минус означает, что электрон находится в атоме в связанном состоянии.
Из формулы (4) следует, что энергетические состояния атома образуют последовательность энергетических уровней, изменяющихся в зависимости от числа n. Это число называют главным квантовым числом. Энергетическое состояние с n = 1 называется основным (нормальным) состоянием; с n > 1 – возбужденными. Энергетический уровень при n = 1 называется основным, все остальные - возбужденными.
Атом
водорода обладает наименьшей
энергией при n
= 1, Е = -13,55 эВ. При n
→∞ (при удалении электрона из атома)
![]() =0.
Энергия Еn
=
=0.
Энергия Еn
=
![]() - E1,
будет энергией ионизации атома.
- E1,
будет энергией ионизации атома.
Согласно 2-му постулату Бора при переходе атома из стационарного состояния с большей энергией Еn в состояние с меньшей энергией Еm испускается квант энергии hν равной Еn-Em
 ,
,
частота излучаемого кванта энергии будет равна
 ,
,
Здесь
R
=
 -
постоянная Ридберга.
-
постоянная Ридберга.
Подставляя в формулу m = 1, n = 2, 3, 4,… получим группу линий серии Лаймана, а при m = 2, n = 3, 4, 5, … - серию Бальмера и т.д. (рис. 173).
Таким образом теория Бора объяснила переход атома в данное состояние из возбужденных состояний, расположенных выше данного, сопровождающееся испусканием соответствующего кванта излучения.
Спектр поглощения атома водорода является линейчатым, но содержит только серию Лаймана. Свободные атомы водорода обычно находятся в основном состоянии (n = 1) с наименьшей энергией. При сообщении атомам извне определенной энергии могут наблюдаться лишь переходы атомов из основного состояния (n = 1) в возбужденные (m = 2, 3, 4, …), что приводит к появлению в спектре поглощения только линий серии Лаймана.
Рис.
173
Элементы современной (квантовой) физики атомов и молекул Атом водорода в квантовой механике
Решение задачи об энергетических уровнях электрона в атоме водорода сводится к задаче о движении электрона в кулоновском поле ядра. Потенциальная энергия U(r) взаимодействия электрона с ядром, обладающим зарядом Z·е, имеет выражение
U(r)
=![]() ,
,
где r – расстояние между электронами и ядром.
С уменьшением r потенциальная энергия U(r) неограниченно убывает (увеличивается по модулю) при приближении электрона к ядру. Графически функция U(r) изображена на рис. 174 непрерывной гиперболической кривой.

Ядро и электроны имеют разные знаки зарядов. Для удаления электрона от ядра требуется работа внешних сил, и тем большая, чем ближе электроны к ядру. Поэтому потенциальная энергия электрона уменьшается (возрастая по абсолютной величине) с приближением электрона к ядру. С другой стороны, за уровень отсчета потенциальной энергии принята потенциальная энергия электрона на бесконечности
U(r)
=![]() ; U(∞)
= 0.
; U(∞)
= 0.
Таким образом, с уменьшением r потенциальная энергия U(r) уменьшается, возрастая по абсолютной величине. Примером обратного свойства является потенциальная энергия тела, поднятого над поверхностью Земли.
