
3 Барометрическая формула
Известно, что
атмосферное давление убывает с высотой.
Найдем функцию
![]() ,
описывающую зависимость давления от
высоты.
,
описывающую зависимость давления от
высоты.
Выделим мысленно
в атмосфере вертикальный столб с
площадью поперечного сечения
![]() ,
равной единице. Атмосферное давление
на высоте
,
равной единице. Атмосферное давление
на высоте![]() обусловлено весом столба воздуха,
который простирается от сечения,
расположенного на данной высоте, до
внешней границы атмосферы. Поэтому
давление с высотой
обусловлено весом столба воздуха,
который простирается от сечения,
расположенного на данной высоте, до
внешней границы атмосферы. Поэтому
давление с высотой![]() убывает. Напомним, что
убывает. Напомним, что![]() означает приращение давления, которое
отличается от убыли знаком. Убыль
давления
означает приращение давления, которое
отличается от убыли знаком. Убыль
давления![]() при переходе от высоты
при переходе от высоты![]() к высоте
к высоте![]() равна весу воздуха, заключенного в
элементе столба высоты
равна весу воздуха, заключенного в
элементе столба высоты![]() :
:
![]() (3.35)
(3.35)
где
![]() - плотность воздуха на высоте
- плотность воздуха на высоте![]() .
.
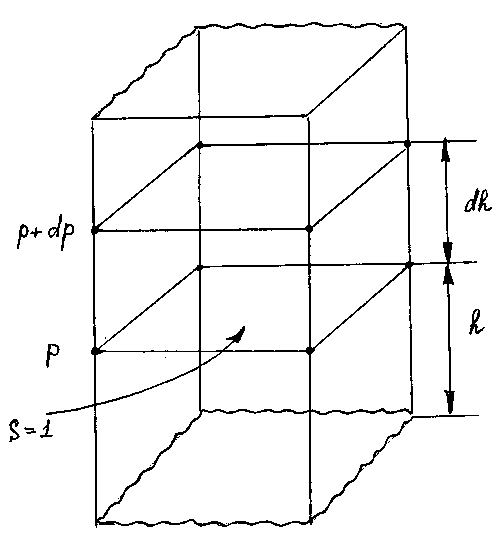
Рис. 8
При условиях,
близких к нормальным (т.е. при
![]() =
1 атм и
=
1 атм и![]() =
00
С) воздух довольно хорошо подчиняется
уравнению состояния идеального газа.
=
00
С) воздух довольно хорошо подчиняется
уравнению состояния идеального газа.
Из уравнения Клапейрона - Менделеева следует, что плотность идеального газа равна
![]() . (3.36)
. (3.36)
Подставим это выражение в формулу (3.35) и получим
![]() . (3.37)
. (3.37)
Здесь
![]() - молярная масса воздуха.
- молярная масса воздуха.
Разделив переменные, придем к дифференциальному уравнению
![]() (3.38)
(3.38)
Для изотермической атмосферы, т.е. для случая, когда температура с высотой не изменяется, интегрирование (3.38) приводит к соотношению:
![]()
или потенцируя, получим
![]() (3.39)
(3.39)
Здесь
![]() - атмосферное давление на высоте
- атмосферное давление на высоте![]() ,
принятой за начало отсчета. Таким
образом, зависимость давления от высоты
,
принятой за начало отсчета. Таким
образом, зависимость давления от высоты![]() описывается формулой (3.39), которая
называетсябарометрической
формулой.
описывается формулой (3.39), которая
называетсябарометрической
формулой.
4 Распределение Больцмана
В формуле (3.39) представим
![]() ,
,
где
![]() - масса молекулы,
- масса молекулы,![]() - постоянная Больцмана,
- постоянная Больцмана,![]() ,
где
,
где![]() - концентрация молекул газа. В результате
придет к соотношению
- концентрация молекул газа. В результате
придет к соотношению
![]() .
.
Таким образом,
![]() (3.40)
(3.40)
Здесь
![]() - плотность молекул или их концентрация
при
- плотность молекул или их концентрация
при![]() ,
,![]() - на высоте
- на высоте![]() .
.
Выражение
![]() представляет собой потенциальную
энергию молекулы
представляет собой потенциальную
энергию молекулы![]() .
.
Поэтому формулу (3.40) можно написать следующим образом:
![]() (3.41)
(3.41)
Л. Больцман доказал, что формула (3.41) справедлива в случае потенциального силового поля любой природы для совокупности любых одинаковых частиц, находящихся в состоянии теплового движения. В связи с этим функцию (3.41) называют распределением Больцмана. Распределение (3.40) – частный случай более общего распределения (3.41).
5 Распределение Максвелла – Больцмана
Между распределениями Больцмана и Максвелла имеется большое сходство.
Возьмем элементарный
объем
![]() ,
расположенный в точке с координатами
,
расположенный в точке с координатами![]() .
Согласно формуле (3.41) в пределах этого
объема находится число молекул
.
Согласно формуле (3.41) в пределах этого
объема находится число молекул
![]() (3.42)
(3.42)
Эта формула обнаруживает еще большее сходство с распределением Максвелла, которое можно представить в виде:
![]() , (3.43)
, (3.43)
где
![]() (см. фор. 3.17).
(см. фор. 3.17).
Заметим, что
кинетическая энергия
![]() равна
равна
![]() .
.
Распределение
(3.42) и (3.43) можно объединить в один закон
Максвелла- Больцмана,
согласно которому число молекул,
компоненты скоростей которых лежат в
пределах от
![]() до
до![]() ,
,![]() ,
,![]() ,
а координаты – в пределах от
,
а координаты – в пределах от![]() до
до![]() ,
,![]() ,
,![]() ,
равно
,
равно
![]() (3.44)
(3.44)
Здесь нормированный
множитель
![]() ,
потенциальная энергия
,
потенциальная энергия![]() ,
кинетическая энергия
,
кинетическая энергия![]() ,
,![]() ,
элемент объема
,
элемент объема![]() .
.
Задачи
Задача 1
Функция
распределения вероятностей
Распределение вероятностей некоторой
величины
![]() описывается формулой
описывается формулой![]() ~
~![]() в интервале
в интервале![]() .
Вне этого интервала
.
Вне этого интервала![]() .
Найти: а) наиболее вероятное и среднее
значения величины
.
Найти: а) наиболее вероятное и среднее
значения величины![]() ;
б) вероятность нахождения
;
б) вероятность нахождения![]() в интервале
в интервале![]() .
.
Решение
а) Наиболее
вероятное значение
![]() соответствует максимуму функции
соответствует максимуму функции![]() .
Из рис. сразу видно, что
.
Из рис. сразу видно, что![]() .
Это случай, не требующий выполнения
условия
.
Это случай, не требующий выполнения
условия
![]() .
.
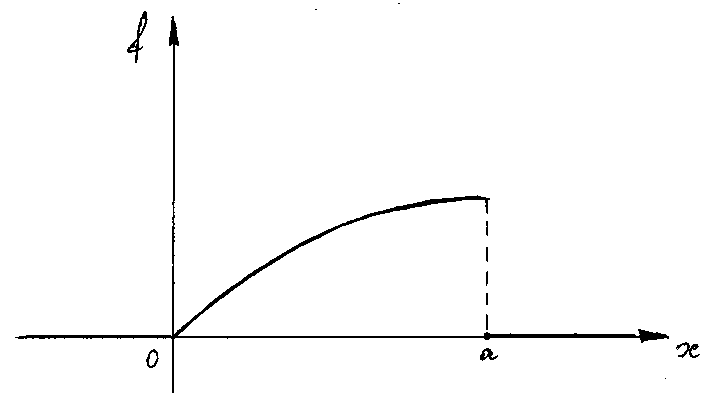
Рис.
Среднее значение
![]() по определению есть
по определению есть
![]() ,
,
где
![]() - нормировочный множитель. Его находим
из условия
- нормировочный множитель. Его находим
из условия
![]() ,
,
откуда
 .
.
В результате
подстановки значения
![]() и интегрирования получим
и интегрирования получим
![]() .
.
б) По определению искомая вероятность
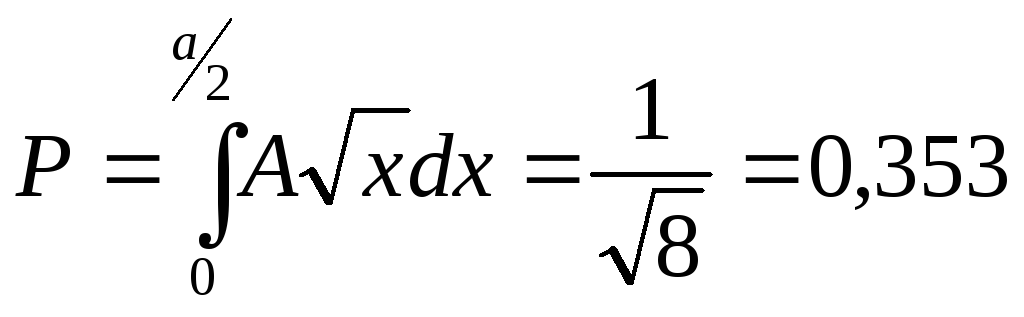 .
.
Задача 2
Распределение
Максвелла
Найти с помощью распределения Максвелла
среднее значение модуля проекции
скорости
![]() ,
если температура газа
,
если температура газа![]() и масса каждой молекулы
и масса каждой молекулы![]() .
.
Решение
По определению искомая величина
![]() (1) Поскольку
интегральная функция всюду положительна
и симметрична относительно начала
координат (
(1) Поскольку
интегральная функция всюду положительна
и симметрична относительно начала
координат (![]() ),
то интеграл (1) можно записать так:
),
то интеграл (1) можно записать так:
![]() (2)
(2)
После подстановки
функции
![]() и
некоторых преобразований получим
и
некоторых преобразований получим
![]() ,
где
,
где
![]() .
Учитывая, что
.
Учитывая, что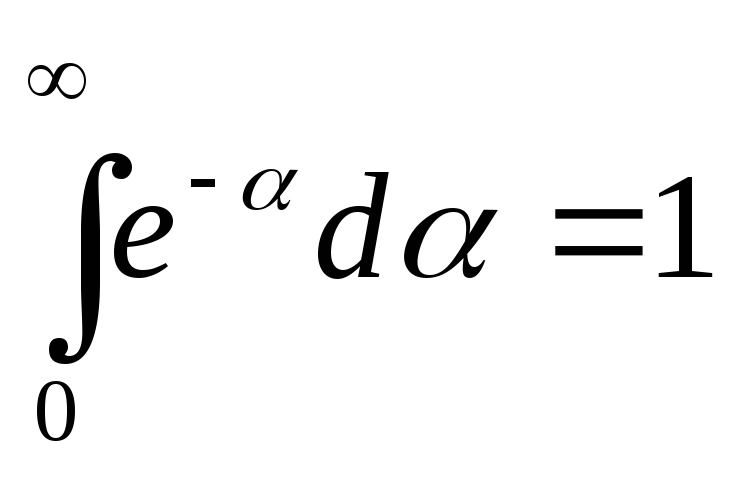 ,
получим
,
получим
![]() .
.
Задача 3
Барометрическая
формула На
какой высоте давление воздуха составляет
75% от давления на уровне моря? Температуру
считать постоянной, равной 00
С. Молярная масса воздуха
![]() =
29·10-3
кг/моль.
=
29·10-3
кг/моль.
Решение
Убывание давления газа с высотой определяется барометрической формулой (3.39)
![]()
или
![]()
Следовательно
![]()
![]() ,
,
![]() м.
м.
Задача 4
Распределение
Больцмана
При наблюдении в микроскоп взвешенных
частиц гуммигута (сгущенного млечного
сока, получаемого из надрезов в коре
некоторых видов деревьев, растущих в
Южной Азии) французский физик Перрен
определил постоянную Больцмана
![]() и постоянную Авогадро
и постоянную Авогадро![]() .
Он обнаружил, что среднее число их в
тонких слоях 1 и 2, расстояние между
которыми по высоте равно
.
Он обнаружил, что среднее число их в
тонких слоях 1 и 2, расстояние между
которыми по высоте равно![]() ,
отличается друг от друга в
,
отличается друг от друга в![]() раз
раз![]() .
Температура среды
.
Температура среды![]() ,
диаметр частиц
,
диаметр частиц![]() и их плотность
и их плотность![]() больше плотности окружающей жидкости.
Найти по этим данным постоянную Больцмана
больше плотности окружающей жидкости.
Найти по этим данным постоянную Больцмана![]() и постоянную Авогадро
и постоянную Авогадро![]() .
.
Решение
Согласно распределению Больцмана отношение частиц в слоях 1 и 2 определяется как
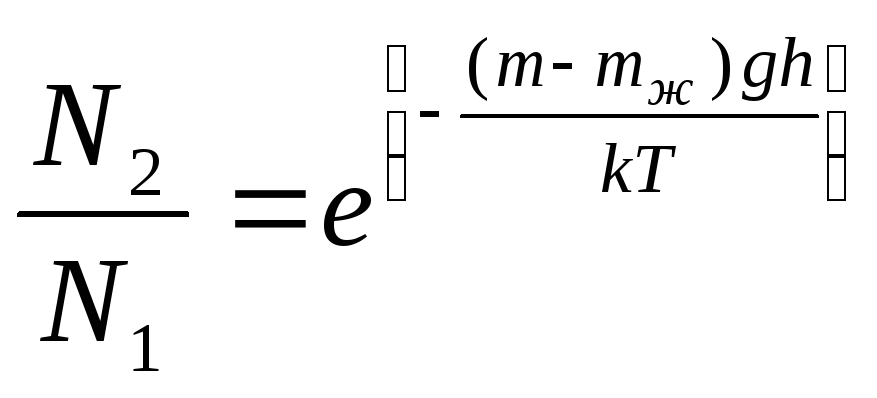 , (1)
, (1)
где учтено, что
на частицу массу
![]() действует сила тяжести
действует сила тяжести![]() и сила Архимеда
и сила Архимеда![]() ).
Преобразуем разность масс в круглых
скобках выражения (1)
).
Преобразуем разность масс в круглых
скобках выражения (1)
![]() . (2)
. (2)
После подстановки (2) в (1) соотношение (1) представим в виде
![]() , (3)
, (3)
отсюда, имея в
виду, что
![]() ,
следует
,
следует
![]() .
.
![]() ,
где
,
где
![]() =
8,31 Дж/моль·К – универсальная газовая
постоянная.
=
8,31 Дж/моль·К – универсальная газовая
постоянная.
Задача 5 Распределение Максвелла в приведенном виде Какая часть молекул газа имеет скорости, превышающие наиболее вероятную скорость?
Решение
Формула (3.30)
позволяет определить
![]() в любом интервале скоростей
в любом интервале скоростей
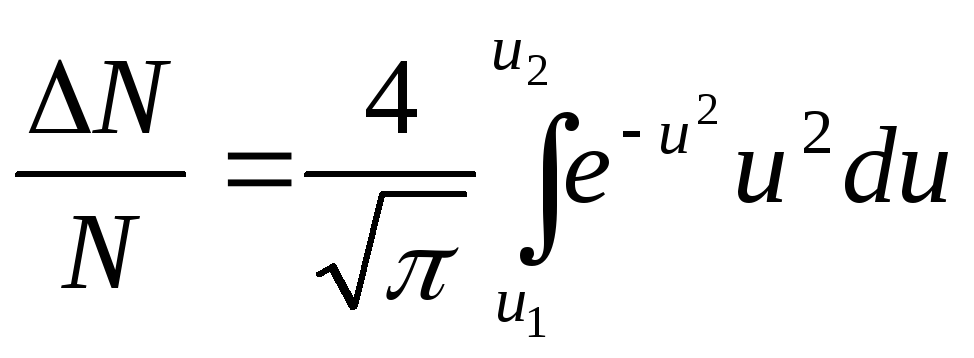 ,
,
где
![]() .
.
В нашем случае
![]() ,
,![]() .
.
Следовательно,
![]() .
.
Пусть
![]() - число молекул, скорость которых меньше
наиболее вероятной, т.е. лежат в интервале
от 0 до
- число молекул, скорость которых меньше
наиболее вероятной, т.е. лежат в интервале
от 0 до![]() или
или![]() изменяется в пределах от 0 до 1, тогда
изменяется в пределах от 0 до 1, тогда
![]()
![]()
![]()
![]()
Задача 6
Какая часть молекул водорода, находящегося
при температуре
![]() ,
обладает скоростями, отличающимися от
наиболее вероятной скорости не более,
чем на 5,0 м/с? Задачу решить для двух
значений
,
обладает скоростями, отличающимися от
наиболее вероятной скорости не более,
чем на 5,0 м/с? Задачу решить для двух
значений![]() :
1) 400 К; 2) 900 К.
:
1) 400 К; 2) 900 К.
Решение
Убедимся, что
выполняется условие
![]() или
или![]() .
Наиболее вероятная скорость
.
Наиболее вероятная скорость
![]() ,
,
![]() м/с
м/с
![]() м/с.
м/с.
Отсюда
![]() ;
;
![]() ;
;
Так как в нашем
случае
![]() ,
то
,
то![]() .
.
Поэтому в расчетах можно воспользоваться формулой (3.34):
![]() .
.
Подстановка числовых значений дает
![]()
![]()
Тесты
1. На рисунке
представлен график функции распределения
молекул идеального газа по скоростям
(распределение Максвелла), где
![]() – доля молекул, скорости которых
заключены в интервале скоростей отv
до v+dv
в расчете на единицу этого интервала.
Выберите верные утверждения.
– доля молекул, скорости которых
заключены в интервале скоростей отv
до v+dv
в расчете на единицу этого интервала.
Выберите верные утверждения.
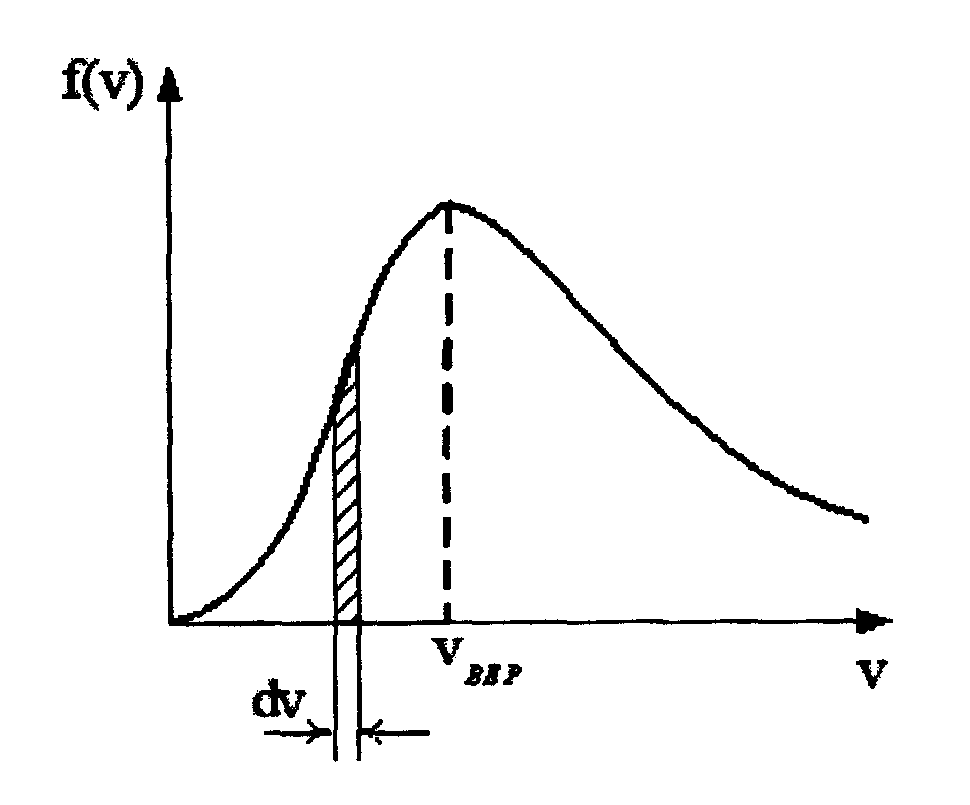
Рис.1
А. Площадь заштрихованной плоскости равна доле молекул со скоростями в интервале от v до v+dv.
В. При понижении температуры максимум кривой смещается влево.
С. При понижении температуры площадь кривой уменьшается.
1. – А, В и С; 2. – А и В; 3. – А и С; 4. – В и С.
2. На рисунке 1
представлен график функции распределения
молекул идеального газа по скоростям
(распределение Максвелла), где
![]() – доля молекул, скорости которых
заключены в интервале скоростей отv
до v+dv
в расчете на единицу этого интервала.
Выберите верные утверждения.
– доля молекул, скорости которых
заключены в интервале скоростей отv
до v+dv
в расчете на единицу этого интервала.
Выберите верные утверждения.
А. Положение максимума кривой зависит как от температуры, так и от природы газа.
В. При понижении температуры максимум кривой смещается влево.
С. При понижении температуры площадь под кривой уменьшается.
1. – А и В; 2. – В и С; 3. – А и С; 4. – А, В и С.
3. На рисунке 1
представлен график функции распределения
молекул идеального газа по скоростям
(распределение Максвелла), где
![]() – доля молекул, скорости которых
заключены в интервале скоростей отv
до v+dv
в расчете на единицу этого интервала.
Выберите верные утверждения.
– доля молекул, скорости которых
заключены в интервале скоростей отv
до v+dv
в расчете на единицу этого интервала.
Выберите верные утверждения.
А. С ростом температуры максимум кривой смещается вправо.
В. С ростом температуры площадь кривой не изменяется.
С. Вид функции распределения не зависит от природы газа (от массы молекул).
1. – А, В и С; 2. – только С; 3. – В и С; 4. – А и В; 5. – только В.
4. Атмосферное давление с ростом высоты над уровнем земли…
1. – растет линейно; 2. – уменьшается линейно; 3. – уменьшается экспоненциально; 4. – растет экспоненциально; 5.– уменьшается обратно пропорционально квадрату высоты.
5. Каким газам: водороду (Н2), гелию (Не) или кислороду (О2) соответствуют зависимости 1, 2, 3? Р – давление газов на высоте h, температуры газов одинаковы.
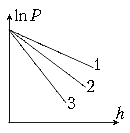
1. – 1 – гелий, 2 – кислород, 3 – водород; 2. – 1 – кислород, 2 – водород, 3 – гелий; 3. – 1 – водород, 2 – гелий, 3 – кислород; 4. – 1 – гелий, 2 – водород, 3 – кислород; 5. – 1 – водород, 2 – кислород, 3 – гелий.
6. Какой из перечисленных скоростей не существует?
1. – наиболее
вероятной
![]() ;
2. – среднеарифметической
;
2. – среднеарифметической![]() ;
3. – среднеквадратичной
;
3. – среднеквадратичной![]() ;
4. – полусредней
;
4. – полусредней![]() ;
5. – средней по абсолютному значению
;
5. – средней по абсолютному значению![]() .
.
7. В трех одинаковых сосудах при равных условиях находятся одинаковое количество водорода, гелия и азота.

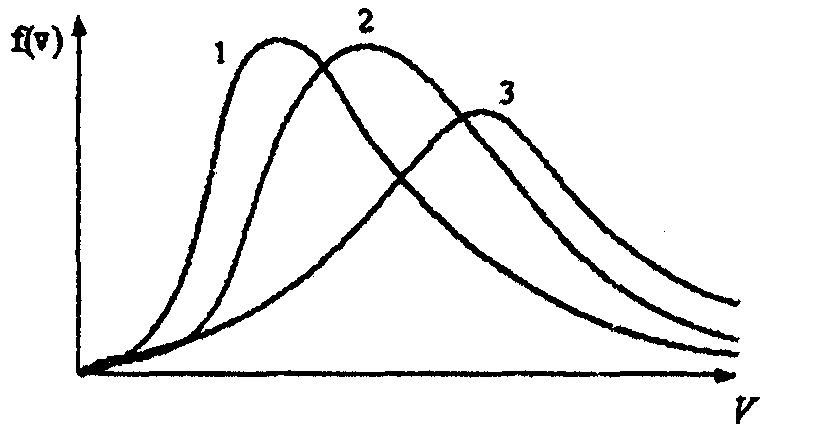
Распределение скоростей молекул гелия будет описывать кривая…
1. – 2; 2. – 1; 3. – 3.
8. Какая формула представляет функцию распределения Максвелла?
1. –
![]() ;
2. –
;
2. –![]() ;
3. –
;
3. –![]() ;
4. –
;
4. –![]() ;
5. –
;
5. –![]() .
.
9. Барометрическую формулу можно представить в виде:
1. –
![]() ,
,![]() – молярная масса,
– молярная масса,![]() – концентрация молекул на высоте
– концентрация молекул на высоте![]() ,
,![]() – универсальная газовая постоянная,
– универсальная газовая постоянная,![]() – абсолютная температура; 2. –
– абсолютная температура; 2. –![]() ,
,![]() – постоянная Больцмана; 3. –
– постоянная Больцмана; 3. –![]() ,
,![]() – диаметр молекул,
– диаметр молекул,![]() – концентрация,
– концентрация,![]() – средняя скорость,
– средняя скорость,![]() – число столкновений; 4. –
– число столкновений; 4. –![]() ,
,![]() - масса молекулы; 5. –
- масса молекулы; 5. –![]() .
.
10. Функция распределения Больцмана определяет распределение молекул идеального газа по…
1. – размерам; 2. – скоростям; 3. – молекулярным массам; 4. – энергии; 5. – импульсам.
11. Если два идеальных газа при одинаковой температуре имеют одну и ту же функцию распределения Максвелла, то у этих газов…
1. – одинаковое количество молекул; 2. – одинаковый объем; 3. – одинаковое давление; 4. – одинаковая молярная масса; 5. – одинаковое число молей.
