
- •№ 16. Аминокислоты
- •«Повсюду, где мы встречаем жизнь, мы находим, что она связана с каким-либо белковым
- •Пребиотический (абиогенный) синтез аминокислот
- •“Натура тем паче всего удивительна, что в простоте своей
- •20 аминокислот могут дать примерно
- •Первая по популярности
- •Белков в клетках больше, чем каких бы то ни было других органических соединений:
- •Аминокислоты – соединения, в
- •Классификации аминокислот
- •2. В зависимости от соотношения числа амино- и карбоксильных групп:
- •В зависимости от того, могут ли аминокислоты синтезироваться в организме
- •-аминокислоты
- •Всоответствии с природой остатка R (боковой цепью)
- •Классификации -аминокислот
- •Классификации аминокислот
- •Классификации аминокислот
- •Классификации аминокислот
- •Классификации аминокислот
- •Классификации аминокислот
- •Полярный радикал
- •Строительный белок клеток.
- •Витамины группы К
- •Природные источники аминокислот
- •Природные источники аминокислот
- •Природные источники аминокислот
- •Номенклатура
- •Номенклатура
- •Аланин
- •Номенклатура аминокислот
- •Номенклатура аминокислот
- •Нестандартные аминокислоты
- •Таурин, 2-аминоэтансульфоновая кислота,
- •Зеркало Венеры (1898), Sir Edward Burne-Jones / Museu Calouste Gulbenkian Lisbon /
- •Стереохимия аминокислот
- •Стереохимия аминокислот
- •D-аминокислоты
- •Gramicidin S
- •Аспартам
- •Физические и химические свойства
- •Аминокислоты являются амфотерными соединениями:
- •Кислотно-основное равновесие
- •Кислотно-основное равновесие
- •Физические и химические свойства
- •электрофорез
- •Изоэлектрическая точка
- •Изоэлектрическая точка
- •Значения pI аминокислот
- •Для моноаминомонокарбоновых кислот pI ≈ 5-6
- •Кислотно-основные свойства
- •Получение аминокислот
- •3. Биологический способ получения аминокислот
- •Химические синтезы аминокислот.
- •Реакции с участием только аминогруппы
- •Бетаин - триметильное производное
- •2.Ацилирование
- •Гиппууровая кислот ау
- •Образование N-ацильных производных
- •Физические и химические свойства
- •3. Образование оснований Шиффа
- •Реакция с формальдегидом
- •«Нингидриновая реакция»
- •4. Дезаминирование аминокислот
- •БИОЛОГИЧЕСКИ ВАЖНЫЕ РЕАКЦИИ
- •Б. Восстановительное дезаминирование
- •Г. Дегидратазное дезаминирование
- •Д. Окислительное дезаминирование
- •Трансаминирование – реакция переноса
- •Физические и химические свойства
- •Физические и химические свойства
- •Реакции, протекающие с участием только карбоксильной группы.
- •2. Образование галогенангидридов
- •3. Восстановление карбоксильной группы до первичной спиртовой
- •Процесс декарбоксилирования-аминокислот в организме
- •Путресцин- 1,4-диаминобутан, образующийся в толстой кишке при ферментативном декарбоксилировании орнитина; при цистинурии обнаруживается
- •Ферментативное гидроксилирование
- •Биогенные амины в организме
- •Декарбоксилирование
- •Декарбоксилирование в организме
- •Реакции, протекающие с участием обеих функциональных групп.
- •Лактим-лактамная таутомерия
- •-аминокислоты
- •-аминокислоты
- •-аминокислоты
- •-аминокислоты
- •2. Образование комплексных солей металлов
- •3.Образование межмолекулярных амидных связей
- •Аминокислоты нередко применяются в качестве лекарственных средств:
- •Met ( метионин ) используется при лечении заболеваний и токсических поражений печени
- •Cys (цистеин) участвуя в обмене хрусталика глаза, полезен
- •Na-соль Glu (глутамат натрия) является очень широко распространенной пищевой добавкой, улучшающей вкус продуктов.
- •Глутаминовая кислота и её соли безопасны!
- •- -аминомасляная (4-аминобутановая) кислота,
- •- Средство для лечения постинсультных
- •пара-Аминосалициловая кислота (4-амино-2- гидроксибензойная кислота, ПАСК) и ее натриевая соль обладают бактериостатической активностью
- •Биологическое значение аминокислот
- •Биологически важные химические реакции
- •Биологически важные химические реакции
- •Биологически важные химические реакции
- •Биологически важные химические реакции
- •Биологически важные химические реакции
- •Биологически важные химические реакции
- •Биологически важные химические реакции
- •Биологически важные химические реакции
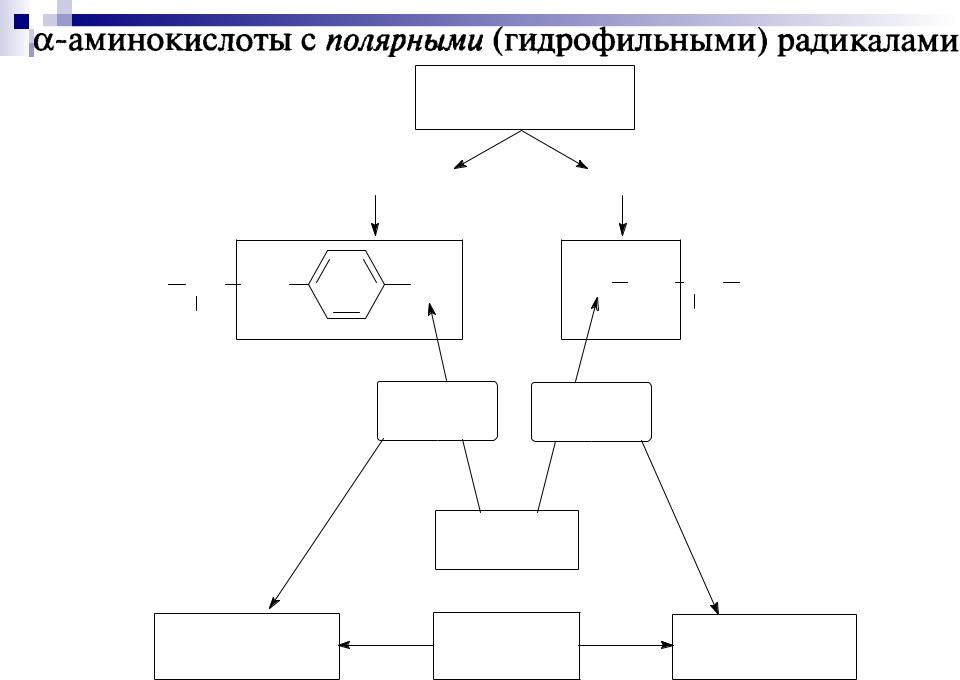
Полярный радикал
|
ионогенный |
неионогенный |
HOOC CH CH |
OH |
HO CH2 CH COOH |
2 |
|
NH2 |
NH |
|
|
2 |
|
|
Тирозин |
|
Серин |
|
фенольная |
спиртовая |
ОН-группа
диссоциирует |
В щелочной |
не диссоциирует |
|
среде |
|||
|
|
||
|
|
26 |
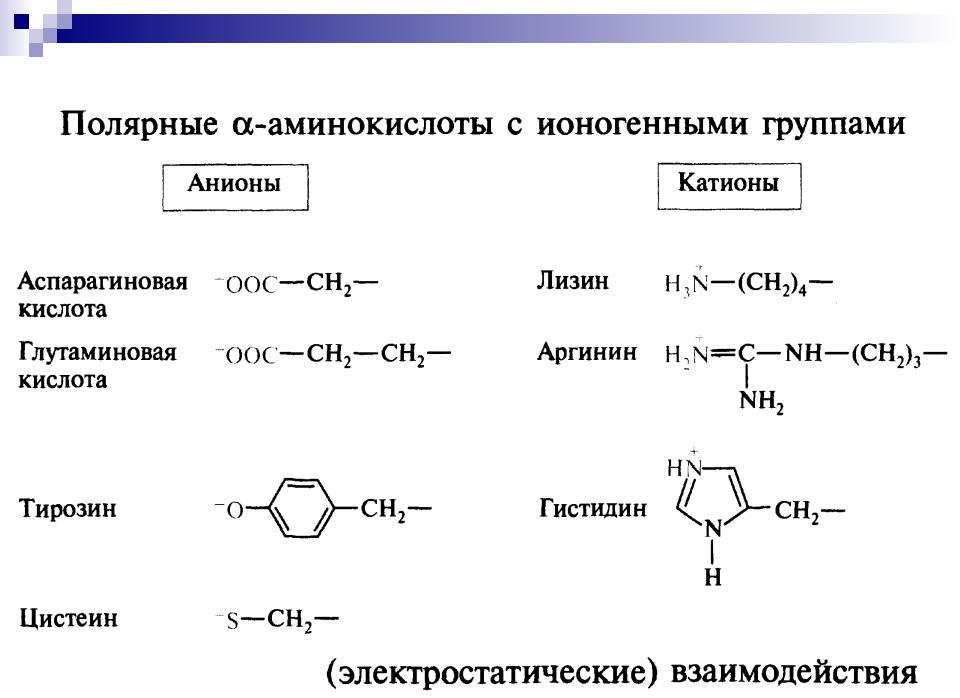
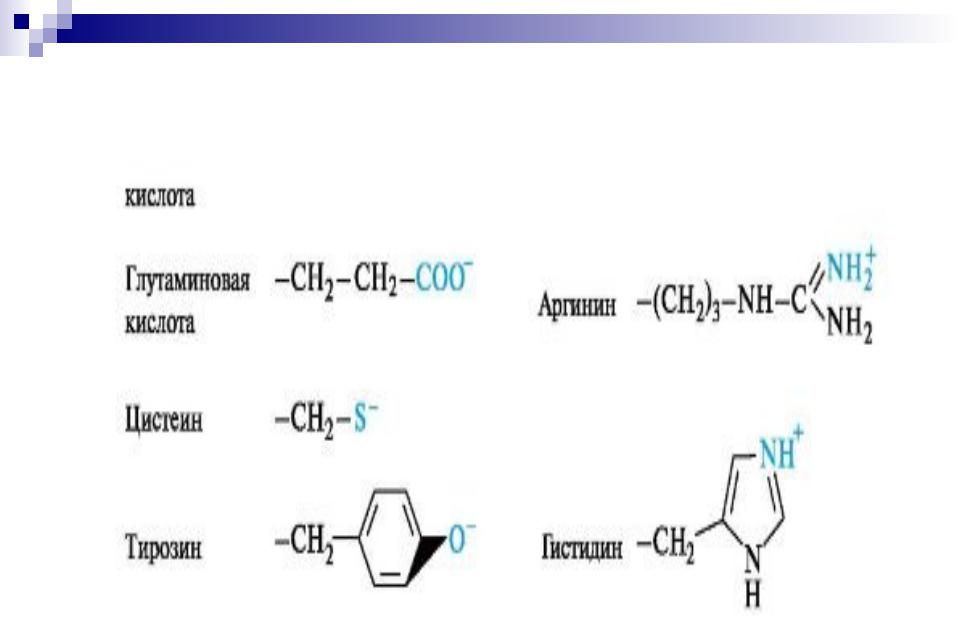
28
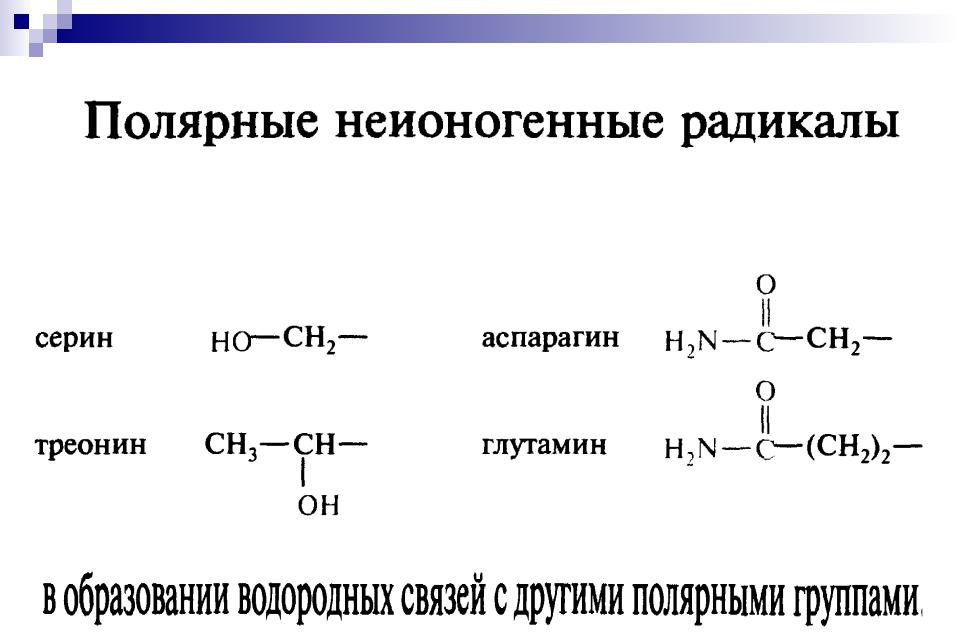
29
Строительный белок клеток.
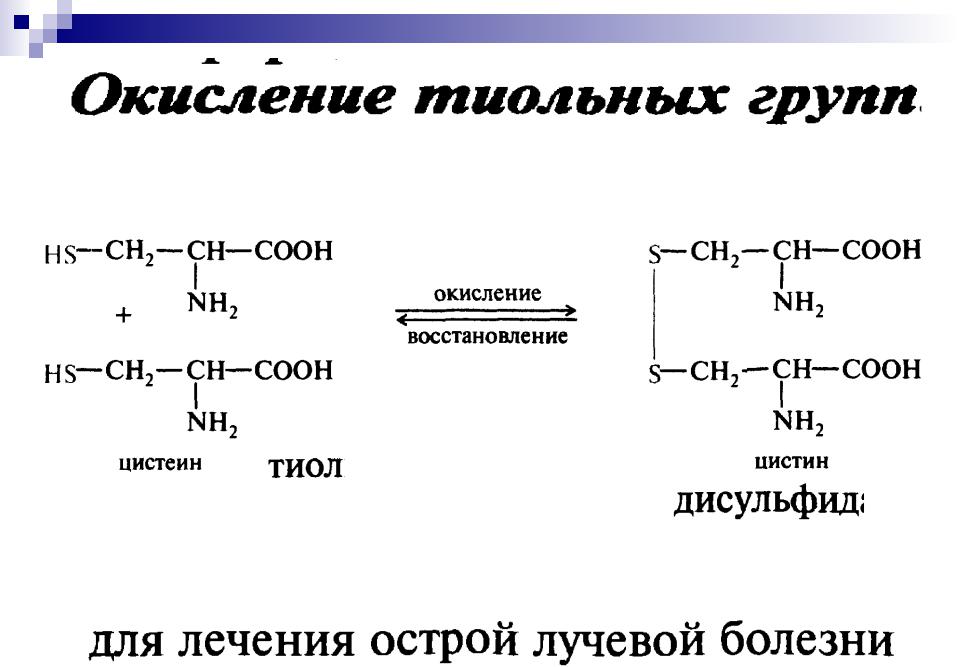
31
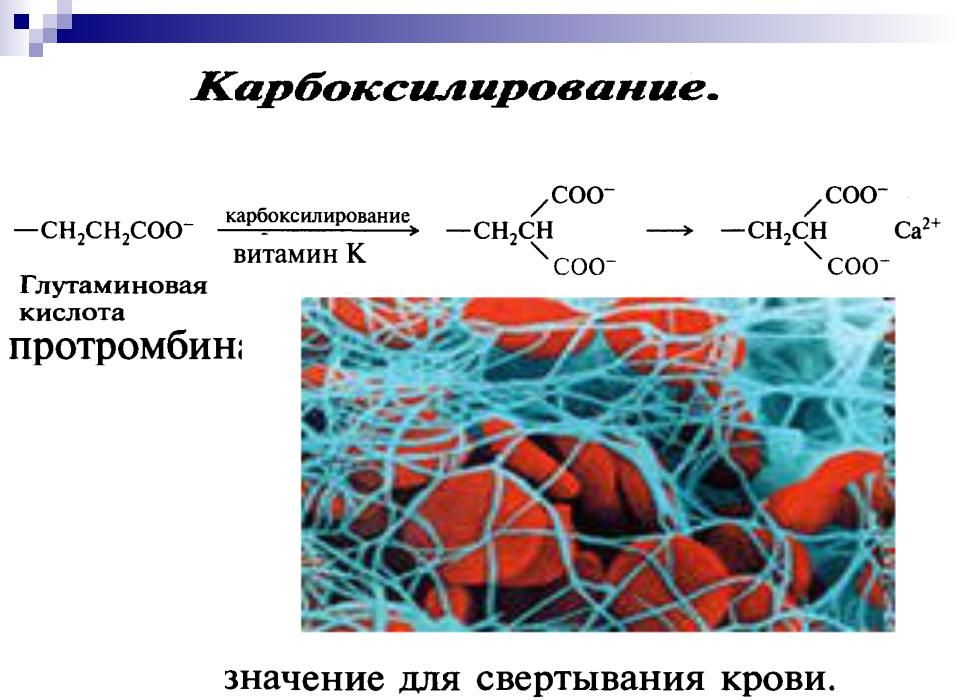
ν
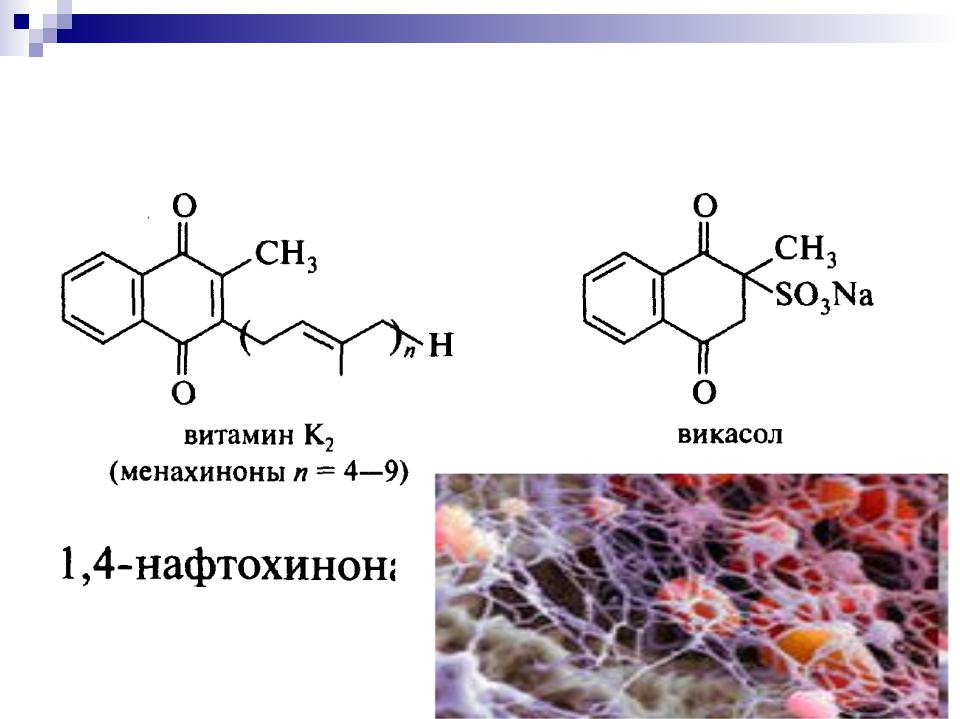
Витамины группы К
антигеморрагический фактор
2
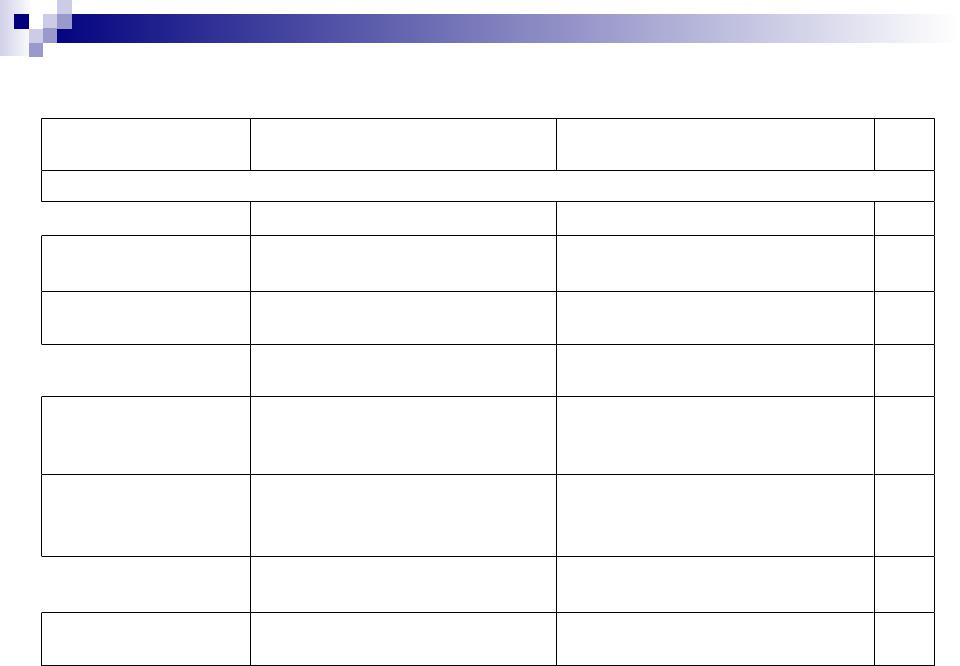
Природные источники аминокислот
Название
 Аланин Валин
Аланин Валин
Лейцин
 Изолейцин Фенилаланин
Изолейцин Фенилаланин
Метионин
 Триптофан Пролин
Триптофан Пролин
Открыватель, исходный |
Материал с наибольшим |
(pI) |
материал |
содержанием |
|
а) Нейтральные гидрофобные аминокислоты |
|
|
Вейль, фиброин шелка (1888) |
фиброин шелка (29,7%) |
6.02 |
Горуп-Безане, экстракт желез |
эластин (17,4%), сухожилия и |
5.97 |
(1856) |
аорта быка (17,6%) |
|
Пруст, творог (1819) |
сывороточный альбумин быка |
5.98 |
|
(12,8%), кукуруза (19%) |
|
Эрлих, патока (1904) |
сывороточный альбумин быка |
6.1 |
|
(2,6%), белок овса (4,3%) |
|
Шульце и Барбьери, ростки |
сывороточный альбумин |
5.88 |
люпина (1879) |
(7,8%), глубулин (4,6%), |
|
|
вальбумин (7,7%) |
|
Мюллер, казеин (1921) |
-казеин (4,1%), овальбумин |
5.8 |
|
(5,2%), лактоглобулин |
|
|
(3,2%) |
|
Гопкинс и Кол, казеин (1901) |
лизоцим (яйца) (10,6%), |
5.88 |
|
лактальбумин (7%)) |
|
Фишер, казеин (1901) |
сальмин (6,9%), казеин |
6.10 |
|
(10,6%), желатин (16,3%) |
|
|
34 |
|
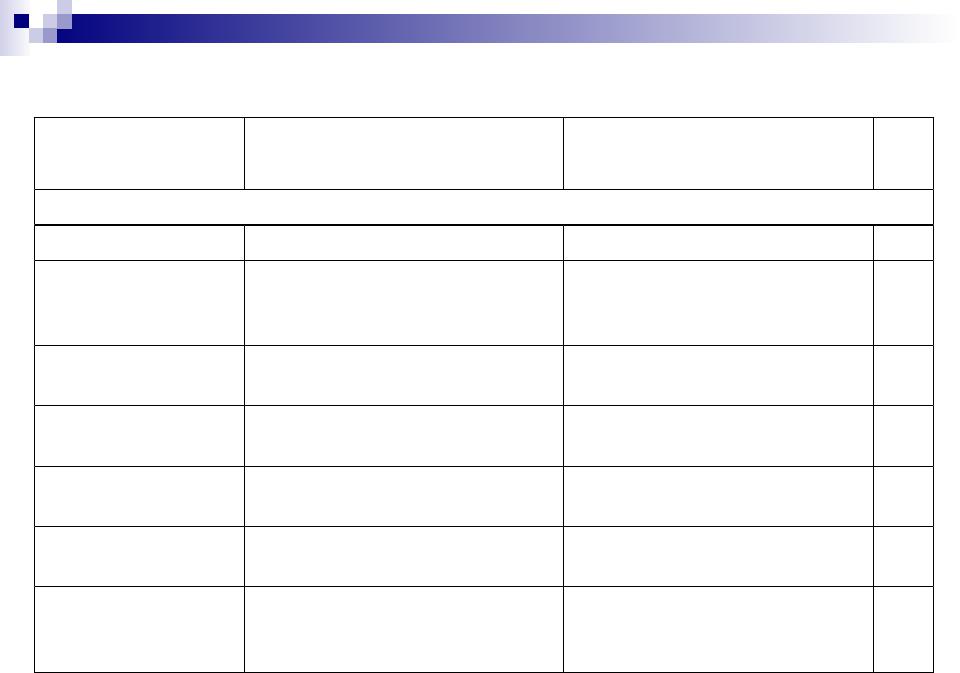
 Природные источники аминокислот
Природные источники аминокислот
Название |
Открыватель, исходный |
Материал с наибольшим |
(pI) |
материал |
содержанием |
|
|
|
б) Нейтральные гидрофильные аминокислоты |
|
|
Глицин |
Браконно, шелк (1820) |
фиброин шелка (29,7%) |
5.97 |
Серин |
Крамер, шелковый клей |
фиброин шелка (16,2%), |
5.70 |
|
(1865) |
трипсиноген (16,7%), пепсин |
|
|
|
(12,2%) |
|
Треонин |
Розе и др., фибрин (1935) |
кератин волос (8,5%), |
6.50 |
|
|
яичный белок (10,5%) |
|
Тирозин |
Либих, сыр (1846) |
фиброин шелка (12,8%), |
5.65 |
|
|
папаин (14,7%) |
|
Аспарагин |
Вокелин и Робике, спаржа |
|
5.41 |
|
(1806) |
|
|
Глутамин |
Шульце, сахарная свекла |
|
|
|
(1877) |
|
|
Цистеин |
Бауман, цистин (1884) |
кератин волос (14,4%), |
5.02 |
|
|
кератин перьев (8,2%), |
|
|
|
кератин шерсти (11,9%) |
|
35
