
- •№ 16. Аминокислоты
- •«Повсюду, где мы встречаем жизнь, мы находим, что она связана с каким-либо белковым
- •Пребиотический (абиогенный) синтез аминокислот
- •“Натура тем паче всего удивительна, что в простоте своей
- •20 аминокислот могут дать примерно
- •Первая по популярности
- •Белков в клетках больше, чем каких бы то ни было других органических соединений:
- •Аминокислоты – соединения, в
- •Классификации аминокислот
- •2. В зависимости от соотношения числа амино- и карбоксильных групп:
- •В зависимости от того, могут ли аминокислоты синтезироваться в организме
- •-аминокислоты
- •Всоответствии с природой остатка R (боковой цепью)
- •Классификации -аминокислот
- •Классификации аминокислот
- •Классификации аминокислот
- •Классификации аминокислот
- •Классификации аминокислот
- •Классификации аминокислот
- •Полярный радикал
- •Строительный белок клеток.
- •Витамины группы К
- •Природные источники аминокислот
- •Природные источники аминокислот
- •Природные источники аминокислот
- •Номенклатура
- •Номенклатура
- •Аланин
- •Номенклатура аминокислот
- •Номенклатура аминокислот
- •Нестандартные аминокислоты
- •Таурин, 2-аминоэтансульфоновая кислота,
- •Зеркало Венеры (1898), Sir Edward Burne-Jones / Museu Calouste Gulbenkian Lisbon /
- •Стереохимия аминокислот
- •Стереохимия аминокислот
- •D-аминокислоты
- •Gramicidin S
- •Аспартам
- •Физические и химические свойства
- •Аминокислоты являются амфотерными соединениями:
- •Кислотно-основное равновесие
- •Кислотно-основное равновесие
- •Физические и химические свойства
- •электрофорез
- •Изоэлектрическая точка
- •Изоэлектрическая точка
- •Значения pI аминокислот
- •Для моноаминомонокарбоновых кислот pI ≈ 5-6
- •Кислотно-основные свойства
- •Получение аминокислот
- •3. Биологический способ получения аминокислот
- •Химические синтезы аминокислот.
- •Реакции с участием только аминогруппы
- •Бетаин - триметильное производное
- •2.Ацилирование
- •Гиппууровая кислот ау
- •Образование N-ацильных производных
- •Физические и химические свойства
- •3. Образование оснований Шиффа
- •Реакция с формальдегидом
- •«Нингидриновая реакция»
- •4. Дезаминирование аминокислот
- •БИОЛОГИЧЕСКИ ВАЖНЫЕ РЕАКЦИИ
- •Б. Восстановительное дезаминирование
- •Г. Дегидратазное дезаминирование
- •Д. Окислительное дезаминирование
- •Трансаминирование – реакция переноса
- •Физические и химические свойства
- •Физические и химические свойства
- •Реакции, протекающие с участием только карбоксильной группы.
- •2. Образование галогенангидридов
- •3. Восстановление карбоксильной группы до первичной спиртовой
- •Процесс декарбоксилирования-аминокислот в организме
- •Путресцин- 1,4-диаминобутан, образующийся в толстой кишке при ферментативном декарбоксилировании орнитина; при цистинурии обнаруживается
- •Ферментативное гидроксилирование
- •Биогенные амины в организме
- •Декарбоксилирование
- •Декарбоксилирование в организме
- •Реакции, протекающие с участием обеих функциональных групп.
- •Лактим-лактамная таутомерия
- •-аминокислоты
- •-аминокислоты
- •-аминокислоты
- •-аминокислоты
- •2. Образование комплексных солей металлов
- •3.Образование межмолекулярных амидных связей
- •Аминокислоты нередко применяются в качестве лекарственных средств:
- •Met ( метионин ) используется при лечении заболеваний и токсических поражений печени
- •Cys (цистеин) участвуя в обмене хрусталика глаза, полезен
- •Na-соль Glu (глутамат натрия) является очень широко распространенной пищевой добавкой, улучшающей вкус продуктов.
- •Глутаминовая кислота и её соли безопасны!
- •- -аминомасляная (4-аминобутановая) кислота,
- •- Средство для лечения постинсультных
- •пара-Аминосалициловая кислота (4-амино-2- гидроксибензойная кислота, ПАСК) и ее натриевая соль обладают бактериостатической активностью
- •Биологическое значение аминокислот
- •Биологически важные химические реакции
- •Биологически важные химические реакции
- •Биологически важные химические реакции
- •Биологически важные химические реакции
- •Биологически важные химические реакции
- •Биологически важные химические реакции
- •Биологически важные химические реакции
- •Биологически важные химические реакции
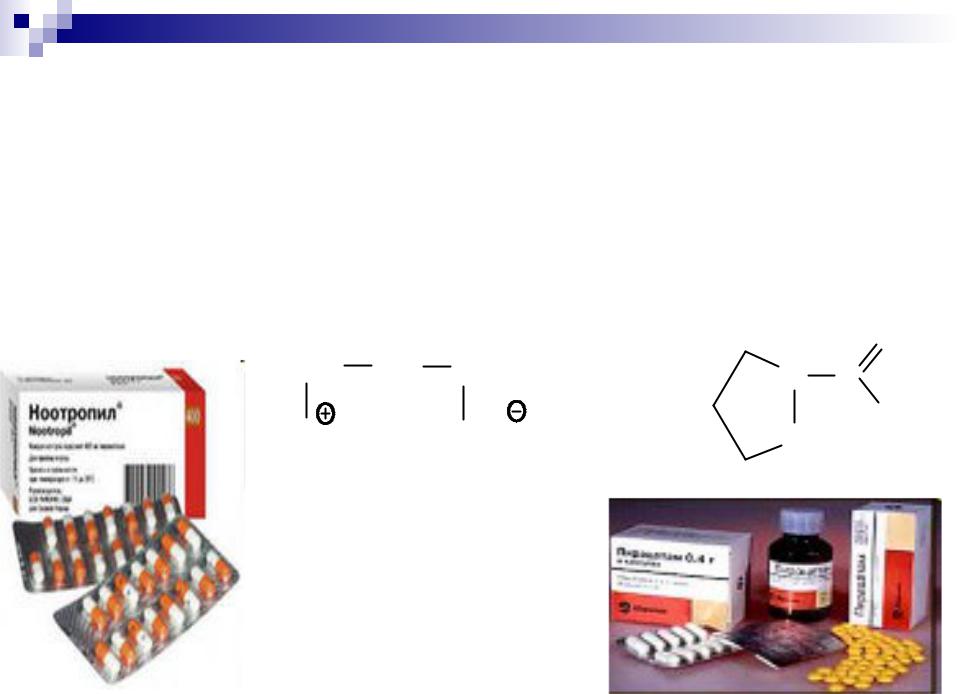
- -аминомасляная (4-аминобутановая) кислота,
принимает участие в обменных процессах головного мозга; лактам ее N-ацетилированной формы
(ноотропил, или пирацетам) широко
используется в медицине для лечения нарушений функций головного мозга
CH2 |
CH2 CH2 |
N C O |
H3N |
COO |
CH3 |
C=О |
||
-Аминомасляная кислота |
Пирацетам |
|
- Средство для лечения постинсультных
больных (церебролизин) состоит главным
образом из смеси аминокислот, получаемых в |
|
результате гидролиза мозгового вещества |
|
- |
крупного рогатого скота. |
108

109

пара-Аминосалициловая кислота (4-амино-2- гидроксибензойная кислота, ПАСК) и ее натриевая соль обладают бактериостатической активностью в отношении бактерий туберкулеза и являются известным противотуберкулезным препаратом.
Этиловый эфир 4-аминобензойной кислоты (анестезин)
и 2-диэтиламиноэтиловый эфир той же кислоты
(новокаин, или прокаин) широко используются в
качестве анестетиков:
H N |
OH H2N |
|
H2N |
. |
3 |
|
COOC2H5 |
|
|
|
COO |
|
COOCH2CH2N(C2H5)2 |
|
ПАСК |
|
Анестезин |
|
Новокаин |
110
Биологическое значение аминокислот
1. Аминокислоты являются теми мономерными молекулами, из которых в организме образуются практически все биологически важные биополимеры: простые и сложные белки (именно поэтому природные аминокислоты называют протеиногенными);
2. В ходе обменных процессов,, аминокислоты превраща- ются в разнообразные биологически важные соединения других классов. Например, Arg служит компонентом цикла образования мочевины, Asp предшествует синтезу пуринов, пиримидинов, щавелевоуксусной кислоты, а без Gly невозможен биосинтез порфиринов, пуринов,глутатиона, креатина;
3. Cущественна роль аминокислот как предшественников разнообразных нейромедиаторов:
CH CHCOO |
|
CH CHCOO |
CH CH NH |
2 |
HOCHCH2NH2 |
|
2 |
2 2 |
|
||
2 |
|
NH3 |
|
|
|
NH |
|
|
|
|
|
3 |
|
|
|
|
; |
|
|
|
HO OH |
|
|
Фенилаланин |
HO |
OH |
|
HO OH |
|
|
3,4-Диоксифенилаланин Дофамин |
|
Норадреналин |
||
ДОФА или DOPA |
111 |
N |
CH2CHCOO |
N |
CH2CH2NH2 |
N |
NH3 |
N |
; |
H |
Гистидин |
H |
Гистамин |
отвечает за развитие аллергических реакций
|
|
J |
|
|
J |
|
|
|
|
HO |
CH2CHCOO |
HO |
|
O |
|
CH CHCOO |
|
|
|
Тирозин NH3 |
J |
|
|
J |
2 |
|
|
|
|
|
|
NH3 . |
|
|
|||||
Тироксин |
|
|
|||||||
|
гормон щитовидной железы (регулирует обмен веществ) |
||||||||
|
CH2CHCOO |
CH CH NH |
2 |
HO |
|
CH CH NH |
|
||
|
|
2 2 |
|
|
2 |
||||
N |
NH3 |
N |
|
|
|
2 |
2 |
|
|
|
|
N |
|
|
. |
||||
H Триптофан |
H Триптамин |
|
|
Серотонин |
|||||
|
|
H |
|
|
|||||
серотонинэргический
медиатор, вызывает торможение
112
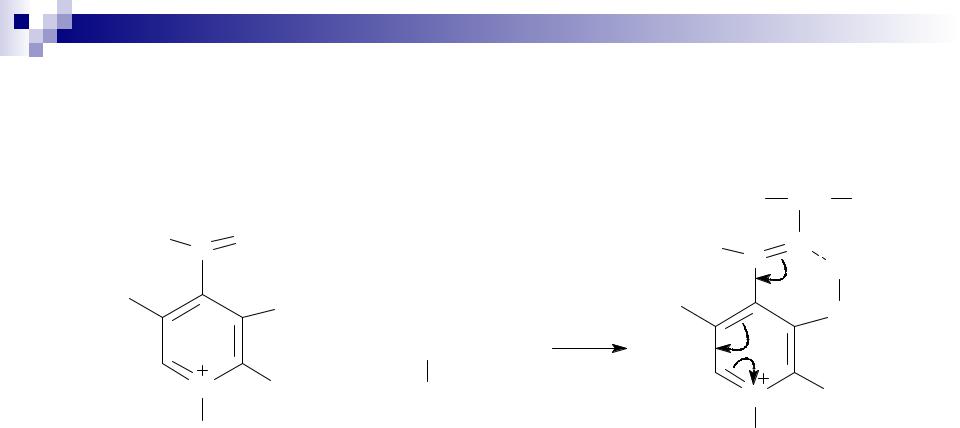
Биологически важные химические реакции
|
|
|
|
R |
CH COOH |
|
H C |
O |
|
H |
C |
N |
H |
|
|
|
|
|
||
2-O3POCH2 |
|
|
2- |
|
|
|
OH |
|
|
|
O |
||
|
|
O3POCH2 |
|
|
||
|
+ |
NH2CHCOOH |
|
|
|
|
N |
CH3 |
R |
|
N |
|
CH3 |
H |
|
|
|
H |
|
|
|
|
|
|
|
|
|
пиридоксальфосфат |
-аминокислота |
Альдимин I |
|
|||
113
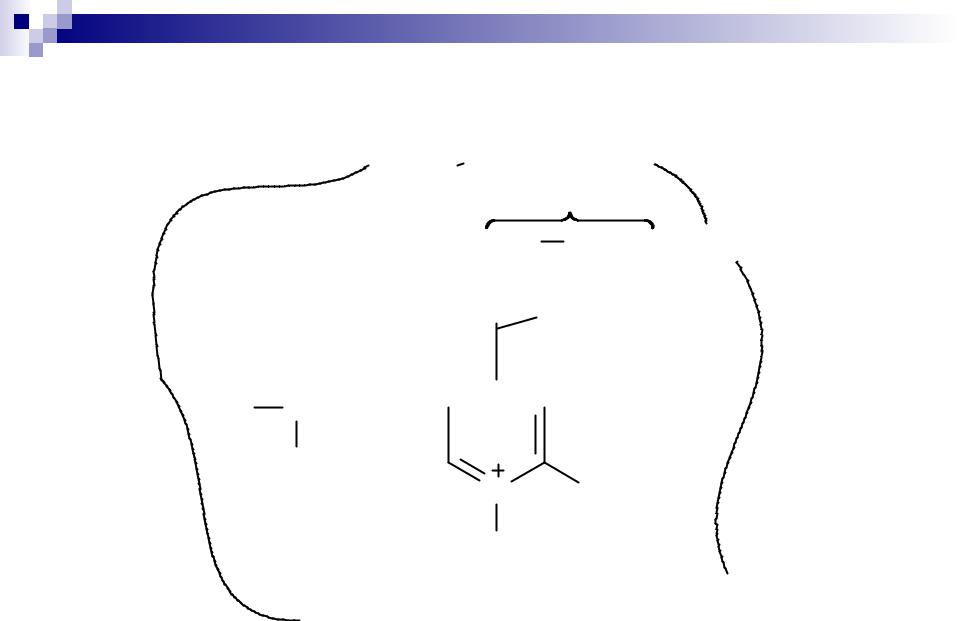
Биологически важные химические реакции
фермент































 Lys
Lys
NH2 (CH2)4


H O O
O O
-O P

 O
O
 OH
OH
O- |
CH3 |
N |
H
пиридоксальфосфат
114
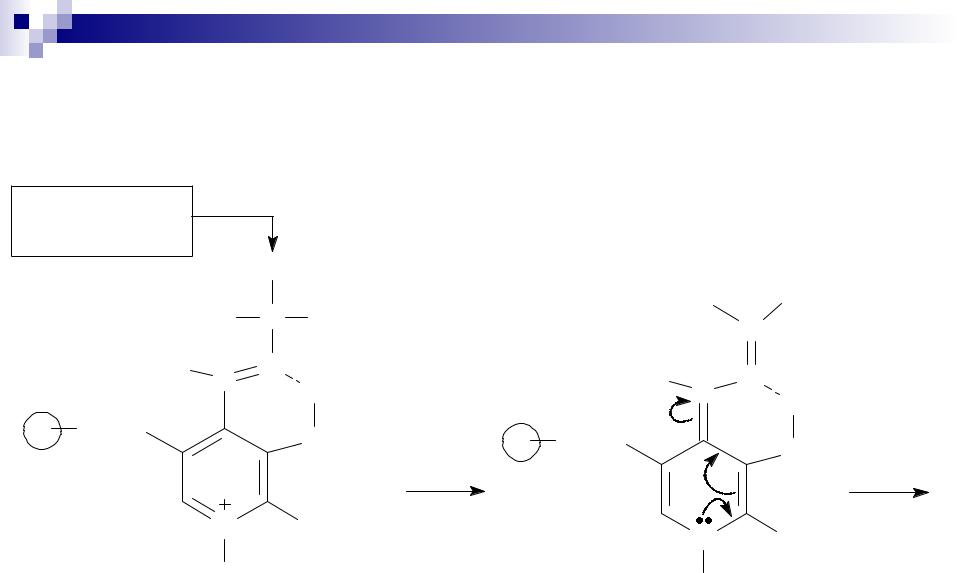
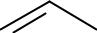
Биологически важные химические реакции
Перенос аминогруппы
Подвижный |
|
|
|
|
|
|
|
атом водорода |
|
|
|
|
|
|
|
|
H |
|
|
R |
|
COO- |
|
R |
C COO- |
|
C |
|
|||
|
|
|
|
||||
|
|
|
|
|
|
|
|
H C |
N |
H |
H |
C |
N |
H |
|
|
|
|
|
|
|||
P OCH2 |
|
|
|
|
|
|
|
|
O |
P OCH2 |
|
|
O |
|
|
|
|
|
|
H+ |
|||
|
|
|
-H+ |
|
|
|
|
N |
|
CH3 |
N |
|
CH3 |
|
|
|
|
|
|
||||
H |
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
Альдимин I |
|
|
II |
|
|
|
|
|
|
|
|
|
|
|
|
115
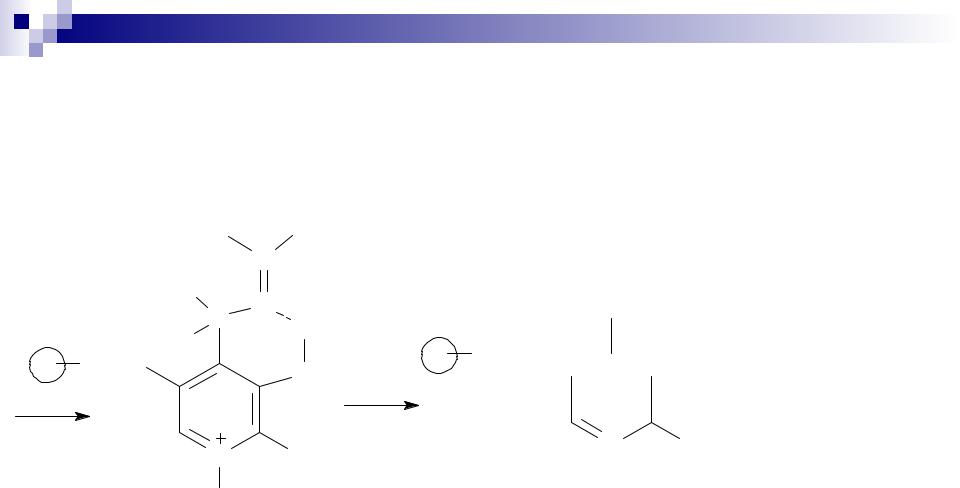
Биологически важные химические реакции
Перенос аминогруппы
RCOO-
H |
C |
|
N H |
|
|
C |
|
|
H |
|
|
P OCH2 |
O |
+H2O |
|
|
|
N |
CH3 |
|
H |
|
|
CH2NH2
POCH2

 OH
OH
|
|
|
|
+ R |
|
C |
|
COO- |
||
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
CH3 |
|
|
|
|
|
|
|||
|
O |
|
|
|||||||
|
|
|
|
|||||||
H |
|
|
|
|
|
|
|
|||
Пиридоксаминфосфат -оксокислота
116
