
- •№ 3. Общая характеристика реакций органических соединений.
- •Классификация органических реакций
- •2. Реакции присоединения Ad (аddition
- •3. Реакции отщепления, E (El) (еlimination):
- •4. Перегруппировки
- •5. Реакции окисления-восстановления
- •Степень окисления углерода
- •II.По механизму
- •2. Ионные реакции называются гетеролитическими.
- •3. Согласованные реакции (синхронные)
- •III. По молекулярности реакции делятся на мономолекулярные и бимолекулярные
- •SN2 Бимолекулярная реакция:
- •Типы реагентов
- •Электрофилы ( акцепторы электронов)
- •Нуклеофильный реагент
- •нуклеофилы
- •Радикальные реагенты
- •При оценке основности за субстрат принимают протон, при оценке нуклеофильности
- •Селективность ( избирательность) химических превращений.
- •in vivo
- •Факторы,определяющие реакционную способность
- •Электронный фактор
- •Интермедиаты
- •Карбкатионы представляют собой замещенные атомы углерода, имеющие вакантную (незаполненную) орбиталь
- •Возможность делокализации положительного заряда является основным фактором, обусловливающим стабильность карбкатиона.
- •Сверхсопряжение (гиперконъюгация) (1935)
- •Аллильный катион
- •Бензильный катион
- •Ряд устойчивости катионов:
- •Перегруппировки катионов
- •1,2- метильный сдвиг
- •Свободными радикалами называются
- •Чем больше возможностей для делокализации свободного электрона предоставляет структура свободного радикала, тем стабильнее
- •Ряд увеличения стабильности свободных радикалов:
- •Карбанионы образуются в результате отщепления протона от тех соединений, которые функционируют как
- •Рассредоточение отрицательного заряда
- •Ряд устойчивости анионов:
- •КИСЛОТНО-ОСНОВНЫЕ СВОЙСТВА ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ. № 4
- •Теория Брёнстеда-Лоури.
- •Кислоты Брёнстеда
- •Кислотность по Брёнстеду
- •Константа кислотности (Ка)
- •Качественной характеристикой
- •С – Н кислоты
- •По группам (Поляризуемость)
- •3. Влияние органического радикала, связанного с кислотным центром
- •В ароматическом ряду:
- •4. Влияние растворителя.
- •Основность по Брёнстеду
- •2. Оксониевые основания
- •3. Сульфониевые основания (центр основности сера) :
- •Сила n-оснований с одинаковыми радикалами
- •-основания
- •Алифатические амины
- •Основные свойства
- •Ароматические амины
- •Новокаин
- •Новокаинамид
- •Мазь
- •Кислотно-основные свойства аминокислот. Амфотерность
- •Фосфатидилхолин
- •Гетероциклические соединения
- •Гетероциклические соединения Пиррол
- •Имидазол
- •Пиридин Пиррол
- •Гетероциклические соединения Пиридин
- •Гетероциклические соединения Пиридин
- •Теория Льюиса (1923)
- •Американский физикохимик
- •Кислоты Льюиса – это любые соединения со свободной орбиталью
- •Теория Льюиса

С – Н кислоты

По группам (Поляризуемость)
При одинаковых радикалах кислотность уменьшается в ряду:
-SH >-OH > -NH > -CH.

2.
|
|
|
|
O |
O |
O |
H3C |
а |
O ; |
CH3 C |
О |
CH3 C |
èëè CH3 C |
|
|
б |
О |
О . |
||
Спирт |
|
|||||
|
|
|||||
карбоновая кислота
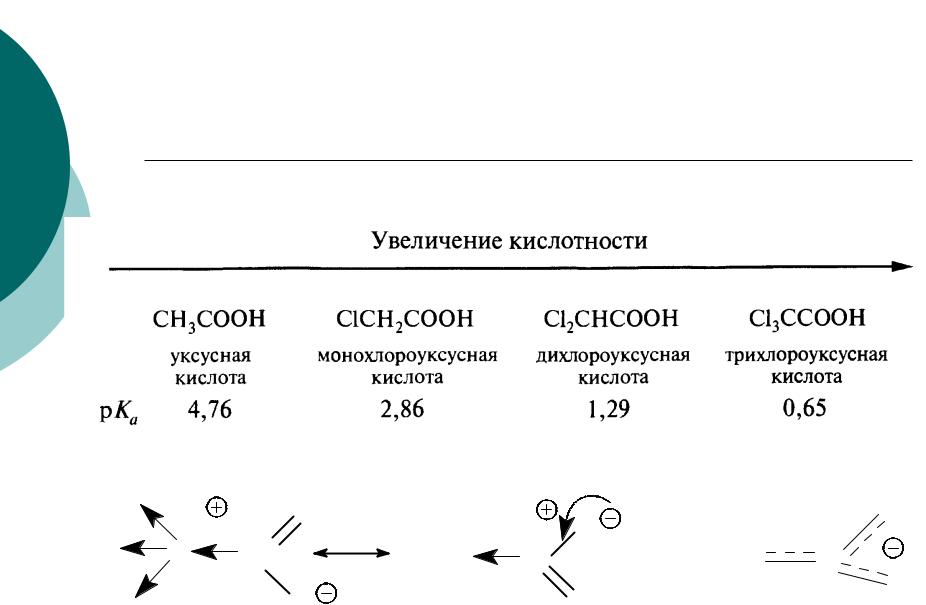
3. Влияние органического радикала, связанного с кислотным центром
Cl |
|
O |
|
' |
O |
O |
|
Cl С |
CCl3 |
C |
|||||
|
C |
C |
èëè CCl3 |
||||
Cl |
в |
О |
|
|
О |
О . |
|
|
|
|
|


CH3 — CH2 — OH + H2O |
H3O+ + CH3 — CH2 O- |
этоксид-анион + IС2Н5
Спирт
— OH + H2O |
H3O+ + |
— O- : |
фенол |
феноксид-анион |
|
Фенолы более кислые, чем алифатические спирты.

В ароматическом ряду:

4. Влияние растворителя.
Эффект сольватации (гидратации).
лучше гидратируются небольшие по размеру ионы с низкой степенью делокализации заряда.
|
НСООН |
СН3СООН |
СН3 -СН2 |
С15Н31 -СООН |
|
муравьиная |
уксусная |
-СООН |
пальмитиновая |
|
|
|
пропановая |
|
рКа |
3.7 |
4,7 |
4,9 |
|


Основность по Брёнстеду
Основания Брёнстеда – это
нейтральные молекулы или ионы, способные присоединять протон (акцепторы протонов).
_
основание катион

n-
основания
1. Аммониевые основания
(центр основности азот)
RNH2 RNHR' RN(R')R'' |
RCH=NH |
RC N |
Àì èí û |
Àçî ì åòèí û |
Н итрилы |
.. |
..N |
NH |
N.. |
||
N |
|
|
П иридин |
Õèí î ëèí |
Им идазо л |
