
- •Тема 3. Альдегиды и кетоны 36
- •Вопросы для самоподготовки
- •Этапы занятия и контроль усвоения знаний
- •Основные направления реакционной способности углеводородов в зависимости от их электронного строения
- •Циклоалканы
- •Циклопропан с3н6
- •Транс-1,4-диметилциклогексан цис-1,4-диметилциклогексан
- •1. Гидрирование
- •Пропен пропан
- •2. Галогенирование
- •3. Гидрогалогенирование:
- •6. Полимеризация:
- •Алкадиены Это углеводороды, содержащие две двойные связи. Общая формула Сn h2n-2.
- •1. Гидрирование:
- •2. Гидрогалогенирование:
- •Ароматические углеводороды (арены)
- •Химические свойства
- •Заместители 2 рода ( -cooh, -so3h, -cho, -no2 и др.) – электроноакцепторы, уменьшают электронную плотность в кольце, затрудняют реакцию se и ориентируют электрофил в мета-положение.
- •Тема 2. Спирты. Фенолы. Нафтолы. Тиолы
- •Вопросы для самоподготовки
- •Этапы занятия и контроль усвоения знаний
- •Содержание этапов занятия
- •Кислотность и основность органических соединений
- •Кислоты тон
- •Одноатомные спирты
- •Дегидрирование альдегид
- •Дегидрирование кетон
- •Многоатомные спирты
- •Спирты высшей атомности
- •Свойства фенолов как ароматических соединений. Реакции электрофильного замещения
- •Нафтолы
- •Ароматические спирты
- •Химические свойства
- •Глоссарий
- •Тема 3. Альдегиды и кетоны
- •Пиридоксаль пиридоксальфосфат
- •Этапы занятия и контроль усвоения знаний
- •Содержание этапов занятия
- •I. Реакции нуклеофильного присоединения
- •4. Взаимодействие с галогенсодержащими реагентами
- •II. Реакции за счет -сн2-звена
- •1. Галогенирование:
- •III. Реакции, характерные только для альдегидов
- •Глоссарий
- •Тема 4. Карбоновые кислоты и их функциональные производные
- •Конкретные задачи
- •Вопросы для самоподготовки
- •Содержание этапов занятия
- •Этановая кислота 2-метилпропановая бутен-3-овая кислота
- •Высшие жирные кислоты (вжк)
- •Изомерия
- •Малеиновая фумаровая кислота
- •Линолевая кислота
- •Химические свойства
- •2. Реакции нуклеофильного замещения (sn ):
- •Двухосновные карбоновые кислоты
- •Трехосновные кислоты
- •Ноос–сн2–с–сн2–соон лимонная 3-гидрокси – 3-карбокси -
- •Специфические реакции двухосновных кислот
- •Тема 5. Липиды
- •Конкретные задачи
- •Вопросы для самоподготовки
- •Этапы занятия и контроль усвоения знаний
- •Омыляемые липиды
- •Омыляемые липиды
- •Жирные кислоты
- •Простые омыляемые липиды
- •Сложные омыляемые липиды
- •Фосфолипиды
- •Глицерофосфо- сфингофосфо-
- •Гликолипиды
- •Стероиды
- •Классификация стероидов
- •Эстрадиол
- •Глоссарий
Содержание этапов занятия
1-й этап.Преподаватель проверяет выполнение домашнего задания по теме и отвечает на вопросы студентов, выставляет оценку по пятибалльной системе.
2-й этап.Студент письменно отвечает на билет тест – контроля. Ответ оценивается по десятибалльной системе (0, 5, 10 балов).
3-й этап.При опросе теоретического материала студенты у доски разбирают:
– особенности электронного строения карбоксильной группы и связь с химическим поведением;
– способность кислот к диссоциации и сравнение силы различных кислот на примере масляной, 2-оксимасляной, 2-метилмасляной, 2-хлормасляной и янтарной кислот;
– химические свойства кислот, обусловленные реакциями по карбоксильной группе: образование сложных эфиров, ангидридов, галогенангидридов, амидов;
– химические свойства, обусловленные реакциями в радикале: реакции по двойной связи непредельных кислот на примере акриловой кислоты, реакции замещения в радикале предельных кислот на примере пропановой кислоты, реакции замещения в ароматическом кольце на примере бензойной кислоты;
– специфические свойства двухосновных кислот, проявляющиеся при нагревании, на примере пропандиовой, бутандиовой и гександиовой кислот.
4-й этап.Студенты по 2 человека выполняют предложенные лабораторные работы.
5-й этап.Студенты оформляют лабораторные работы по унифицированной форме в виде таблицы, данной в рабочей тетради.
6-й этап.Студент представляет оформленный протокол и объясняет полученные результаты.Преподаватель оцениваетего практические навыки.
Теория
Карбоновыми кислотами называются органические соединения, содержащие карбоксильную группу – СООН, общая формула R-(COOH)n
Классификация.
1. По числу функциональных групп (–СООН): одно- и многоосновные.
2. По характеру радикала R:
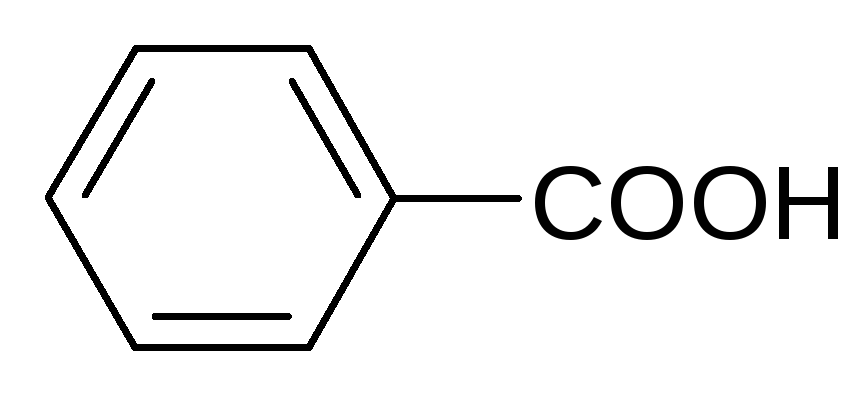 предельные, непредельные,
ароматические.
предельные, непредельные,
ароматические.
СН3–СН2–СООН, СН2= СН–СООН;
Одноосновные карбоновые кислоты
Номенклатура.
В основе международной номенклатуры ИЮПАК лежат названия нормальных (неразветвленных) углеводородов. Наличие карбоксильной группы отражается в названии кислоты окончанием -овая:
СН3-СООН СН3-СН-СООН СН2=СН–СН2-СООН
СН3
Этановая кислота 2-метилпропановая бутен-3-овая кислота
кислота
Для двухосновных кислот название строится так же, с окончанием -диовая:
НООС–СН2–СН2-СООН (бутандиовая кислота).
В названиях ароматических кислот в качестве родоначальной структуры используется бензойная кислота.
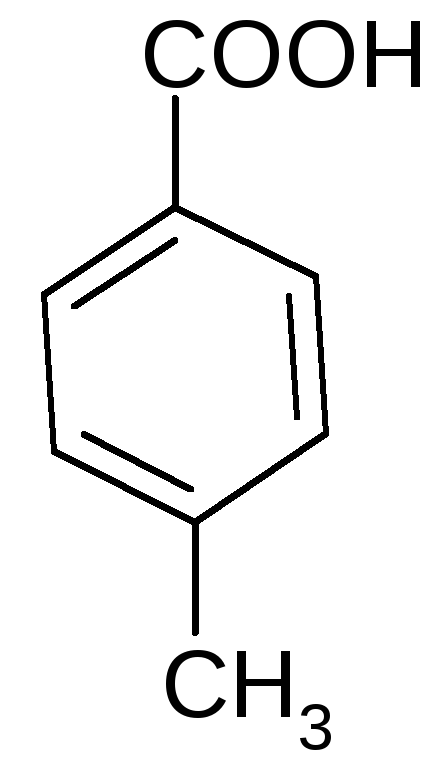
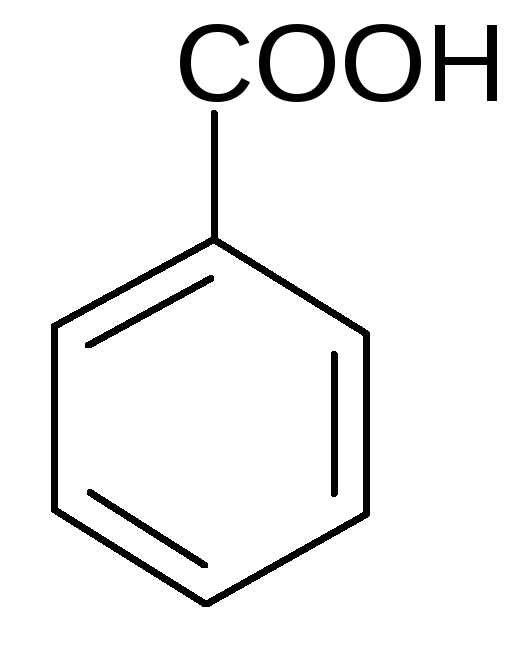
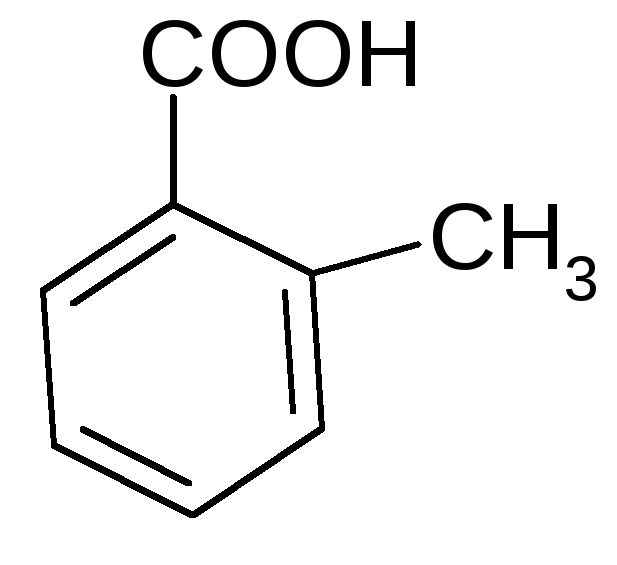
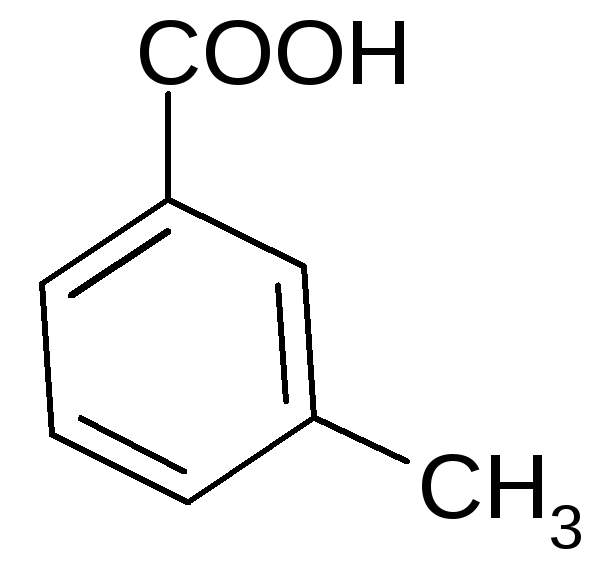
бензойная 2-метил- 3-метил- 4-метил-
кислота бензойная бензойная бензойная
кислота кислота кислота
Карбоновые кислоты известны с давних времен, поэтому для многих из них прочно утвердились тривиальные названия. Происхождение таких названий, как правило, связано с природными объектами, из которых они выделены.
Рассмотрим наиболее широко распространенные одноосновные предельные и непредельные карбоновые кислоты.
|
Формула |
Тривиальное |
ИЮПАК |
|
название | ||
|
Н-СООН |
Муравьиная |
метановая |
|
СН3-СООН |
Уксусная |
этановая |
|
СН3-СН2-СООН |
Пропионовая |
пропановая |
|
СН3-СН2-СН2-СООН |
Масляная |
бутановая |
|
СН3-СН-СООН СН3 |
Изомасляная |
2-метилпропановая |
|
СН3-СН2-СН2-СН2-СООН |
Валериановая |
пентановая |
|
СН2=СН-СООН |
Акриловая |
пропеновая |
