
- •Занятие №1 Ароматические и гетероциклические соединения. Спектральные методы исследования и идентификации органических соединений: электронная и инфракрасная спектроскопия.
- •I. Цель занятия:
- •II. Исходный уровень знаний:
- •III. После изучения этой темы студент должен
- •IV. Основные вопросы темы:
- •VII. Задания для самостоятельной работы на занятии
Занятие №1 Ароматические и гетероциклические соединения. Спектральные методы исследования и идентификации органических соединений: электронная и инфракрасная спектроскопия.
I. Цель занятия:
1.Научиться составлять названия ароматических соединений.
2.Познакомиться с концепцией ароматичности и научиться определять, является ли соединение ароматическим.
3.Изучить химические реакции производных бензола, рассмотреть способы синтеза некоторых лекарственных препаратов на основе бензола .
4.Познакомиться с конденсированными ароматическими системами. Рассмотреть особенности химического поведения этих систем.
5.Познакомиться с пяти-, шестиатомными гетероциклическими соединениями, изучить химические свойства важнейших из них.
6.Познакомиться с биологическими веществами и лекарственными препаратами, содержащими открытые и циклические сопряжённые системы.
7.Познакомиться с некоторыми методами исследования и идентификации сопряженных систем - электронной и инфракрасной спектроскопией
II. Исходный уровень знаний:
1.Теория А.М. Бутлерова.
2.Типы гибридизации атомных орбиталей -sp2 (-sp, -sp3).
3. Основные свойства бензола и его гомологов. Способы получения бензола.
4.Номенклатура радикалов, гомологов, изомеров и производных бензола.
5.Изомерия ароматических углеводородов.
III. После изучения этой темы студент должен
знать:
- строение, изомерию, номенклатуру и характер химических связей в аренах.
- особенности строения и химических свойств сопряжённых алкадиенов
- химические свойства ароматических углеводородов, ориентирующее действие заместителей и особенности биологического окисления аренов.
- механизм реакции электрофильного замещения SE.
- возможные электронные состояния атомов азота и влияние их на основность, нуклеофильность и комплексообразующую способность азотсодержащих соединений.
- строение и свойства пяти - и шестичленных ароматических азотсодержащих гетероциклических соединений.
- строение и свойства пиримидиновых и пуриновых производных.
- возможности использования электронных и инфракрасных спектров для изучения структуры и идентификации сопряженных систем и фрагментов.
уметь:
- определять, является ли соединение ароматическим, а для гетероциклических, кроме того, π-избыточным или π-недостаточным.
- объяснить направляющее действие заместителей и предсказать конечный продукт реакции.
- составлять уравнения химических реакций ароматических и гетероциклических соединений с рассмотрением механизма электрофильного замещения (SE).
IV. Основные вопросы темы:
1.Классификация органических реакций. Электронные эффекты заместителей: индуктивный и мезомерный.
2.Открытые сопряжённые системы: диены, природа химической связи и особенности реакционной способности.
3.Классификация ароматических систем. Условия ароматичности. Термодинамическая устойчивость ароматических систем.
4.Правила замещения в бензольном кольце.
5.Реакции электрофильного замещения в бензольном кольце (SE): галогенирование, нитрование, сульфирование, алкилирование для гомологов и производных бензола. Механизм SE.
6.Особенности реакционной способности ароматических молекул с конденсированными кольцами.
7. π-избыточные (пиррол, фуран, тиофен, индол) и π-недостаточные (пиридин, хинолин, пиримидин) ароматические молекулы. Имидазол. Пурин
8. Особенности химических свойств гетероциклических соединений.
9. Открытые и циклические сопряжённые системы как основа биологически активных
веществ и лекарственных препаратов.
10. Основы электронной и инфракрасной спектроскопии. Возможности использования УФ- и ИК-спектров для определения и идентификации сопряженных фрагментов и молекул.
V. Вопросы и задания для самоподготовки: ( обязательные домашние задания выполняемые в отдельной тетради).
1 Дайте определение «сопряжения» и «ароматичности».
2. Укажите сопряжённые участки в молекулах биологически важных соединений: ретинола, сорбиновой кислоты, циклопентадиена и циклопентадиенил-аниона.
3. Объясните химические свойства систем с открытой цепью сопряжения: реакции электрофильного присоединения. АЕ (1, 2), АЕ (1,4) на примере изопрена.
4.Классификация систем с замкнутой цепью сопряжения. Напишите формулы стирола,фенантрена,фурана,пиримидина.
5.Условия ароматичности. Правило Хюккеля. Энергия сопряжения ароматических молекул. Докажите и сравните ароматичность бензола, нафталина,пиррола и пиридина.
6.Напишите и назовите:
а) 3 ближайших гомолога бензола, их структурные изомеры (там,где они есть,)
б) радикалы - фенил, бензил, (о-, м-, n-) толил.
7.Объясните,почему для аренов характерны реакции электрофильного замещения (SE).
Рассмотрите механизм SE на примере реакции получения толуола (алкилирование бензола).
8.Правила замещения в бензольном кольце. Ориентанты I и II рода. Согласованное и несогласованное действие заместителей. Получите из бензола м-бромнитробензол и п-бромнитробензол.
9.Напишите уравнения следующих реакций и рассмотрите механизм SE:
а) сульфирование толуола
б) нитрование бензойной кислоты
в) бромирование фенола
10.Напишите формулы промежуточных и конечных продуктов в следующих схемах:
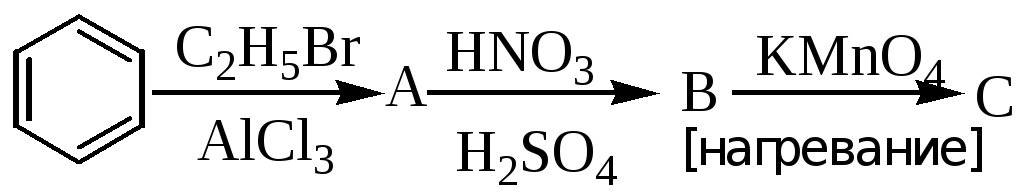
11.Сравните химические свойства конденсированных аренов (нафталина, антрацена, фенантрена) и бензола. Напишите уравнения соответствующих реакций:
а) сульфирование и окисление нафталина
б) гидрирование антрацена
в) бромирование (бромная вода) фенантрена
12.Какие биологически-активные вещества содержат структурные фрагменты конденсированных углеводородов?
13.Гетероциклические пятичленные соединения: пиррол, фуран, тиофен, индол. Почему они называются π-избыточными системами? Что означает термин «пиррольный атом азота»? Напишите уравнения реакций:
а) нитрование фурана
б) сульфирование пиррола
в) алкилирование индола
д) взаимодействия пиррола с натрием.
14. Гетероциклические π-недостаточные системы - пиридин, хинолин, пиримидин. Что означает термин «пиридиновый атом азота». Напишите уравнения реакций и назовите полученные соединения:
а) пиридина с H2О и HNO3
б) сульфирования пиридина
в) окисления 3-метил пиридина
Каково медико-биологическое значение производных хинолина?
15. Имидазол, амфотерные свойства имидазола. Пурин - конденсированная система двух гетероциклов ─ пиримидина и имидазола. Значение в процессах жизнедеятельности.
Пиримидиновые и пуриновые основания.
16.Спектральные методы исследования аренов:
а) электронные спектры поглощения: природа и способы изображения электронных спектров. Связь УФ-спектров со строением сопряженных молекул.
б) инфракрасные спектры: типы колебаний атомов в молекуле. Характеристические частоты. Интерпретация ИК- спектров.
VI. Вопросы для самоконтроля (включены в коллоквиум и зачетное занятие)
1.Что такое сопряжение и ароматичность?
2 Как определить, что следующие молекулы являются ароматическими?
1)
 2)
2)
![]() 3)
3)
![]() 4)
4)
. Назовите их, пронумеруйте атомы в молекулах. Укажите наиболее реакционные центры.
3. Почему заместители СН3, ОН, NH2 (электронодоноры) являются о-, n – ориентантами, а заместители СООН, NO2, SO3H (электроноакцепторы) – м-ориентантами?
4.Приведите примеры согласованного и несогласованного действия заместителей.
5.Почему пиррол – π-избыточная система, а пиррол - π-недостаточная? Докажите это. Что означает «пиррольный атом азота» и «пиридиновый атом азота»?
6.Какое положение (α или β ) пиррола наиболее реакционноспособно в реакциях SE? Почему?
7.Почему пиррол обладает слабокислыми свойствами? Какой реакцией это можно доказать?
8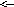

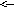
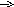
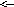
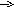 .Как
можно осуществить превращение пиррол
фуран тиофен пиррол?
.Как
можно осуществить превращение пиррол
фуран тиофен пиррол?
9.Что означает ацидофобность пиррола?
10.Вступает ли индол в реакции SE? Какое положение (α или β) наиболее реакционноспособно?
11.Почему пиридин обладает основными свойствами? Покажите это с помощью соответствующих реакций.
12.Легче или труднее вступает пиридин в реакции SE по сравнению с бензолом? Почему?
13.Что такое витамин PP?
14.Сравните химическую активность хинолина, бензола, пиридина в реакциях SE на примере реакции нитрования.
15.Название пара-метилизопропилбензол соответствует соединению:
1)
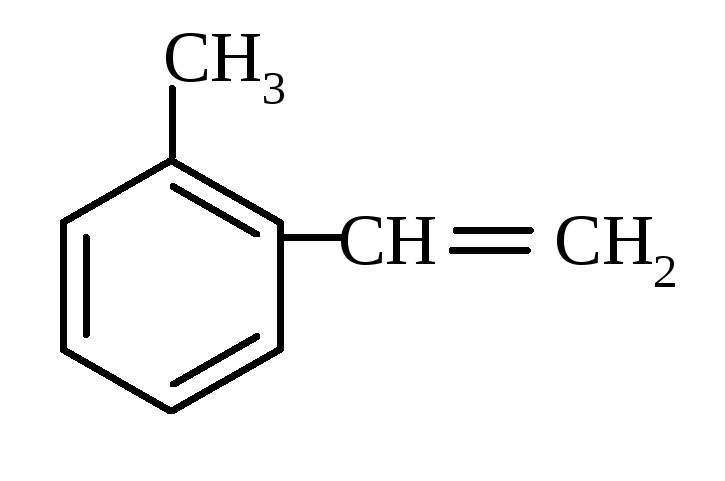 2).
2).
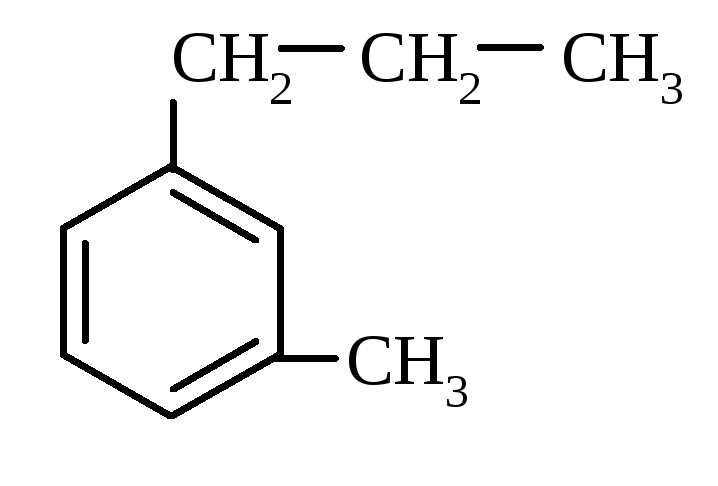 3)
3)
 4)
4)

16. В каком соединении все заместители проявляют электронодонорные свойства:
1)
 2)
2)
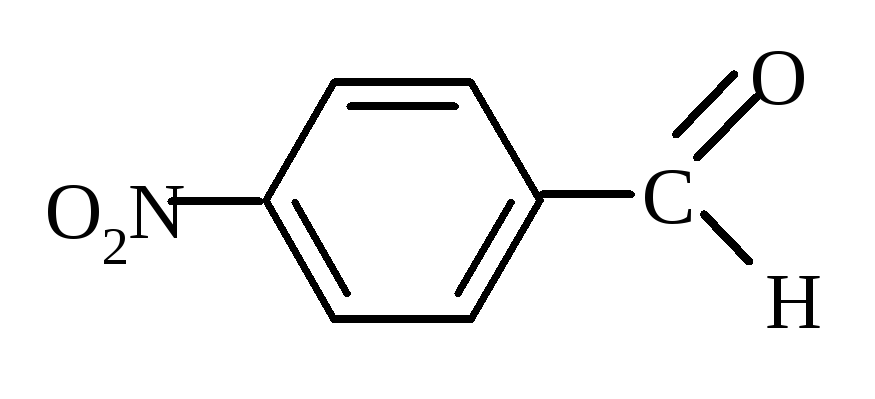 3)
3)
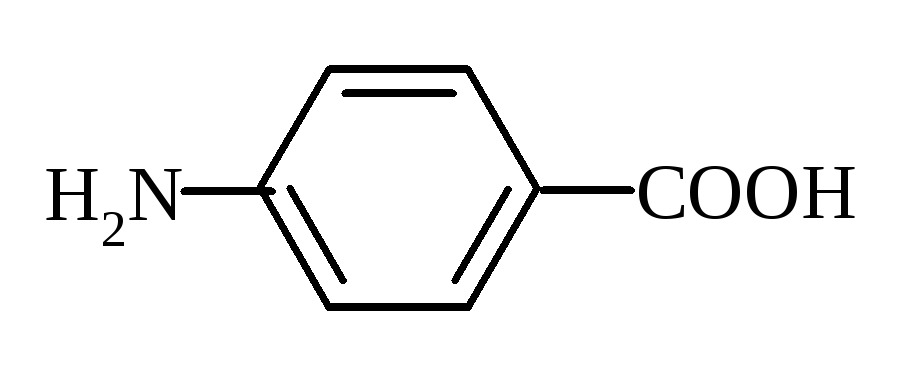 4)
4)

17. Молекула не имеет сопряжённую систему связей:
1)
 2)
2)
![]() 3)
3)
 3)
3)
![]()
18 Инфракрасные спектры позволяют констатировать
1. присутствие в соединении фенильной группы
2. число заместителей
3. положение заместителей в цикле
4. энергию сопряжения
19. Влияние природы заместителей на бензольный хромофор УФ спектра( 1980, A)
1.электронодонорные заместители увеличивают поглощение
2 .электронодонорные заместители уменьшают поглощение
3. электроноакцепторные заместители увеличивают поглощение
4. электроноакцепторные заместители уменьшают поглощение
Ответы
|
15 |
16 |
17 |
18 |
19 |
|
В |
4 |
4 |
1,2,3 |
1 |
