
attachments_21-10-2012_19-29-50 / Лабораторный практикум по химии. Часть 1
.pdf
1.1.4.Возбужденное состояние атома
Вопределенных условиях электроны в атоме могут переходить с орбиталей обладающих минимальной энергией на вакантные орбитали с большей энергией. При этом электроны (и атом в целом) поглощают избыточную энергию, необходимую для этого перехода. Данная энергия излучается атомом при обратном переходе электрона. Состояние атома, когда один или несколько электронов обладают избыточной энергией и находятся на орбиталях с большей энергией, называется возбужденным. Как правило, такие переходы происходят с электронами внешнего уровня и в пределах одного уровня. Если у атома на внешнем уровне нет свободных орбиталей, то у него отсутствует возбужденное состояние.
Пример: электронное строение бора 5В:
|
|
|
|
↑ |
|
|
|
|
|
|
|
|
|
|
↑ |
↑ |
|
|
|
|
5B |
|
↑↓ |
|
|
hv |
5B* |
|
↑↓ |
↑ |
|
(1.9) |
|||||||||
↑↓ |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
2p1 |
|
|
2p2 |
|
|
||||||||||||||
2 |
|
|
1 |
|
|
|
|
|||||||||||||
|
1s2 |
2s |
|
|
|
|
1s2 2s |
|
|
|
|
|
||||||||
Пример: электронное строение кислорода 8O:
|
|
|
|
↑↓ |
↑ |
↑ |
|
hv |
|
8O |
|
|
↑↓ |
(1.10) |
|||||
↑↓ |
|
||||||||
|
|
2p4 |
|||||||
|
2 |
|
|
|
|||||
|
1s2 |
2s |
|
|
|
|
|
||
Возбужденного состояния у атома кислорода нет, т.к. нет свободных орбиталей в пределах второго уровня, а переход на третий уровень энергетически невыгоден.
Пример: электронное строение атома хлора 17Cl:
|
|
|
|
|
|
|
|
|
|
|
|
hv |
|
|
|
|
|
|
|
↑ |
↑ |
↑ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
↑↓ |
↑↓ |
↑ |
|
|
|
|
|
|
|
17Cl* [10Ne] |
|
↑ |
↑ |
↑ |
|
|
|
|
|
|
|
||
17Cl [10Ne] |
|
|
|
|
0 |
|
|
|
|
|
|
|
3 |
|
|
|
|||||||||
↑↓ |
|
|
|
4s0 |
|
|
3d |
|
↑ |
|
|
|
|
4s0 |
|
|
3d |
(1.11) |
|||||||
|
5 |
|
|
|
|
3 |
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
3s2 |
|
|
|
|
|
|
|
|
|
3s1 |
|
|
|
|
|
|
|
||||||||
|
|
3p |
|
|
|
|
|
|
|
|
|
|
3p |
|
|
|
|
|
|
|
|
|
|||
основное состояние |
|
|
возбужденное состояние |
||||||||||||||||||||||
Исходя |
из |
нормального |
|
и возбужденного состояний |
атома, |
можно |
|||||||||||||||||||
предсказать существование различных ионов данного элемента и оценить их окислительно-восстановительные свойства.
1.1.5. Ионизированное состояние атома
При взаимодействии атомов может происходить переход электронов от одного атома к другому, при этом атомы превращаются в заряженные частицы
11

– ионы. Анионы – отрицательно заряженные ионы, приобретают отрицательный заряд за счет присоединения избыточных электронов на внешний уровень нейтрального атома. Катионы – положительно заряженные ионы, приобретают положительный заряд за счет отдачи электронов с внешнего уровня нейтрального атома. Процесс присоединения или отдачи электронов оказывается наиболее выгодными, если в результате его внешний электронный подуровень атома полностью заполняется электронами или становиться полностью вакантным.
Присоединение электронов к атому более выгодно, в случае, если для полного заполнения электронами внешнего подуровня необходимо небольшое количество электронов. Данными свойствами обладают неметаллы:
|
|
|
|
|
|
|
↑↓ |
↑ |
↑ |
|
|
|
|
|
|
|
|
|
↑↓ |
↑↓ |
↑↓ |
|
|
|
|
|
|
|
↑↓ |
+ 2e- |
|
|
|
|
↑↓ |
(1.12) |
|||||||||||
|
0 |
|
|
|
|
|
2p4 |
|
|
|
2- |
|
|
|
|
|
2p6 |
|
|
||||
8O |
↑↓ |
2s2 |
|
|
8O |
↑↓ |
2s2 |
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
1s2 |
|
|
|
|
|
|
1s2 |
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
Способность отдавать электроны (проявлять положительные степени окисления) характерна практически для всех элементов в таблице Д. И. Менделеева. Наиболее легко способны отдавать электроны металлы из-за того, что у них на внешнем уровне небольшое количество электронов. Некоторые элементы способны отдавать разное количество электронов и проявлять разные степени окисления. Максимально возможная степень окисления элемента соответствует номеру группы в таблице Д. И. Менделеева, в которой он расположен.
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
15P [10Ne] |
|
↑ |
↑ |
|
↑ |
|
|
|
|
|
|
|
|
|
|
- 3e- |
15P 3 |
[10Ne |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
↑↓ |
|
4s |
|
|
|
|
3d0 |
|
|
↑↓ |
|
|
|
4s |
|
|
|
|
3d0 |
|
|
|
|
||||||||||||
|
3p |
3 |
|
|
|
|
|
|
0 |
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
3s |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3s |
|
3p |
|
|
|
|
(1.13) |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
hv |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
↑ |
|
|
|
|
|
- 5e- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
15P [10Ne] |
|
|
↑ |
↑ |
|
↑ |
|
|
|
|
|
|
|
|
|
15P 5 |
[10Ne |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
↑ |
|
|
|
|
|
|
3d1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
3d0 |
|
|
|
|
|||||||||
|
|
4s |
|
|
|
|
|
|
|
|
|
|
|
4s |
|
|
|
|
|
|
|
||||||||||||||
|
3p |
3 |
|
|
|
|
|
|
|
|
0 |
|
|
|
|
||||||||||||||||||||
|
|
3s |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3s |
|
3p |
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
1.2.Контрольные вопросы
1.Модель строения атома.
2.Как определить число протонов, нейтронов и электронов в атоме? Приведите пример.
3.Квантовые числа, их физический смысл.
12
4.Принцип Паули и следствия из него.
5.Возбужденное состояние атома.
6.Правило Хунда.
7.Изотопы и изобары.
8.Ионное состояние атомов.
1.3.Контрольные задания
1.Для всех элементов 2 и 3-го периодов таблицы Д. И. Менделеева приведите: а) полную электронную формулу, б) сокращенную электронную формулу, в) сокращенную электронно-графическую формулу элемента в нормальном состоянии, г) сокращенную электроннографическую формулу элемента в ионизированном состоянии.
Пример:
а) 3Li 1s2 2s1 2p0 ; |
|
б) 3Li [2He] 2s1 2p0 ; |
|
|
|
|
|
||||||||||||
в) |
|
Li [ He] |
|
|
|
|
|
г) |
|
Li 1+ |
[ He] |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
↑ |
|
|
|
; |
|
|
|
|
|
|
|
|
. |
|||||
|
|
0 |
|
|
|
|
|
0 |
|
|
|||||||||
|
3 |
2 |
2s1 |
|
2p |
|
3 |
|
2 |
2s0 |
|
2p |
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
2.Приведите сокращенные электронно-графические формулы элементов 25Mn и 35Br в нормальном и ионизированном состояниях. Укажите сходство и различие этих элементов.
3.Приведите сокращенную электронную формулу следующих элементов:
57La, 64Gd, 72Hf, 52Те, 48Cd, 88Ra.
Лабораторная работа 2
КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
Цель работы: Изучить состав, механизм образования и некоторые свойства комплексных соединений, получить представление о структуре, диссоциации и номенклатуре комплексных соединений.
2.1.Теоретическая часть
2.1.1.Общие положения
Комплексные соединения (КС) имеют исключительно большое значение в природе. На основе образования комплексных соединений разработаны
13
эффективные методы получения химически чистых металлов из руд, редких металлов, красителей и др. С использованием комплексных соединений связана возможность получения лаков, красок, электрохимических покрытий, фотоматериалов, средств переработки и консервирования продуктов питания. Гемоглобин и хлорофилл, ответственные за процессы дыхания и фотосинтеза в животных и растительных организмах, являются комплексными соединениями железа (Fe) и магния (Mg).
Как следует из названия, комплексные соединения являются достаточно сложными веществами. В основе любого комплексного соединения лежит центральный атом или ион (называемый комплексобразователем) который способен координировать вокруг себя различные частицы – лиганды (атомы, ионы или молекулы). Вместе, комплексообразователь и лиганды, образуют
внутреннюю сферу комплексного соединения (комплексный ион), которая может являться как заряженной положительно или отрицательно, так и нейтральной. Если комплексный ион является заряженным, то он за счет сил электростатического притяжения способен удерживать ионы противоположного знака, которые образуют внешнюю сферу. Принято, при написании формулы комплексного соединения символы комплексообразователя и лигандов (т.е. частицы образующие внутреннюю сферу) заключать в квадратные скобки, причем символ комплексообразователя указывается первым, а ионы внешней сферы за скобками:
|
внешня |
внешня |
|
|||||||
|
|
сфера |
сфера |
|
||||||
|
|
|
|
|
|
|
|
|||
|
[Ni(H2O)6 |
](NO3 |
)2 |
|
|
|
(2.1) |
|||
|
|
K3[Fe(CN)6] |
||||||||
|
|
|
|
|
|
|
|
внутрення |
|
|
внутрення |
|
|
|
|
||||||
|
сфера |
|
|
|
сфера |
|
||||
Ионы комплексообразователя |
– обычно это |
ионы металлов (кроме |
||||||||
щелочных и щелочно-земельных металлов), например Cr3+, Mn2+, Fe2+, Fe3+, Cu2+, Zn2+, Co2+ и т.д. У всех этих ионов на внешнем уровне есть свободные орбитали.
В качестве лигандов обычно выступают либо анионы (кислотные остатки) либо нейтральные молекулы:
- |
- - |
- |
- |
- |
- |
2- |
- |
2- |
(2.2) |
|
Cl , Br , J , F , OH , CN , CNS , SO4 |
, NO3 |
, CO3 |
, H2O, NH3, CO, NO. |
|||||||
|
|
|
|
|
|
|
14 |
|
|
|
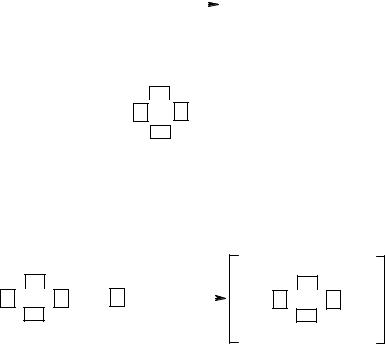
У лигандов обычно имеется свободная пара электронов, за счет которой они способны координироваться вокруг комплексообразователя, образуя химическую связь с комплексообразователем по донорно-акцепторному механизму.
В качестве примера рассмотрим строение комплексного иона [Zn(NH3)4]2-. На внешнем энергетическом уровне иона цинка Zn2+ имеется четыре свободные орбитали:
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
↑↓ |
↑↓ |
↑↓ |
↑↓ |
↑↓ |
|
|
|
|
|
- |
|
2+ |
|
|
|
↑↓ |
↑↓ |
↑↓ |
↑↓ |
↑↓ |
|
|
|
|
|
|||
|
↑↓ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
0 |
|
|
|
|
|
|
|
|
0 |
|
|
||||||||||||||||||
30Zn [18Ar] |
|
|
|
|
3d10 |
|
|
|
|
4p |
|
|
|
|
- 2e |
30Zn |
|
[18Ar] |
|
|
|
|
3d10 |
|
|
|
|
4p |
|
(2.3) |
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
4s |
0 |
|
|
|
|
|
|
|
|||||||||
|
4s |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Молекула аммиака (лиганд) имеет неподеленную пару электронов и
H
. .
H : |
N |
: H |
(2.4) |
. . |
|
|
|
способна образовывать ковалентную связь с ионом цинка (Zn2+) по донорноакцепторному механизму. Ион цинка находится в состоянии sp3-гибридизации и координирует четыре молекулы аммиака:
2+
NH. . 3
|
|
|
+ 4 : NH3 |
|
|
|
|
|
Zn2+ |
|
H3N : Zn2+ |
: NH3 (2.5) |
|||||
|
||||||||
|
|
|
|
|
. . |
|
|
|
NH3
Общее число химических связей, которое образует комплексообразователь с лигандами, называется координационным числом комплексообразователя. Значение координационного числа для различных комплексообразователей определяется его размерами, зарядом и наличием свободных орбиталей у комплексообразователя. Чаще всего координационное число равно 6,4,2.
Следует помнить, что при образовании комплексного соединения вначале образуется комплексный ион (заряд которого равняется алгебраической сумме зарядов комплексообразователя и лигандов), а затем, в зависимости от его заряда, формируется внешняя сфера. Если комплексный ион положителен, то внешняя сфера отрицательна. Такие комплексы относятся к катионным:
15

2+ |
0 2+ |
2+ |
0 2+ - |
|
||
[Zn(NH3)4] (NO3)-2, |
[Cu(H2O)4] Cl2 |
(2.6) |
||||
Если комплексный ион отрицателен, то внешняя сфера положительна. |
||||||
Такие комплексы называют анионными: |
|
|
|
|||
|
+ |
4+ - 2- |
+ 2+ |
- |
2- |
(2.7) |
(NH4)2[PtCl6], |
K2[Cu(CN)4] |
|
||||
У нейтральных комплексов внешняя сфера отсутствует, что связано с отсутствием заряда комплекса:
4+ |
0 - 0 |
0 |
0 0 |
|
[Pt(NH3)2Cl4], |
[Cu(NH3)4] |
(2.8) |
||
2.1.2. Диссоциация комплексных соединений
Анионные и катионные комплексы легко подвергаются диссоциации по типу сильных электролитов с отщеплением внешней сферы, например:
1. диссоциация анионного комплекса:
K3[Fe(CN)6] |
|
|
|
3 K++ [Fe(CN)6]3- |
(2.9) |
|
|
||||
|
|
|
2. диссоциация катионного комплекса:
|
|
|
|
[Cu(NH3)4]2++ SO42- |
(2.10) |
[Cu(NH3)4]SO4 |
|
|
|
||
|
|
||||
|
|
|
Дальнейшая диссоциация самого комплексного иона на комплексообразователь и лиганды идет с большим трудом. Мерой устойчивости комплексного иона служит константа нестойкости комплексного иона (константа диссоциации), обозначается Кн:
|
3- |
|
|
|
|
|
3+ |
|
- |
[Fe(CN)6] |
|
|
|
|
|
|
Fe |
+ 6 CN |
(2.11) |
|
|
|
|
|
|
||||
|
|
|
|
|
|
||||
|
3+ |
|
- |
|
|
6 |
|
||
Кн = [Fe ][CN |
|
] |
= 10-14 |
|
|||||
[[Fe(CN) ]3- |
] |
|
|
||||||
|
6 |
|
|
|
|
|
|
||
Чем меньше значение константы, тем больше тем более устойчив комплексный ион. В справочниках обычно приведено значение показателя константы нестойкости pКн = - lg Кн. Очевидно, чем выше значение рКн, тем прочнее комплексный ион.
16
2.1.3. Номенклатура комплексных соединений
Название комплексного соединения образуется из названий частиц образующих комплексное соединение с указанием их количества. Так, лиганды в комплексных соединениях имеют следующие названия:
|
Ионы: |
Молекулы: |
F- – фторо; |
NO2- – нитрито; |
H2O – аква; |
Cl- – хлоро; |
CN- – циано; |
NH3 – аммин; |
Br- – бромо; |
CNS- – родано; |
NH2R – амин; |
J- – йодо; |
S2- – тио; |
NO2 – нитро; |
OH- – гидроксо; |
PO43- – фосфато; |
CO – карбонил; |
NO3- – нитрато; |
CO32- – карбонато. |
NO – нитрозил. |
Если в комплексном соединении есть несколько однотипных лигандов, то перед их названием указывается их количество греческим числительным:
2 |
– ди; |
5 |
– пента; |
8 |
– окта; |
3 |
– три; |
6 |
– гекса; |
9 |
– нона; |
4 |
– тетра; |
7 |
– гепта; |
10 – дека. |
|
В названии комплексного соединения сначала дается название аниона, затем катиона. После названия комплексообразователя римской цифрой в скобках указывается степень окисления комплексообразователя. Если комплексообразователь входит в состав комплексного аниона, то для названия комплексообразователя используют латинское название элемента комплексообразователя, если комплексообразователь в составе комплексного катиона, то используют русское название элемента комплексообразователя
[Pt(NH3)4Cl2]Cl2 – хлорид дихлоротетраамминплатины (IV), [Fe(H2O)4Cl2]NO3 – нитрат дихлоротетраакважелеза (III), K4[Fe(CN)6] – гексацианоферрат (II) калия, (NH4)2[Mo(CNS)4] – тетрароданомолибдат (II) аммония.
2.1.4. Двойные соли
Двойными солями называют продукты замещения атомов водорода в кислотах на атомы двух различных металлов. В водных растворах двойные соли диссоциируют, образуя два различных катиона и анион, например:
17

NaAl(SO4)2 |
|
|
|
Na+ + Al3++ 2 SO42- |
(2.12) |
|
|
||||
|
|
|
2.2. Экспериментальная часть
Опыт 1. Получение и диссоциация аммиаката меди – соединения с комплексным катионом.
К 5-6 каплям раствора сульфата меди добавьте по каплям раствор аммиака до выпадения осадка основной соли меди (запишите уравнение реакции и отметьте цвет осадка). К этому осадку добавьте избыток раствора аммиака до растворения осадка и образования окрашенного раствора, содержащего комплексный катион (напишите уравнение реакции и укажите цвет раствора). Назовите полученные соединения. Полученный раствор аммиаката меди разделите на две части. В первую пробирку добавьте 1-2 капли раствора гидроксида натрия. Почему не выпадает осадок? Во вторую пробирку добавьте 1-2 капли раствора хлорида бария. Наблюдения запишите.
Напишите уравнения всех реакций и уравнения диссоциации полученных комплексных соединений.
Опыт 2. Комплексные соединения в реакциях обмена.
Вотдельные пробирки налейте по 3-4 капли растворов сульфата меди (II)
ихлорида железа (III). Прилейте в каждую пробирку по 2-3 капли раствора гексацианоферрата(II) калия ( K4[Fe(CN)6] ).
Отметьте цвет полученных соединений. Составьте уравнения реакций в ионной и молекулярной формах. Образование окрашенных комплексных
соединений Cu2[Fe(CN)6] и Fe4[Fe(CN)6]3 используют для обнаружения ионов Cu2+ и Fe3+ в растворах.
Опыт 3. Комплексные соединения в окислительно-восстановительных реакциях.
Налейте в пробирку 5-6 капель раствора перманганата калия (KMnO4), 3-4 капли раствора серной кислоты (H2SO4) и добавьте 3-5 капель раствора гексацианоферрата(II) калия (K4[Fe(CN)6]).
18
Обесцвечивание раствора KMnO4 происходит вследствие восстановления его до сульфата марганца MnSO4. Комплексное соединение
K4[Fe(CN)6] окисляется до K3[Fe(CN)6].
Напишите уравнение окислительно-восстановительной реакции и уравняйте его методом электронного баланса.
Опыт 4. Нестойкость комплексных ионов двойных солей.
В три пробирки налейте по 5-6 капель раствора железо-аммонийных квасцов ( NH4[Fe(SO4)2] ). В первую пробирку добавьте 5-6 капель раствора гидроксида натрия для обнаружения ионов NH4+ (по слабому запаху аммиака) и ионов Fe3+ (по выпадению бурого осадка), во вторую 5-6 капель раствора роданида аммония (NH4CNS) для обнаружения ионов Fe3+, в третью пробирку – 5-6 капель раствора хлорида бария (BaCl2) для обнаружения сульфат ионов SO42-. Напишите уравнения диссоциации квасцов и трех качественных реакций.
Сделайте вывод из проделанных опытов и составьте таблицу 4.1, в которую включите все комплексные соединения из проделанной лабораторной работы и назовите их.
|
|
|
|
|
Таблица 4.1 |
|
|
|
Комплексные соединения |
|
|
||
|
|
|
|
|
|
|
|
Формула |
Комплексообра- |
Лиганды |
Координа- |
|
|
Номер |
зователь и его |
Комплексный ион |
|
|||
опыта |
комплексного |
степень окисле- |
и их |
ционное |
и его заряд |
|
|
соединения, название |
ния |
заряд |
число |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2.3.Контрольные вопросы
1.Дайте определение понятия «комплексные соединения».
2.Состав внутренней и внешней сфер комплексного соединения.
3.Комплексообразователь и лиганды (примеры).
4.Каким бывает и от чего зависит координационное число?
5.От чего зависит заряд комплексного иона?
6.Диссоциация комплексных соединений и двойных солей.
7.Номенклатура комплексных соединений.
19
2.4.Контрольные задания
1.Напишите формулы соединений, содержащих комплексные ионы [Ag(NH3)2]+, [Fe(CN)6]4-, [PtCl6]2- и выражения констант нестойкости для этих ионов. Чему равна степень окисления и координационное число комплексообразователя в данных ионах?
2.Из частиц Co3+, H2O, Na+, Cl- составьте формулы шести комплексных соединений, назовите их и напишите уравнения диссоциации их в водных растворах.
3.Составьте формулы комплексных соединений из предложенных ионов и обсудите их по плану: а) номенклатура; б) строение; в) диссоциация; г) образование химической связи, тип гибридизации и пространственная конфигурация данного соединения.
а) [Fe(H2O)6]3+ и [Fe(CN)6]3-; |
б) [CoF6]3- и [Co(NH3)6]3+. |
Лабораторная работа 3
СКОРОСТЬ ХИМИЧЕСКИХ РЕАКЦИЙ И ХИМИЧЕСКОЕ РАВНОВЕСИЕ
Цель работы: исследовать влияние температуры и концентрации на скорость химических реакций, а также влияние концентрации реагирующих веществ на смещение химического равновесия.
3.1. Теоретическая часть
3.1.1. Химическая кинетика
Учение о скорости химических реакций и механизме их протекания называется химической кинетикой. Системы, в которых протекают реакции, делят на два типа – гомогенные и гетерогенные. Гомогенная система состоит из одной фазы, все реагирующие вещества находятся в одном агрегатном состоянии, и реакция в ней протекает во всем объеме. Гетерогенная система состоит из нескольких фаз (жидкость + газ, жидкость + твердое вещество и т.д.), и реакция в ней протекает на поверхности раздела фаз.
Скорость химической реакции характеризуется изменением концентрации реагирующего или образующегося вещества за единицу времени в единице реакционного пространства. В кинетическом уравнении принято
20
