
- •Обмен белков и аминокислот Курс лекций для студентов специальности
- •«Биологическая химия»
- •Обмен белков и аминокислот
- •Азотофиксация. Нитрогеназа
- •Реакции биосинтеза аминокислот
- •3. Превращение одной аминокислоты в другую.
- •4. Прямое аминирование фумаровой кислоты.
- •Восстановительное аминирование-кетокислот
- •Трансаминирование кислот
- •Взаимопревращения аминокислот
- •Прямое аминирование фумаровой кислоты
- •Синтез незаменимых аминокислот
- •Биосинтез белка
- •Синтез днк – репликация
- •Синтез рнк – транскрипция
- •Биологический код
- •Биосинтез белков – трансляция
- •Понятие о мутациях
- •Переваривание белков
- •Биологическая ценность белков
- •Катаболизм аминокислот
- •Дезаминирование аминокислот
- •Декарбоксилирование аминокислот
- •Обезвреживание аммиака и биогенных аминов
- •Орнитиновый цикл мочевинообразования
- •Список используемой литературы
Трансаминирование кислот
В реакции трансаминирования донором аминогрупп служит в основном глутаминовая кислота, их акцептором – -кетокислоты – промежуточные продукты катаболизма моносахаридов; при этом образуются -кетоглутаровая кислота и соответствующая аминокислота. Эта реакция катализируется пиридоксальзависимым ферментом – трансаминазой:

Если в качестве исходной -кетокислоты используется пировиноградная кислота – конечный продукт гликолиза, то в результате реакции трансаминирования образуется аминокислота аланин (Ала):

Если оксалоацетат (ЩУК), то образуется аспарагиновая кислота (Асп).

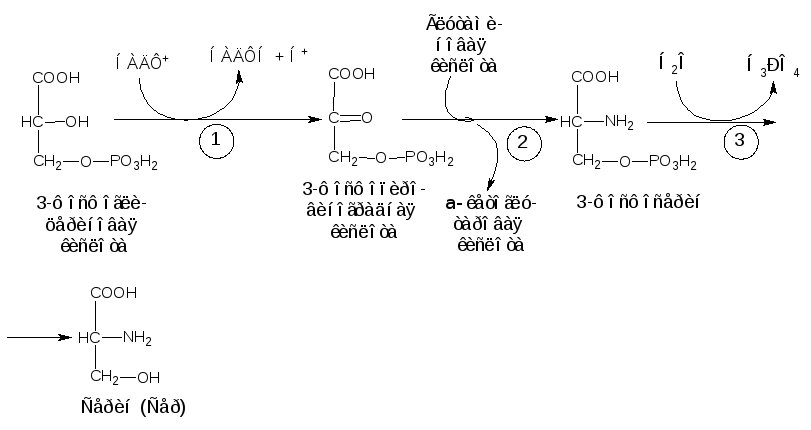
Глутаминовая кислота является донором аминогрупп при синтезе серина (Сер), углеродным скелетом которого является промежуточный продукт гликолиза – 3-фосфоглицериновая кислота. В первой стадии 3-фосфоглицериновая кислота окисляется до 3-фосфопировиноградной, которая подвергается трансаминированию с образованием 3-фосфосерина (реакция 2); последний под действием фосфатазы гидролизуется с образованием серина (Сер) (реакция 3):
Весьма сложен синтез аминокислоты гистидин (Гис). Исходным веществом в формировании имидазольной группы гистидина является АТФ, донором углеродного скелета боковой цепи гистидина служит фосфорибозилпирофосфат, а донором аминогрупп – глутамин. Реакция включает 11 стадий; лишь на последних стадиях синтеза осуществляется процесс трансаминирования.
Взаимопревращения аминокислот
Реакциями восстановительного аминирования -кетокислот и трансаминированием синтезируются заменимые аминокислоты Ала, Асп, Асн, Глу, Глн, Сер.
Такие аминокислоты как пролин, тирозин, цистеин образуются в результате биохимических превращений других аминокислот, в которых принимают участие специфические ферментные системы.
Предшественником пролина (Про) является глутаминовая кислота. В первой стадии реакции Глу восстанавливается в -полуальдегид, затем происходит образование пятичленного гетероцикла с его дальнейшим восстановлением:

Предшественником тирозина (Тир) является незаменимая аминокислота фенилаланин. Он образуется путем гидроксилирования фенильной группы в положении 4. Эта реакция катализируется фенилаланин-4-монооксигеназой в присутствии НАДФН+Н+ и кислорода:

Таким образом, отсутствие в пище незаменимой кислоты фенилаланина ведет к отсутствию в организме и тирозина.
Предшественником глицина (Гли) является серин. Основной путь превращения заключается в переходе трехуглеродной молекулы серина в двухуглеродную молекулу глицина путем отщепления -углеродного атома. Эта реакция катализируется ферментом серингидроксиметилтрансферазой, коферментом которой является тетрагидрофолат, представляющий собой активную форму фолиевой кислоты (вит. Вс). Он является переносчиком группы –СН2ОН от молекулы серина на какой-либо другой акцептор. Отщепляемый от серина -углеродный атом образует метиленовый мостик между атомами азота тетрагидрофолата в положениях 5 и 10, в результате чего синтезируется N5-, N10-метилентетрагидрофолат:

Важнейшим элементом в составе многих биологически активных соединений является сера. Она входит в состав двух аминокислот –цистеина и метионина.
Предшественником цистеина (Цис) является серин, а в качестве источника серы для синтеза цистеина используется неорганический сульфат SO42-.
В растениях и бактериях сульфатная группа восстанавливается в сульфит (SO32-), а затем в сульфид (S2-). Реакция катализируется двумя редуктазами, каждая из которых использует в качестве донора электронов НАДФН + Н+; всего необходимо 4 молекулы НАДФН + Н+ (8 электронов). Синтез цистеина из серина и сульфида идет через промежуточное производное о-ацетилсерин:

