
Ado_A_D_Patologicheskaya_fiziologia
.pdfонного барьера, в норме препятствующего фильтрации белков, не сущих на себе отрицательный заряд (альбумины).
• Гемодинамический фактор, связанный с увеличением гломерулярного капиллярного давления или фильтрационной фракции может обусловить лротеинурию вследствие увеличения диффузионных сил без существенного изменения проницаемости гломерулярных ка пилляров.
Последний механизм обычно способствует нерезкой протеинурии, часто возникающей при застойной сердечной недостаточности, тяжелой артериальной гипертензии.
Гпомерулярная протеинурияхарактеризуется высоким содержанием белка в моче, свыше 4—5 г/сут, а при нефротическом синдроме может до стигать 50 г/сут.
Альбумины преобладают в моче (до 60 % ) , но при тяжелых формах гломерулонефрита (чаще пролиферативных изменениях) в мочу наряду с альбуминами в значительном количестве выделяются и глобулины.
Тубулоинтерстициальные болезни почек служат причиной канальце вой протеинурии. Канальцевая протеинурия может наблюдаться при раз ных формах поражения интерстиция почек (при синдроме Фанкони, кад миевой интоксикации, обструкции мочевых путей, диспротеинемии, радиационном нефрите и др.).
В моче определяются альбумины, низкомолекулярные белки (Р2 - микроглобулин), ферменты — лизоцим. Общее содержание белка при ка нальцевой протеинурии не превышает 1 г/сут, но иногда может дости гать 2 г/сут.
При воспалительных заболеваниях мочевыводящих путей в моче иногда обнаруживаются уроэпителиальные мукопрбтеины и секреторный 1дА, что обычно сопровождается незначительной протеинурией.
Лротеинурию при моноклоновой гаммапатии, миеломной болезни и других заболеваниях, сопровождающихся повышением концентрации аномальных белков в крови, называют протеинурией «перегрузки», по скольку причиной появления аномальных белков в моче является сниже ние реабсорбционных возможностей канальцев.
Выделение аномальных белков с мочой редко сопровождается аль буминурией, последняя возможна при присоединении осложнений (амилоидоза почек).
Ортостатическая протеинурия (у лиц не старше 30 лет) характери зуется появлением (или увеличением) содержания белка в моче в поло жении «стоя» и резким уменьшением протеинурии в положении «лежа».
В отдельных случаях при ортостатической протеинурии содержание белка в моче может приближаться к таковому при заболевании почек, однако прогноз, как правило, благоприятный, у таких пациентов не раз вивается почечная недостаточность.
Появление белка в моче у здоровых людей может быть связано с введением белковых растворов, переливанием крови. Возможно разви-
558
тие кратковременной протеинурии после напряженной мышечной работы и спортивных состязаний.
Появление эритроцитов в моче в значительном количестве называ ется гематурией. В норме количество эритроцитов в моче не должно пре вышать 2 клеток при микроскопии с объективом х45. Гематурия может наблюдаться как при заболеваниях почек (гломерулонефриты), так и при механическом повреждении мочевых путей (уролитиаз). При фазово-кон- трастной микроскопии различают эритроциты гломерулярные (или дисморфные разной формы и размеров) и внегломерулярные — более со хранные клетки.
Появление лейкоцитов в моче свыше 3 клеток при микроскопии с объективом х45 называется лейкоцитурией. Лейкоцитурия, как правило, обусловлена инфекцией мочевого тракта.
Эритроцитарные или лейкоцитарные цилиндры, обнаруживаемые в моче, как правило, свидетельствуют о наличии патологии почек (пораже ние клубочкового аппарата или инфекции в паренхиме почек). Основой образования цилиндров является белок Т а т т - Н о ^ а Н , а также белок, профильтровавшийся из поврежденных гломерул и свернувшийся при определенном рН.
Кристаллурия в значительном количестве (оксалаты, ураты и фос фаты) может совпадать с наличием камней в почках, но может быть и обыч ным явлением в нормальной моче.
24.4. Нефротический синдром
Понятие «нефротический синдром» рассматривают как клинико-био- химический симптомокомплекс, включающий высокую протеинурию (свыше 3,5 г/сут), гипопротеинемию, гиперхолестеринемию и развитие распространенных отеков. Причиной развития нефротического синдро ма могут быть собственно заболевания почек (гломерулонефриты), сис темные заболевания (системная красная волчанка, амилоидоз, сахарный диабет), а также тромбоз почечных вен, злокачественные новообразова ния, паразитарные болезни и многие другие болезни. В связи с этим вы делен первичный и вторичный нефротический синдром соответственно.
Основой развития нефротического синдрома являются увеличенная проницаемость фильтрационного барьера и последующее появление высокой протеинурии.
Причины, способствующие развитию высокой проницаемости клу бочкового фильтра, не установлены. Данные по эффективности иммунодепрессантов при некоторых вариантах нефротического синдрома (так на зываемые «минимальные изменения») косвенно поддерживают точку зрения о возможной роли иммунных механизмов.
Появление высокой протеинурии при нефротическом синдроме с минимальными изменениями связывают с нарушением структуры поли анионного слоя гломерулярных капилляров и выходом главным образом белков, несущих отрицательный заряд.
559

Схема 24.1. Патофизиология нефротического синдрома (Bernard D., Salant D.J. The Principles and Practice of Nephrology / Ред. H. Jacobson etal. — Mosby, 1995, p. 119).
Современный взгляд на характер расстройств при нефротическом синдроме представлен на схеме 24.1.
24.5. Острая почечная недостаточность
Острая почечная недостаточность (ОПН) — синдром, характерным
признаком которого является внезапное нарушение функций почек, со провождающееся накоплением в крови азотистых шлаков и прогресси рующей азотемией.
Некоторые формы ОПН относят к потенциально обратимым патологическим процессам (в отличие от хронической почеч ной недостаточности), поскольку функции почек при ОПН могут быть восстановлены при своевременном устранении повреждающего фактора.
560

Схема 24.2. Причины острой почечной недостаточности (Bonventre J., Shah S.V. et al. The principes and practice of nephrology /
Ред. H. Jacobson etal. — Mosby, 1995).
В зависимости от этиологических факторов ОПН подразделяют на преренальную, ренальную и постренальную (схема 24:2).
Разные этиологические факторы, относящиеся к преренальной и ренал ьной группам, могут обусловитьразвитиеострого тубулярногонекро за — тяжелой формы ОПН.
561
Ишемические факторы особенно многочисленны. Ишемическая ОПН может быть следствием падения «эффективного» внутрисосудистого объе ма (кровотечение, ожоги, потеря жидкости желудочно-кишечным трактом, осмотический диурез и др.) или—- падения «эффективного наполнения артериального русла», но при сохранении общего объема внеклеточной жидкости (застойная сердечная недостаточность, перитонит, анафилакти ческий шок).
Локальная ишемия может быть причиной острого тубулярного не кроза при васкулитах, злокачественной гипертензии, а также при преэклампсии, остром отторжении трансплантата, сепсисе, гепаторенальном синдроме.
Целесообразность использования понятия «острый тубулярный не кроз» признана в тех случаях, когда характер изменений биохимических показателей крови и мочи свидетельствует о тяжелом повреждении ка нальцевой системы почек.
Нефротоксическое влияние чаще обусловлено действием антибио тиков (аминогликозиды), рентгеноконтрастных веществ, химиотерапевтических средств, цитостатиков. В последние годы значительно расши рился перечень этиологических факторов, ведущих к рабдомиолизу или обструкции канальцев другого генеза (гемоглобинурия, уратная нефропатия).
Современное представление о патогенезе ОПН основано главным образом на результатах экспериментальных данных: ишемической мо дели — наложение зажима на почечную артерию или введение норадре налина; нефротоксической модели (аминогликозиды, хлористая ртуть),
миоглобинурической модели (глицерол).
Независимо от характера этиологического фактора повреждение нефрона при ОПН зависит от развития гипоксии или аноксии клеток ка нальцев, клеток сосудистого эндотелия и гладких мышц сосудов.
При ОПН в результате прекращения (или снижения) крово снабжения почек нарушается клиренс отдельных веществ и реабсорбционная функция канальцев.
Патогенез и ш е м и ч е с к о й ОПН. Гипоперфузия почек является пусковым механизмом развития ОПН. На ранних стадиях ишемия обус ловливает комплекс биохимических изменений в эпителии канальцевых клеток, и в эндотелии сосудов (схема 24.3). В зависимости от продолжи тельности ишемии и баланса между тяжестью повреждения и компенса торной возможностью внутриклеточных механизмов достигается определенный функциональный дисбаланс, определяющий дальнейшее прогрессирование или восстановление функций клеток.
Прекращение или уменьшение доступа кислорода к клетке, прежде всего, приводит к нарушению функций митохондрий в связи с нарушени ем синтеза аденозинтрифосфата (АТФ). АТФ снабжает клетки энергией, поэтому падение АТФ прямо или косвенно вызывает повреждение клетки. Например, снижение АТФ регулирующей функцию Ыа+, К+ аденозин-
562
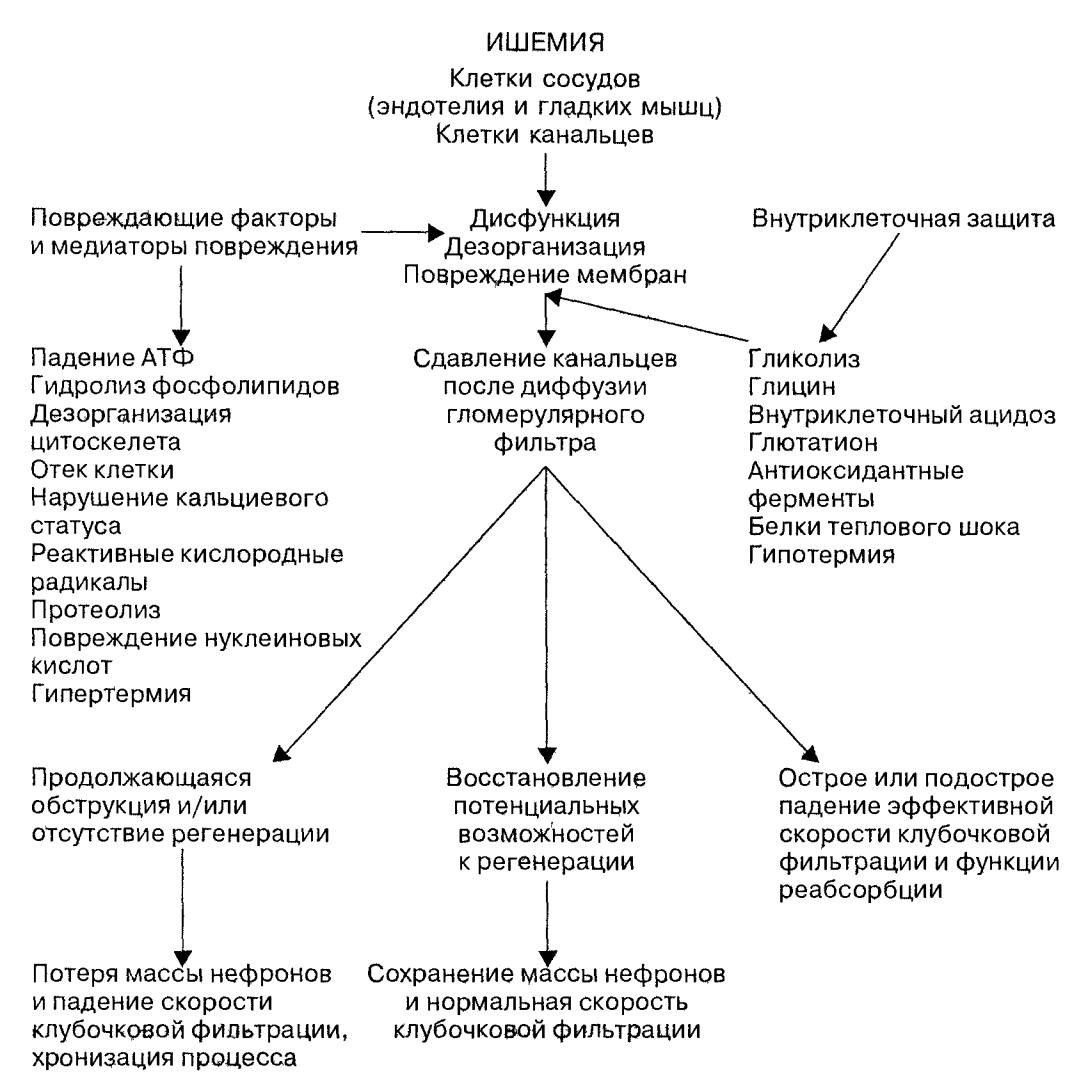
Схема 24.3. Патогенез ишемической ОПН. [модифицированная схема по J. Weinberg: The principes and practice of nephrology /
Ред. H. Jacobson etal. — Mosby, 1995].
трифосфотазы приводит к увеличению внутриклеточного № + , потере К+, деполяризации клеточной мембраны, притоку воды в клетку.
Падение АТФ вызывает также изменение кальциевого статуса в клет ке, поскольку нарушается выкачивание кальция из клетки и увеличивается
цитозольный |
кальций. Увеличение |
цитозольногр |
кальция может |
активиро |
|||
вать |
процесс |
расщепления |
внутриклеточных белков, |
липидов, |
нуклеино |
||
вых |
кислот и |
обусловить |
нарушение |
цитоскелета |
клетки. |
|
|
Ишемическое повреждение эндотелия способствует увеличению проницаемости эндотелия, диффузии плазмы и повышению вязкости кро-
563
ви в сосудах почек. Наряду с этим ишемия влияет на гладкомышечные клет ки сосудов, вызывая дисбаланс между продукцией медиаторов, обуслов ливающих вазоконстрикцию и вазодилатацию, и способствуя нарушению регуляции внутрипочечного сосудистого тонуса (и, таким образом, поте ре функциональной интеграции нефрона).
Продолжающаяся гипоперфузия ссопроввождается прогрессирую щим повреждением клеток проксимальных канальцев и последующим на рушением канальцевой реабсорбции и секреции. Расстройства функций обнаруживают и в дистальных канальцах, включая толстый восходящий сегмент петли Генле. Необратимые изменения или некроз клеток вызыва ют увеличение проницаемости плазменной части мембраны клетки и раз витие закупорки просвета канальцев продуктами распада клеток, образо вавшимися цилиндрами, диффузии гломерулярного фильтрата в интерстиций.
Последствиями этих процессов являются сдавление канальцев отеч ным интерстицием с повреждением апикальной части клеток канальцев, дисфункция канальцев, увеличение внутриканальцевого давления, поте ря эпителиального барьера и уменьшение скорости гломерулярной фильт рации.
Нарушение функций почек при ишемической ОПН. В течение ост рой почечной недостаточности выделяют три стадии:
•начальная;
•стадия олигоанурии;
•стадия восстановления диуреза.
Выделение стадий при ОПН условно. В последние годы доказана воз можность развития ОПН без олигурии, т.е. выделена так называемая неолигурическая форма ОПН, для которой характерны менее тяжелое по вреждение клеток и лучший прогноз,
Тяжесть функциональных расстройств при ОПН определяется тяже
стью повреждения системы канальцев и степенью нарушения СКФ.
Начальная стадия (от нескольких часов до нескольких суток) редко распознается, хотя именно в этот период имеется максимум возможнос тей для восстановления функций почек, если будут распознаны и удале ны этиологические факторы. Распознавание ранней стадии ОПН в клини ке возможно при проведении квалифицированной оценки факторов, потенциально способных вызвать ОПН, так как признаки нарушения функ ций почек могут отсутствовать. При тщательном контроле СКФ на ранней стадии ОПН можно зарегистрировать только нерезкое падение скорости клубочковой фильтрации и в некоторых случаях обнаружить повышение в крови азотистых шлаков.
Вторую стадию обозначают как стадию схабилизации повреждения почек. Продолжительность второй стадии 10—14дней, при тяжелых фор мах ОПН и при присоединении осложнений — до 6 недель. В этот период наблюдают значительное падение почечного кровотока, однако отмече на его региональная неоднородность. Почечный кровоток наружной медул-
564
лярной зоны снижается до 10 20 % от нормы, в то время как почечный кро воток внутренней медуллярной зоны увеличивается, поэтому кортикаль ный почечный кровоток умеренно снижается — до 50 % от нормы. Скорость клубочковой фильтрации в этот период может падать ниже 5—10 мл/мин и при тяжелом течении ОПН низкий уровень СКФ может сохраняться в тече ние 2 нед или более.
Несоответствие между характером изменения почечного кровотока и степенью снижения СКФ свидетельствует об участии разных механизмов в развитии этих расстройств. Предполагают, что падение СКФ при ише мической ОПН связано с нарушением интеграции тонуса афферентной и эфферентной артериолы, регулирующего внутригломерулярное перфузионное давление и последующим изменением коэффициента ультрафильт рации, а также вызвано обструкцией канальцев, выходом канальцевой жидкости и повышением внутриканальцевого давления.
В период второй стадии при олигурической ОПН наблюдается паде
ние диуреза (ниже 400 мл/сут) с последующим нарушением функций про ксимальных канальцев, развитием дисфункций дистальных канальцев, включая толстый сегмент петли Генле. Нарушается реабсорбция натрия,
хлоридов, бикарбонатов, |
концентрация натрия в |
моче увеличивается до 40 |
|
мэкв/л, |
хотя определяется |
низкий удельный вес |
мочи и низкая осмоляль |
ность |
мочи. |
|
|
Нарушение функции разведения и концентрирования мочи обуслов лено расстройством концентрационной способности дистальных каналь цев, частично вследствие потери их чувствительности к АДГ.
Третья стадия — стадия выздоровления характеризуется восстанов лением диуреза или развитием полиурии.
Восстановление диуреза предшествует повышению скорости клубоч ковой фильтрации, хотя в течение последующих нескольких дней падает концентрация в крови креатинина и СКФ достигает нормальных величин в течение 2—4 нед.
Увеличение СКФ в эксперименте обычно регистрируют через 24—48 ч после восстановления диуреза. Восстановление канальцевых и клубочковых функций происходит асинхронно, с умеренным повышением СКФ в течение 1—2 нед и затем более медленным восстановлением канальцевых функций.
Нарушение концентрационной функции почек и способности к подкислению мочи может сохраняться длительный период (годы), несмотря на восстановление диуреза, поэтому
ходим тщательный мониторинг содержания натрия и калия в моче.
Биохимические показатели при ОПН. Характерным для ОПН явля
ется значительное увеличение концентрации креатинина и азота мочеви
ны в крови, однако не всегда степень повышения этих веществ в крови адек ватна степени снижения СКФ, например, при состояниях с повышенным катаболизмом (сепсис, диабет) или применении некоторых лекарств
565
(кортикостероиды) возможно увеличение концентрации азота мочевины при нормальной скорости СКФ. Повышение содержания креатинина — бо^ лее адекватный показатель снижения СКФ при ОПН и только в редких слу чаях (например, ОПН вследствие рабдомиолиза) может значительно воз растать уровень креатинина в крови без сопутствующего снижения СКФ.
Развитие метаболического ацидоза при ОПН обусловлено наруше нием экскреции нелетучих кислот, которые в норме ежедневно продуци руются в организме в результате метаболизма пищевых белков. Ацидозу при ОПН сопутствует накопление в сыворотке отрицательно заряженных анионов, фосфатов и сульфатов. Содержание бикарбонатов в сыврротке у больных ОПН падает до 1 —2 мэкв/л, а при усилении катаболических про цессов (например, при сепсисе) регистрируется более резкое падение бикарбонатов в крови. При различных формах ОПН развитие метаболи ческого ацидоза могут определять разные механизмы. Так, при диабети ческой нефроп^тии возможны кетоацидоз и лактикоацидоз.
Метаболический ацидоз при ОПН может обусловить развитие дыха ния Куссмауля и ряд метаболических и гемодинамических расстройств, например депрессию миокарда с развитием гипотензии, резистентность к инсулину, увеличение катаболизма белков.
Расстройство водно-злектролитного баланса при ОПН способствует к задержке жидкости и гиперволемии, связанной с нарушением экскре ции воды и солей. При неолигурической ОПН наблюдается менее резкое расстройство водно-электролитного баланса, однако неадекватное вве дение жидкости в этих случаях также может обусловить быстрое развитие гиперволемии.
Гиперкалиемия при ОПН может быть следствием нарушения способ ности почек адекватно экскретировать калий, но не всегда проявляется клинически, поскольку она может быть компенсирована функцией дисталь ных канальцев, а также зависеть от наличия или отсутствия олигурии, Из менения на ЭКГ регистрируются при значительном увеличении содержа ния калия в сыворотке — выше 6 ммоль/л, При некоторых формах ОПН содержание калия может сохраняться на нормальном уровне или даже по ниженным, например, при неолигурической форме нефротоксической ОПН, вызванной цисплатином.
Осложнения при ОПН определяются тяжестью расстройств функций сердечно-сосудистой системы (сердечная недостаточность вследствие гиперволемии, аритмии), патологией крови (анемия, нарушение функций тромбоцитов под влиянием увеличения оксида азота и др. причин), невро логическими расстройствами (мышечные подергивания, судороги, уреми ческая энцефалопатия).
Присоединение инфекций — самая частая причина смерти пациен тов ОПН, и связано с подавлением иммунных функций — хемотаксиса ней трофилов, относительной лимфопенией и нарушением клеточно опосре дованной иммунной защиты.
566
24.6. Хроническая почечная недостаточность
Хроническая почечная недостаточность (ХПН) — синдром, развива
ющийся вследствие постепенного снижения функций почек, обусловлен ного прогрессирующей гибелью нефронов. ХПН — в большинстве случа ев необратимый процесс.
Термин «уремия» обычно используют для обозначения конечной ста дии ХПН, когда определяется комплекс биохимических и патофизиологи ческих расстройств и особенно выражены клинические проявления «уре мического отравления».
П р и ч и ны ХПН. Хроническая почечная недостаточность — исход многих болезней почек, чаще исход гломерулонефрита; к ХПН могут при вести интерстИциальные болезни почек, урологическая патология, поликистоз почек, амилоидоз и диабетическая нефропатия, стеноз почечной артерии, системные болезни и др. В последние годы отмечено учащение ХПН как исхода токсического воздействия лекарств.
Стадии ХПН. При медленном прогрессировании ХПН целесообраз но выделить три стадии, которые в определенной степени отражают тя жесть расстройств функций почек. Первая стадия характеризуется паде нием скорости клубочковой фильтрации до 50 % от нормы, т.е. клиренс креатинина составляет 50—60 мл/мин. В этот период у пациентов сохра няется способность поддерживать жизненно важные функции — выделять воду, органические вещества без существенного изменения диеты. При уменьшении массы нефронов и снижении скорости клубочковой фильт рации в крови прежде всего накапливаются соединения, баланс которых поддерживается уровнем клубочковой фильтрации — т.е. азотистые шла
ки, креатийин и (в меньшей степени) мочевина. На ранних стадияхХПН от
мечают нерезкое увеличение этих веществ в крови. Возможно эпизодичес кое повышение их концентрации при воздействии некоторых отягощающих факторов (инфекция, кровотечение или потеря жидкости).
Первую стадию ХПН обозначают как стадию снижения почечного
резерва, т.е. стадией снижения способности к максимально достигаемо му уровню клубочковой фильтрации.
Вторая стадия соответствует снижению СКФ на 75 % от нормы или клиренсу креатинина 20—30 мл/мин. В этот период содержание азотис тых шлаков в крови значительно увеличивается. Однако при стабилиза ции СКФ на уровне 25 мл/мин не всегда регистрируют признаки нару шенного гомеостаза и могут наблюдаться периоды кратковременного снижения концентрации азотистых шлаков. Нарастание тяжести ХПН (сни жение СКФ до 10—15 мл/мин) сопровождается высокой азотемией, рас стройством водно-электролитного баланса, нарушением концентрирова ния мочи, гиперволемией, гиперкальциемией, гиперфосфатемией и развитием метаболического ацидоза.
Дальнейшее прогрессирование ХПН приводит к третьей стадии или стадии уремии, когда клиренс креатинина падает ниже 15 мл/мин, выра жены высокая трудно корректируемая азотемия, расстройство функций многих органов и систем.
567
