- •3) Атмосферная циркуляция и климатообразование
- •6) Биоценоз и биом, классификация сообществ, их географическое районирование
- •7) Географические закономерности распространения организмов и сообществ на суше, в океанах и морях
- •8) Природно-территориальные комплексы, их структура, функционирование, динамика и эволюция
- •9) Природные и природно-антропогенные ландшафты, прикладное ландшафтоведение
- •10) Миграция химических элементов
- •11) Типы элементарных ландшафтов по Полынову б.Б., Перельману а.И., Глазовской м.А.
- •21,22) Экологическое законодательство, право природопользования и правовой механизм охраны окружающей среды
- •23) Юридическая ответственность за экологические правонарушения
- •Масштабы проблемы
- •Регионально-географический аспект продовольственной проблемы
- •Особенности
- •[Править]Область распространения
- •Радиочувствительность
- •30) Экологическая ситуация и здоровье населения
БЛОК 3. ОБЩЕПРОФЕССИОНАЛЬНЫЕ ДИСЦИПЛИНЫ
1)Тепловой баланс земной поверхности
Тепловой баланс Земли, соотношение прихода и расхода энергии (лучистой и тепловой) на земной поверхности, в атмосфере и в системе Земля — атмосфера. Основным источником энергии для подавляющего большинства физических, химических и биологических процессов в атмосфере, гидросфере и в верхних слоях литосферы является солнечная радиация, поэтому распределение и соотношение составляющих Т. б. характеризуют её преобразования в этих оболочках.
Т. б. представляют собой частные формулировки закона сохранения энергии и составляются для участка поверхности Земли (Т. б. земной поверхности); для вертикального столба, проходящего через атмосферу (Т. б. атмосферы); для такого же столба, проходящего через атмосферу и верхние слои литосферы или гидросферу (Т. б. системы Земля — атмосфера).
алгебраическая сумма потоков тепла, приходящих на земную поверхность и уходящих от нее. Выражается уравнением:
![]()
где R — радиационный баланс земной поверхности; P — турбулентный поток тепла между земной поверхностью и атмосферой; LE — затрата тепла на испарение; В — поток тепла от земной поверхности в глубь почвы или воды или обратно. Соотношение компонентов баланса изменяется во времени в зависимости от свойств подстилающей поверхности и географические широты места. Характер теплового баланса земной поверхности и его энергетический уровень определяют особенности и интенсивность большинства экзогенных процессов. Данные о тепловом балансе земной поверхности играют большую роль в изучении изменений климата, географических зональности, термического режима организмов.
2)Климатические пояса Земли
Кли́мат (др.-греч. κλίμα (род. п. κλίματος) — наклон[1]) — многолетний режим погоды, характерный для данной местности в силу её географического положения.
Климат — статистический ансамбль состояний, через который проходит система: гидросфера → литосфера → атмосфера за несколько десятилетий. Под климатом принято понимать усреднённое значение погоды за длительный промежуток времени (порядка нескольких десятилетий) то есть климат — это средняя погода. Таким образом, погода — это мгновенное состояние некоторых характеристик (температура,влажность, атмосферное давление). Отклонение погоды от климатической нормы не может рассматриваться как изменение климата, например, очень холодная зима не говорит о похолодании климата. Для выявления изменений климата нужен значимый тренд характеристик атмосферыза длительный период времени порядка десятка лет.
Климатические пояса и типы климата
Климатические пояса и типы климата существенно меняются по широте, начиная от экваториальной зоны и заканчивая полярной, но климатические пояса являются не единственным фактором, также важное влияние оказывает близость моря, система циркуляции атмосферы и высота над уровнем моря.
Краткая характеристика климатов России:
Арктический: t января −24…-30, t лета +2…+5. Осадки — 200—300 мм.
Субарктический: (до 60 градуса с.ш.). t лета +4…+12. Осадки 200—400 мм.
Умеренно континентальный: t января −4…-20, t июля +12…+24. Осадки 500—800 мм.
Континентальный климат: t января −15…-25, t июля +15…+26. Осадки 200—600 мм.
Резко континентальный: t января −25…-45, t июля +16…+20. Осадки — более 500 мм.
Муссонный: t января −15…-30, t июля +10…+20. Осадки 600—800. мм
В России и на территории бывшего СССР использовалась классификация типов климата, созданная в 1956 году известным советским климатологом Б. П. Алисовым. Эта классификация учитывает особенности циркуляции атмосферы. Согласно этой классификации выделяется по четыре основных климатических поясов на каждое полушарие Земли: экваториальный, тропический, умеренный и полярный (в северном полушарии — арктический, в южном полушарии — антарктический). Между основными зонами находятся переходные пояса — субэкваториальный пояс, субтропический, субполярных (субарктический и субантарктический). В этих климатических поясах в соответствии с преобладающей циркуляцией воздушных масс можно выделить четыре типа климата: материковый, океанический, климат западных и климат восточных берегов.
Экваториальный пояс
Экваториальный климат
Субэкваториальный пояс
Тропический муссонный климат
Муссонный климат на тропических плато
Тропический пояс
Тропический сухой климат
Тропический влажный климат
Субтропический пояс
Средиземноморский климат
Субтропический континентальный климат
Субтропический муссонный климат
Климат высоких субтропических нагорий
Субтропический климат океанов
Умеренный пояс
Умеренный морской климат
Умеренно-континентальный климат
Умеренный континентальный климат
Умеренный резко континентальный климат
Умеренный муссонный климат
Субполярный пояс
Субарктический климат
Субантарктический климат
Полярный пояс: Полярный климат
Арктический климат
Антарктический климат
В мире широко распространена классификация климатов, предложенная русским ученым В. Кёппеном (1846—1940). В её основе лежат режим температуры и степень увлажнения. Согласно этой классификации выделяется восемь климатических поясов с одиннадцатью типами климата. Каждый тип имеет точные параметры значений температуры, количества зимних и летних осадков.
Также в климатологии используются следующие понятия, связанные с характеристикой климата:
Континентальный климат
Морской климат
Высокогорный климат
Аридный климат
Гумидный климат
Нивальный климат
Солярный климат
Муссонный климат
Пассатный климат
3) Атмосферная циркуляция и климатообразование
Общей циркуляцией атмосферы называют систему крупномасштабных воздушных течений над Земным шаром, т. е. таких течений, которые по своим размерам соизмеримы с большими частями материков и океанов. От общей циркуляции атмосферы отличают местные циркуляции, такие, как бризы на побережьях морей, горно-долинные ветры, ледниковые ветры и др.
Разнообразие проявлений общей циркуляции атмосферы в особенности зависит от того, что в атмосфере постоянно возникают огромные волны и вихри, по-разному развивающиеся и по-разному перемещающиеся. Это образование атмосферных возмущений — циклонов и антициклонов — является самой характерной чертой общей циркуляции атмосферы.
Антициклон — это атмосферная масса, вихревое движение воздуха с высоким давлением в центре, по часовой стрелке — в Северном полушарии, против часовой стрелки — в Южном.
Цикло́н — атмосферный вихрь огромного (от сотен до нескольких тысяч километров) диаметра с пониженным давлением воздуха в центре.
Каждому состоянию глобального климата соответствуют свои закономерности в теплообороте, влагообороте и атмосферной циркуляции, т. е. в трех комплексах климатообразующих процессов, формирующих локальный климат в каждой точке Земли. Основными географическими факторами климата являются: географическая широта; высота над уровнем моря; распределение суши и воды на поверхности земного шара; орография (формы рельефа) поверхности суши; океанические течения; растительный, снежный и ледяной покров. Особое место занимает деятельность человеческого общества, в настоящее время также влияющая на климатообразующие процессы и тем самым на климат путем изменения тех или иных географических факторов. Микроклиматом называются местные особенности в режимных метеорологических величинах, обусловленные неоднородностью строения подстилающей поверхности и существенно меняющиеся уже на небольших расстояниях, но наблюдающиеся в пределах одного типа климата. Микроклиматические различия зависят от мелкомасштабных различий в строении и свойствах подстилающей поверхности.
4)Химический состав природных вод
|
Химический состав природных вод | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Химический состав природных вод разнообразен. Воды Мирового океана отличаются от пресных степенью минерализации. В тоже время воды морей могут различаться как по химическому составу, так и по степени минерализации. Состав пресных вод зависит от условий его формирования. Сравнение качества воды различных водных объектов выполняется в соответствии с классификацией природных вод. Классификация природных вод В природных водах, используемых для бытовых целей, обычно присутствуют анионы и катионы, от которых в основном и зависят вкусовые и санитарно-гигиенические свойства воды. Поэтому природные воды в основном классифицируют по степени минерализации по химическому составу. Классификация по степени минерализации Природные воды представляют собой собственно воду - химическое соединение кислорода и водорода - и растворенные в ней вещества, обусловливающие ее химический состав и свойства. В воде растворяются твердые, жидкие и газообразные вещества, которые делятся на три группы:
Минерализацией называют сумму содержащихся в воде минерал веществ. Минерализацию пресных вод принято выражать в м: граммах на литр (мг/л) или граммах на литр (г/л), соленых вод рассолов - в граммах на литр или процентах (%). В зависимости от практического применения существует несколько видов классификации природных вод по степени минерализации,. Наиболее часто используется классификация, представленная в табл. 1.12. Таблица 1.12. Классификация вод по степени минерализации
Классификация по химическому составу
В
подавляющем большинстве случаев
солевой состав природных вод
определяется катионами Са2+,
Мg2+,
Nа+,
К+ и
анионами НСO3-,
Сl- ,
SO42-.
Эти ионы называются главными
ионами воды илимакрокомпонентами;
они определяют химический тип воды.
Остальные ионы присутствуют в
значительно меньших количествах и
называются микрокомпонентами;
они не определяют химический тип
воды.
Классификация природных вод
по химическому составу, предложенная
О. А. Алекиным (рис. 1.13), считается
наиболее приемлемой для вод, используемых
в питьевых и хозяйственно-бытовых
целях. В ее основу положены два
принципа: преобладающих ионов и
соотношения между ними.
Рис.
1.13. Классификация природных вод по
химическому составу
По
преобладающему аниону воды делятся
на три класса: гидрокарбонатные,
сульфатные и хлоридные. Воды каждого
класса делятся, в свою очередь, по
преобладающему катиону на три группы:
кальциевую, магниевую и натриевую.
Каждая группа подразделяется на 4
типа по соотношению содержащихся в
воде ионов (в эквивалентах). При этом
класс природных вод обозначается
символом соответствующего аниона: С
— НСО3-,
S — SO42-,
Сl — Сl-;
группа: символом катиона: К+,
Na+,
Са2+,
Мg2+;
тип - римской цифрой.
Формула воды
записывается следующим образом. К
символу класса добавляется нижний
индекс - значение минерализации (с
точностью до 0,1 г/л ), к символу группы
- верхний индекс - значение общего
катионного состава (с точностью до
целых единиц вещества в ммоль/л),
например:
С1,2 Nа0,5 -
гидрокарбонатно-натриевая вода с
общей минерализацией 1,2 г/л и
преобладающей концентрацией
гидрокарбонатных ионов и ионов
натрия.
В природных водах присутствуют
также растворенные газы. В основном
это газы, которые диффундируют в воды
из атмосферы воздуха, такие как
кислород, углекислый газ, азот. Но в
то же время в подземных водах или
водах нецентрализованных источников
водоснабжения, в минеральных и
термальных водах могут присутствовать
сер водород, радиоактивный газ радон,
а также инертные и другие газы.
В
табл. 1.13 представлены ионы, наиболее
часто встречающиеся в природных
водах. Таблица 1.13. Ионы, наиболее часто встречающиеся в природных водах
Растворимые и слаборастворимые соли в природных вода
Возвращаясь
к главным ионам пресных вод, необходимо
отметить, что их катионный и анионный
состав определяется наличием в
осадочных породах хорошо растворимых
минералов. Поэтому в воде присутствуют
катионы К+ и
Nа+ и
анионы Сl-;
и SO42-.
Ионы кальция и магния с карбонатным
ионом CO32- (продукт
второй ступени диссоциации угольной
кислоты) образуют малорастворимые
соединения - так называемые соли
жесткости. Эти соединения представлены
в природе в виде известняков, мелов,
мраморов, кальцитов, доломитов и
других минералов, содержащих карбонаты
кальция и магния. В то же время
бикарбонатные ионы HCO3-(продукт
первой ступени диссоциации угольной
кислоты) образуют хорошо растворимые
соединения с ионами кальция и
магния. Карбонатные ионы присоединяют
ион водорода и превращаются в
бикарбонатный ион:
СО32- +
Н+ —› НСО3-.
При
высоких концентрациях водородных
ионов (высокой кислотности соответствует
низкое значение рН - меньше 6) происходит
растворение карбонатов, поэтому в
природных водах могут присутствовать
бикарбонатные ионы , карбонатные ионы
, а также катионы жесткости Са2+ и Мg2+
.
Между этими составляющими существует
строгое равновесие, которое связано
с содержанием в воде углекислого
газа, катионов жесткости и бикарбонатных
ионов.
Угольная кислота имеет две
ступени диссоциации:
Н2СО3 —› Н+ +
НСО3-;
НСО —› Н+ +
СО32-.
и
существует, в основном, в виде
углекислого газа, концентрация
которого определяется парциальным
давлением СО2 в
атмосфере и его растворимостью в
соответствии с таблицей растворимости
газов.
В зависимости от содержания
в природной воде различных форм
угольной кислоты природная вода имеет
различное значение водородного
показателя (рис. 1.14).
Правильно также
и другое положение: концентрация
водородных ионов определяет соотношение
между бикарбонатными HCO32- и
карбонатными CO32- ионами.
Рис.
1.14. Соотношение форм угольной кислоты
в воде при различных значениях
рН
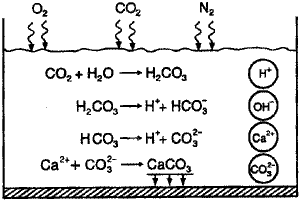
Динамическое
равновесие между углекислым газом,
анионами угольной кислоты, ионами
кальция и нерастворимым карбонат
кальция в какой-то степени может быть
пояснено рис. 1.15.
Рис.
1.15. Образование карбоната кальция
Из
рисунка видно, что при снижении
кислотности раствора концентрация
водородных ионов снижается, рН раствора
повышается и ( приобретает щелочную
реакцию, бикарбонаты переходят в
карбонаты, которые после взаимодействия
с ионами кальция образуют растворимый
карбонат кальция. Происходит осаждение
кристаллической фазы карбоната
кальция. И, наоборот, при повышенной
кислотности воды карбонатные ионы
переходят в бикарбонатные, что приводит
к растворению карбоната кальция
СаСО3.
Кстати, приблизительно по такой же
схеме происходит вымывание кальция
из костей скелета и зубов. Примеси, встречающиеся в воде
Вода
является великолепным растворителем,
в котором могут растворяться минеральные
и органические вещества, созданные
как природой, так и человеком. Говорят,
что «вода камень точит». И в то время
в ней могут присутствовать вещества
во взвешенном состоянии: частицы
песка и глины, коллоидные и механические
примеси и живые существа различных
форм и размеров. Исходная, чистая вод
попадающая на землю в виде дождя,
снега, града, росы, изморози и тумана,
насыщаясь различными веществами и
организмами, загрязняется и, как
правило, становится непригодной для
питья или использования в быту без
предварительной очистки.
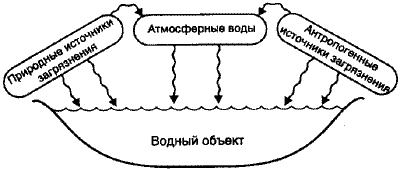
Источниками
загрязнения природных вод могут быть
как природные объекты, так и объекты,
созданные руками человека (рис.
1.16).
Значительное воздействие на
природные водные объекты оказывает
сельскохозяйственное производство.
Интенсификация оросительного
земледелия приводит к поднятию уровня
грунтовых вод и усилению; засоленности
почв с последующим исключением их из
сельскохозяйственного оборота.
Рис.
1.16. Источники загрязнения природных
вод
В
природные водные объекты поступают
канцерогенные и другие вредные для
здоровья людей вещества. Многие
природные вещества в процессе
подготовки воды для питьевого
водоснабжения могут стать канцерогенными
- это вторичное загрязнение природных
вод. Водные объекты могут быть
загрязнены в результате судоходства,
сброса хозяйственно-бытовых и
сельскохозяйственных сточных вод.
При этом происходит и термическое
загрязнение водных объектов.
Присутствующие в сточных водах фосфор
и азот (температура этих вод, как
правило, выше температуры природных
вод) способствуют развитию сине-зеленых
водорослей. Интенсивное использование
воды для охлаждения оборудования
также ведет к термическому загрязнению
вод, в результате чего повышается их
температура, снижается содержание
кислорода и, соответственно, способность
водоемов к самоочищению.
К антропогенным
источникам поступления канцерогенных
веществ в природные воды относятся
производственные и природные сточные
воды, ливневые и талые воды, протекающие
по загрязненной территории, хранилища
нефтепродуктов, свалки и захоронения
твердых и жидких отходов, отвалы
шлаков и пепла, хранилища минеральных
удобрений, животноводческие комплексы,
пыль и стоки автомобильных дорог и
т. д.
К числу природных источников
канцерогенных веществ необходимо
отнести залежи горючих ископаемых
(сланцы, полиметаллические,
асбестосодержашие, селитровые и
мышьяковистые руды), геотермальные
и минеральные воды.
Вещества,
поступающие в водные объекты,
насчитывают десятки и сотни тысяч
наименований. Для того чтобы признать
эти загрязнения или вещества, в
которые они могут трансформироваться,
потенциально опасными для здоровья
человека, необходимо проведение
специальных исследований. Для всего
спектра загрязнений такие исследования
провести невозможно.
На территории
РФ действует утвержденный Минздравом
СССР «Перечень веществ, продуктов,
производственных процессов и бытовых
факторов, канцерогенных для человека».
К их числу отнесены асбесты,
бенз(а)пирен(1,2,3), винилхлорид(1,2),
неочищенные минеральные масла, мышьяк
и его соединения и многие другие
вещества.
Санитарные правила и
нормы, определяющие гигиенические
требования к питьевой воде источников
централизованного и нецентрализованного
водоснабжения, содержат нормативы
предельно допустимых концентраций
веществ, которые могут оказать
канцерогенное или иное вредное
воздействие на организм
человека.
Канцерогенное воздействие
полиароматических (циклических)
углеводородов (ПАУ), к числу которых
относится и бенз(а)пирен, наиболее
изучено. Опасность поступления их с
водой сравнительно невелика. Многие
ароматические углеводороды могут
накапливать в организмах гидробионтов,
которые в свою очередь являются пищей
для человека.
Опасны для человека
и хлорорганические соединения,
присутствующие в воде. Это, в первую
очередь, полихлордифенилы (ПХД) и
дельные пестициды (ДДТ, ГХЦГ и
гексахлорбензол). Строение
некоторых циклических углеводородов
представлено на рис. 1.17. Эти
соединения обладают высокой
стабильностью в условиях окружающей
среды.
При обработке природных вод
хлорированием из неканцерогенных
«предшественников» могут образовываться
опасные в канцероген» отношении
галогенсодержащие соединения (ГСС).
В питьевой воде может содержаться до
100 ГСС, среди них наиболее часто и в
небольшем количестве встречаются
хлороформ, дихлорбромметан,
дибромхлорметан, бромоформ, 4-хлористый
углерод, дихлорэтан, трихлорэтан,
тетрахлорэтан и др. Причем в
нехлорированной воде эти вещества,
по мнению ряда исследователей, не
встречаются или встречаются в
минимальном количестве. Наибольшее
количество ГСС образуется при
хлорировании природных компонентов,
таких как гуминовые кислоты, дубильные
вещества, винилиновая и галловая
кислоты, а также фульвокислоты,
метаболиты водорослей - всего более
80 веществ.
Микроорганизмы и паразиты, присутствующие в воде
В
природных водах присутствуют и
размножаются микроорганизмы, водоросли,
ракообразные, рыбы, земноводные, в
толще воды развиваются личинки комара,
на поверхности воды живут водомерки.
Многие из этих организмов, называемых
гидробионтами, являются опасными для
здоровья и жизни человека, например,
огромные морские хищники - акулы - или
небольшие хищные рыбы пираньи. Но и
небольшие микроорганизмы - микробы
- могут нанести непоправимый вред
здоровью человека.
В воде могут
присутствовать также микроскопические
личинки паразитов, амебные цисты,
бактерии в споровой форме и другие
патогенные формы. Основным источником
патогенных организмов, распространяемых
водой, являются фекалии человека и
теплокровных животных, а также
фекально-бытовые сточные воды.
Фекальные загрязнения воды ухудшают
ее качество, а патогенные микроорганизмы,
попадающие в воду с выделениями
теплокровных животных и человека,
могут явиться причиной заболеваемости
кишечными инфекциями. Среди патогенных
микроорганизмов чаще других
обнаруживаются в загрязненных
водах сальмонеллы, шигеллы, пастереллы,
вибрионы, микобактерии, энтеровирусы
человека, амебные цисты, личинки
нематод, энтеропатогенные Е.Соli и
др.
Сальмонеллы
(Salmonellа) -
это представители рода сальмонелл,
в который входит около 2000 различных
грамм-отрицательных микроорганизмов,
похожих друг на друга по внешнему
строению и воздействию на человека.
Эти микробы вызывают заболевание
желудочно-кишечного тракта, называемое
сальмонеллезом. В воде сальмонеллы
сохраняются до 120 дней; эффективно
дезинфицируются раствором хлорной
извести.
Шигеллы
(Shigеllа) -
это дизентерийные микробы, поражающие
отдел толстой кишки человека;
вызывают дизентерию (шигеллез) с
признаками интоксикации. Они хорошо
сохраняются в воде и даже могут
размножаться. На них губительно
действуют высокая температура и
дезинфицирующие средства.
Амебные
цисты,
попадающие в организм человека с
загрязненной водой, вызывают амебиаз
- болезнь кишечника, иногда осложняющаяся
абсцессами печени, головного мозга,
поражением Легких и др гих органов.
Возбудитель относится к классу
простейших (Епtamoeba
histolitiса),
размер ее может достигать 20-30
мкм.
Лептоспироз -
острое инфекционное заболевание,
передающееся человеку от животных.
Однако возможен и водный путь передачи
инфекции. Болезнь характеризуется
поражением почек, печени, центральной
нервной системы и мышц, сопровождается
интоксикацией и лихорадкой. Возбудителем
лептоспироза являются лептоспиры
(Leptospirа interrogans) -
спиралевидные организмы, приспособлений
для жизни в воде. Ежегодная заболеваемость
во всем мире составляет 1%, но при
контакте с домашними животными может
достигать В литературе описана вспышка
лептоспироза у 50 человек, которые
купались в реке, протекавшей вблизи
пастбища для коров и свиней.
В этом
ряду инфекционных заболеваний, водный
путь возникновения которых является
наиболее вероятным, необходимо
отметить холеру. Эта
болезнь в XIX в. вызывала в Европе
пандемии. Заболевания холерой были
отмечены в 1947 г. в Египте, в 1964 г. - в
Иране и Ираке, в 1970 г. - в Советском
Союзе (Одесса и Астрахань). В последние
годы вибрионы
холеры были
обнаружены в водоемах Москвы,
Санкт-Петербурга, Тамбова.
Не исключена возможность их появления
и в водоемах других регионов России.
Распространение холеры связано с
нарушениями карантинов, усилением
миграции людей - носителей холерного
вибриона, а также с перевозкой
загрязненных продуктов и воды кораблями
и самолетами.
Возбудителем холеры
являются вибрионы
(Vibrio cholerae).
Холерный вибрион хорошо переносит
низкие температуры и даже замораживание.
При кипячении погибает через 1 мин,
при воздействии дезинфицирующих
средств - почти сразу.
Некоторые
вирусы человека могут передаваться
через воду при ее загрязнении фекалиями.
К ним относятся возбудители инфекционного
гепатита, полиомиелита, энтеровирусных
инфекций, вызывающих поражение
центральной нервной системы, мышц,
миокарда и кожных покровов.
Возможность
передачи вирусов водным путем можно
продемонстрировать на примере вирусного
гепатита.
Самая большая вспышка вирусного
гепатита отмечена в 1955-1956 гг. в Дели.
Несколько тысяч человек были
инфицированы в результате употребления
воды из централизованной системы
водоснабжения. Дело в том, что в
природной воде присутствовали
возбудители кишечных заболеваний,
вирус гепатита и другие патогенные
формы. Обработка воды хлорированием
привела к подавлению возбудителей
кишечных инфекций, но не смогла
подавить вирус гепатита. Этому
препятствовала высокая мутность
исходной воды: вирусы как бы прятались
во взвешенных частицах. В 1996 г.
инфицирование вирусным гепатитом
при употреблении питьевой воды было
отмечено и в России.
Независимо от
происхождения присутствующие в
природных водах примеси можно
объединить в группы по размеру и
физико-химическому состоянию. В
соответствии с классификацией,
разработанной Л. А. Кульским, примеси
(загрязнения) природного и антропогенного
происхождения подразделяются на 4
группы. Первые две группы относятся
к гетерогенным (неоднородным), другие
две - к гомогенным (однородным). В
зависимости от принадлежности примеси
к определенной группе и производится
выбор способа очистки природных
вод.
К первой группе примесей
относятся кинетически неустойчивые
взвеси. Это водоросли, бактерии,
суспензоиды, эмульсоиды и др., снижающие
прозрачность воды (увеличивающие ее
мутность). Более крупные примеси
удаляются фильтрованием, микропроцеживанием
или центрифугированием, остальные
удаляются механическим путем,
коагулированием, флотацией, адгезией
на высокодисперсных и зернистых
материалах, агрегированием при помощи
флокулянтов,
электрофильтрацией.
Воздействие на бактерии тяжелых
металлов (серебра и др.), окислителей,
ультразвука и ультрафиолета способствует
подавлению их жизнедеятельности.Ко
второй группе относятся
агрегативноустойчивые примеси -
вещества, находящиеся в коллоидной
форме. Эти примеси могут быть удалены
ультрафильтрацией, окислением,
адсорбцией, коагулированием.
К
третьей группе относятся
молекулярно-растворенные примеси,
такие кие как газы и органические
вещества биологического происхождения.
Для удаления этих примесей используют
аэрацию, нагревание, окисление,
экстракцию, адсорбцию на активированном
угле и биохимический распад.
И
наконец, четвертая группа примесей
- электролиты. Их удаляют из природной
воды гиперфильтрацией (обратным
осмосом), переводом в малорастворимые
соединения, сепарацией при помощи
фазовых переходов, фильтрованием
через ионообменные материалы, а также
с помощью электродиализа.
Как следует
из данной классификации, нет абсолютно
надежно способа очистки воды от
содержащихся в ней примесей, кроме,
может быть, дистилляции. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
5)водный режим рек , его фазы и основные элементы
Водный режим. Скорость течения в Р. колеблется в больших пределах — от нескольких см/сек (равнинные Р.) до 6—7 м/сек (горные Р.) и распределяется неравномерно по живому сечению (См. Живое сечение) Р. С повышением уровня воды скорость течения, как правило, увеличивается на плёсах и уменьшается на перекатах. Кроме течения, направленного в общем вдоль русла, в речных потоках наблюдаются циркуляционные, винтообразные течения, характер и направление которых зависят от конфигурации русла в поперечном разрезе и в плане. Вследствие турбулентного перемешивания на многих Р. температура воды распределяется равномерно по всему живому сечению Р. температура воды в Р. в тёплый период следует (с некоторым отставанием) за ходом температуры воздуха. Во время ледостава температура воды около 0°С.
Во́дный режи́м — изменения во времени расхода воды, уровней воды и объёмов воды в водотоках (реках и других), водоёмах (озёрах, водохранилищах и других) и в других водных объектах (болота и другие).
В районах с тёплым климатом на водный режим рек основное влияние оказывают атмосферные осадки и испарение. В районах с холодным и умеренным климатом также очень существенна роль температуры воздуха.
[править]Фазы водного режима
Различают следующие фазы водного режима: половодье, паводки, межень, ледостав, ледоход.
Половодье — ежегодно повторяющееся в один и тот же сезон относительно длительное увеличение водности реки, вызывающее подъём её уровня; обычно сопровождается выходом вод из меженного русла и затоплением поймы.
Паводок — сравнительно кратковременное и непериодическое поднятие уровня воды, возникающее в результате быстрого таяния снега при оттепели, ледников, обильных дождей. Следующие один за другим паводки могут образовать половодье. Значительные паводки могут вызвать наводнение.
Межень — ежегодно повторяющееся сезонное стояние низких (меженных) уровней воды в реках. Обычно к межени относят маловодные периоды продолжительностью не менее 10 дней, вызванные сухой или морозной погодой, когда водность реки поддерживается, главным образом, грунтовым питанием при сильном уменьшении или прекращенииповерхностного стока. В умеренных и высоких широтах различают летнюю (или летне-осеннюю) и зимнюю межень.
Ледостав — период, когда наблюдается неподвижный ледяной покров на водотоке или водоёме. Длительность ледостава зависит от продолжительности и температурного режима зимы, характера водоёма, толщины снега.
Ледоход — движение льдин и ледяных полей на реках.
Неравномерный в течение года режим питания рек связан с неравномерностью выпадения атмосферных осадков, таяния снега и льда и поступления их вод в реки.
Колебания уровня воды вызываются в основном изменением расхода воды, а также действием ветра, ледовых образований, хозяйственной деятельностью человека.