
- •2. Биологическая роль
- •3. Классификация углеводов
- •4. Моносахариды (простые углеводы)
- •4.4. Стереоизомерия
- •4.5. D- и l-Стереохимические ряды
- •4.6. Оптическая активность
- •4.8. Таутомерия
- •4.9. Циклические формы сахаров-
- •2) Формулы Хеуорса
- •4.10. Конформация
- •1. Дезоксисахара
- •2. Аминосахара
- •Теоретическая часть
- •Циклические формы Ациклическая форма
- •I. Доказательство наличия -он групп
- •II. Реакции с участием карбонильной группы-
- •III. Реакция Селиванова на фруктозу
- •IV . Общая реакция углеводов с (реакция Молиша)
- •2. Хитин
- •3. Крахмал
- •4. Гликоген.
I. Доказательство наличия -он групп
Моносахариды, подобно глицерину, в водных растворах взаимодействуют со свежеобразованным гидроксидом меди с образованием сахаратов ярко-синего цвета, которые устойчивы, так как являются хелатными комплексами катиона меди.
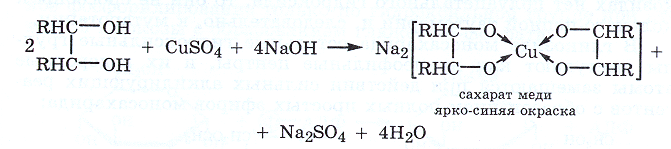
II. Реакции с участием карбонильной группы-
а)Альдозы. Реакции
мягкого окисления углеродного атома
альдегидной группы катионами
![]() и
и![]() (окислители)
лежат в основе таких качественных
реакций на альдозы, как 1) реакция
«серебряного зеркала» (реактив Толленса
-
(окислители)
лежат в основе таких качественных
реакций на альдозы, как 1) реакция
«серебряного зеркала» (реактив Толленса
-![]() )
или 2) реакция образования
)
или 2) реакция образования![]() красно-кирпичного
цвета
(реактив Фелинга –раствор калиево-натриевой
соли винной кислоты или тартрат - ионы),
или 3) реактив Бенедикта – цитратный
(соли лимонной кислоты) комплекс
красно-кирпичного
цвета
(реактив Фелинга –раствор калиево-натриевой
соли винной кислоты или тартрат - ионы),
или 3) реактив Бенедикта – цитратный
(соли лимонной кислоты) комплекс
![]() или
цитрат- ионы.Тартрат
и цитрат – ионы используют для стабилизации
или
цитрат- ионы.Тартрат
и цитрат – ионы используют для стабилизации
![]() .
.

Блестящий налет
на стенках пробирки
Красно-кирпичный
цвет
Продукты окисления альдегидной группы альдоз называются гликоновыми кислотами.
Гликозиды не дают положительной пробы с этими реагентами, так как не могут самопроизвольно образовать альдозу.
б) Кетозы. Несмотря на устойчивость кетонов к окислению, также дают положительные пробы Фелинга и Толленса. Объясняется это тем, что в щелочной среде, в которой проводятся эти реакции, кетозы частично изомеризуются в альдозы.
Изомеризация (кето-енольная таутомерия):
1. в щелочной среде
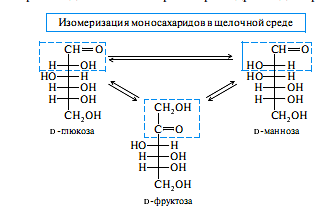
Первой стадией изомеризации альдоз является обратимое образование 1,2-ендиоль-ной структуры под действием основания при участии СН-кислотного центра — атома С-2. Превращение ендиола в карбонильную форму происходит тремя путями (а - в), как показано на схеме. Путь а приводит к кетозе; два других пути отличаются стерической напраатенностью, в результате чего образуются исходная альдоза (путь б) и ее эпимер по С-2 (путь в).

Например, D-глюкоза в растворе гидроксида кальция за 20 дней при 20 °С образует 29% D-фруктозы и 1 % D-маннозы, а с D-маннозой за сутки в 0,5 М растворе гидроксида натрия превращение происходит на 28% и в растворе гидроксида бария — на 40%.
2. в кислой среде
1) . Как и в щелочной среде, начинаются с енолизации фрагмента С-1—С-2.

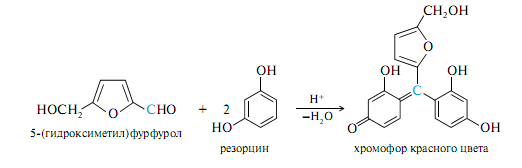
2) Дальнейшие превращения 1,2-ендиола связаны не только с образованием изомерных карбонильных соединений или разрывом связи С—С, но и с отщеплением молекулы воды. Одно из направлений дегидратации сопровождается образованием производных фурфурола, которое приводится ниже только схематически. Из пентоз при этом получается фурфурол, из гексоз — 5-(гидроксиметил) фурфурол.


Реакции окисления используют в структурных исследованиях и биохимических анализах для обнаружения моносахаридов, в частности глюкозы в биологических жидкостях (моча, кровь).
III. Реакция Селиванова на фруктозу
Для кетоз характерна реакция Селиванова- нагревание с хлороводородной кислотой в присутствии резорцина, приводящее к продуктам, окрашенным в красный цвет, альдозы дают более слабую окраску только при длительном нагревании.
В реакцию Селиванова кетозы (фруктоза) вступает легче гексоз и на этом основано определение фруктозы в присутствии других сахаров.
Пентозы с НCl и флороглюцином дают фиолетово-красную окраску раствора.
