- •2. Биологическая роль
- •3. Классификация углеводов
- •4. Моносахариды (простые углеводы)
- •4.4. Стереоизомерия
- •4.5. D- и l-Стереохимические ряды
- •4.6. Оптическая активность
- •4.8. Таутомерия
- •4.9. Циклические формы сахаров-
- •2) Формулы Хеуорса
- •4.10. Конформация
- •1. Дезоксисахара
- •2. Аминосахара
- •Теоретическая часть
- •Циклические формы Ациклическая форма
- •I. Доказательство наличия -он групп
- •II. Реакции с участием карбонильной группы-
- •III. Реакция Селиванова на фруктозу
- •IV . Общая реакция углеводов с (реакция Молиша)
- •2. Хитин
- •3. Крахмал
- •4. Гликоген.
![]()
На какие классы подразделяются углеводы.
Какая качественная реакция является общей для всех углеводов и почему?
С помощью каких реакций можно доказать наличие в молекулах углеводов гидроксильных групп? Приведите примеры.
Напишите формулы открытых форм глюкозы, фруктозы, рибозы, дезоксирибозы.
Какие виды изомерии имеют место у моносахаридов? Сколько оптических изомеров соответствует глюкозе?
Напишите циклические формулы (по Хеуорсу)
 .
.Какие два типа дисахаридов известны? Чем они отличаются по строению и свойствам?
Какие углеводы относят к гомо- и гетерополисахаридам? Приведите примеры
Какие продукты обнаруживаются при гидролизе сахарозы, крахмала, целлюлозы? Какой вывод можно сделать о строении данных соединений?
Будет ли сахароза взаимодействовать с фелинговой жидкостью?
Почему крахмал и гликоген не дают положительной реакции с фелинговой жидкостью?
Вопросы к теме №10

![]()
Определение, биологическая роль
Термин «углеводы введен профессором Тартуского университета К. Шмидтом, в 1844 г.
Углеводы (сахара) – это обширный класс органических соединений, к котору относятся полиоксикарбонильные соединения и их производные.
В растениях УГ составляют до 80% сухой массы, а в животных организмах – не более 2% сухой массы.
2. Биологическая роль

3. Классификация углеводов
Углеводы подразделяют по способности к гидролизу (моносахариды не гидрализуются).
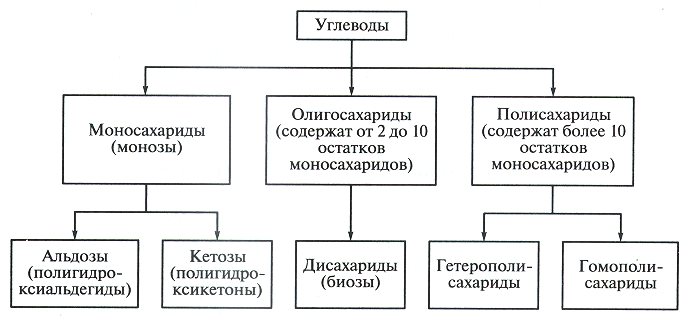
По физико-химическим свойствам углеводы делят на:
нейтральные содержащие только гидроксильные и карбонильные группы;
основные включающие кроме названных аминогруппу (аминосахара) – см ниже;
кислые, ее держащие кроме гидроксильных и карбонильных групп карбоксильные группы.
4. Моносахариды (простые углеводы)
4.1. Моносахариды-
гетерополифункциональные
соединения, содержащие карбонильную и
несколько гидроксильных групп. Общая
молекулярная формула:
![]() (где n=3,4,5 и т.д).
(где n=3,4,5 и т.д).
4.2. Классификация. Классифицируют с учетом двух признаков:
природы карбонильной группы открытой формы: альдозы — полигидроксиальдегиды и кетозы — полигидроксикетоны.
длины углеродной цепи (т.е. от числа атомов углерода в цепи): триозы (С-3), тетрозы (С-4), пентозы, гексозы, гептозы, октозы нонозы, декозы.
Полная классификация учитывает оба признака — длину углеродной цепи и характер карбонильной группы
4.3. Номенклатура. В основу международной номенклатуры сахаров положены тривиальные названия. Для альдоз характерно окончание или суффикс – оза (ксилоза, рибоза, глюкоза, и др. ), а для кетоз- улоза ( рибулоза, ксилулоза).
Производные моносахаридов

Например:

![]()
![]()
4.4. Стереоизомерия
В
молекулах открытых форм пентоз и гексоз
содержится от двух до четырех
асимметрических атомов углерода
(показаны звездочками на схеме ___),
поэтому одной и той же структурной
формуле соответствуют несколько
стереоизомеров — энантиомеров
и диастереомеров. Так, число стереоизомеров
альдопентоз
равно
8 (![]() ,
гдеп
=
3), среди которых 4 пары энантиомеров. У
альдогексоз
будет уже 16 стереоизомеров, т. е. 8 пар
энантиомеров, так как в их углеродной
цепи содержится четыре асимметрических
атома углерода (т.е. 4 разных заместителя).
,
гдеп
=
3), среди которых 4 пары энантиомеров. У
альдогексоз
будет уже 16 стереоизомеров, т. е. 8 пар
энантиомеров, так как в их углеродной
цепи содержится четыре асимметрических
атома углерода (т.е. 4 разных заместителя).
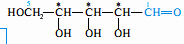

Альдопентоза Альдогексоза
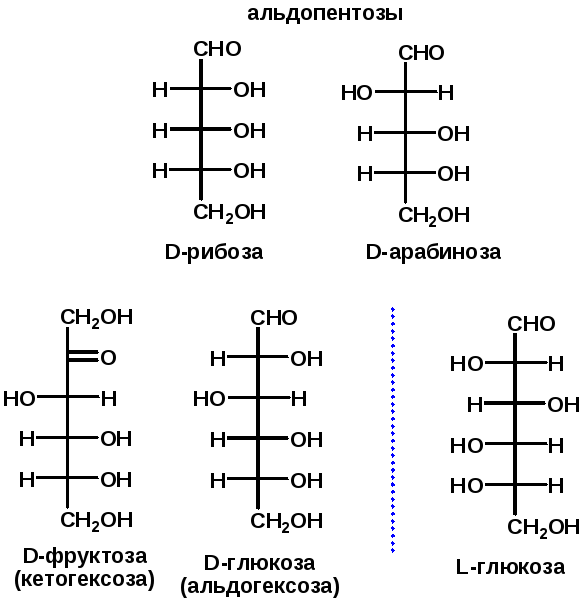
4.5. D- и l-Стереохимические ряды
Отнесение моносахарида к D- или L-стереохимическому ряду проводят по конфигурации хирального центра, наиболее удаленного от оксогруппы, независимо от конфигурации остальных центров. Для пентоз таким «определяющим» центром будет атом С-4, а для гексоз — атом С-5 (углеродная цепь нумеруется с того конца, ближе к которому находится старшая функциональная группа, а именно карбонильная группа).
Структуры открытых форм моносахаридов записывают в виде проекционных формул Фишера, располагая углеродную цепь вертикально с атомом С-1 наверху.
Центр хиральности,
определяющий принадлежность к
стереохимическому ряду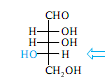

![]()
![]()
Положение гидроксильной группы у последнего центра хиральности справа свидетельствует о принадлежности моносахарида к D-ряду, слева — к L-ряду, т. е. так же, как и в стереохимическом стандарте — глицериновом альдегиде.
Большинство природных моносахаридов принадлежит к D-ряду.
4.6. Оптическая активность
Природные
моносахариды обладают оптической
активностью – свойством вращать
плоскость поляризованного света. Любой
моносахарид с конкретными физическими
свойствами характеризуется специфической
величиной – удельным вращением
![]() .
.
При длительном стоянии растворов сахаров удельное вращение меняется.
Следует подчеркнуть, что стереохимические символы D и L никак не связаны с вращением плоскости поляризованного света вправо или влево, которое обозначается знаками (+) или (-) и определяется экспериментально. Например, принадлежащие к одному стереохимическому ряду две альдопентозы — D-рибоза и D-ксилоза — имеют разные знаки оптического вращения.

4.7. Наиболее важные триозы, пентозы, гексозы
.