
- •Методы анализа кислоты аскорбиновой в растворе для инъекций и их валидация
- •План работы
- •Глава 1. Кислота аскорбиновая, свойства, анализ, применение (обзор литературы).
- •Глава 2. Методы анализа кислоты аскорбиновой в растворе для инъекций и их валидация (экспериментальная часть).
- •Глава 1. Кислота аскорбиновая, свойства, анализ, применение (обзор литературы). 1.Общая характеристика кислоты аскорбиновой.
- •2. Получение кислоты аскорбиновой.
- •3. Свойства кислоты аскорбиновой.
- •4. Способы идентификации аскорбиновой кислоты
- •4.1. Химическими методами.
- •4.1.1. Кислотные свойства [1,18,19, 28,29]:
- •Проведения экстракции спиртом 96%.
- •4.2.2. Идентификация и дискриминация кислоты аскорбиновой методом бик-спектроскопии
- •4.2.3. Анализ уф-спектров кислоты аскорбиновой
- •Количественное определение кислоты аскорбиновой.
- •5.1. Титриметрические методы
- •Физико-химические методы
- •Биологическая роль
- •Авитаминоз и гипервитаминоз
- •Суточная норма потребления
- •Фармакодинамика
- •Фармакокинетика
- •Лекарственные формы
- •Выводы по обзору литературы
- •Глава 2. Методы анализа кислоты аскорбиновой в растворе для инъекций и их валидация (экспериментальная часть).
- •1.1.Установление специфичности в тестах «Испытание на подлинность»
- •Валидационная оценка методики анализа кислоты аскорбиновой йодатометрическим методом
- •Валидационная оценка методики анализа кислоты аскорбиновой в растворе йодатометрическим методом по показателю «Прецизионность»
- •3.Валидационная оценка методики анализа кислоты аскорбиновой йодиметрическим методом
- •Общие выводы.
- •Литература
Глава 1. Кислота аскорбиновая, свойства, анализ, применение (обзор литературы). 1.Общая характеристика кислоты аскорбиновой.
|
|
|
|
Аскорбиновая кислота —органическое соединение, родственноеглюкозе, является одним из основных веществ в человеческом рационе, которое необходимо для нормального функционирования соединительной и костной ткани. Выполняет биологические функции восстановителя икоферментанекоторыхметаболических процессов, являетсяантиоксидантом. Биологически активен только один из изомеров —L-аскорбиновая кислота, который называют витамином C. В природе аскорбиновая кислота содержится во многих фруктахиовощах[21].
2. Получение кислоты аскорбиновой.
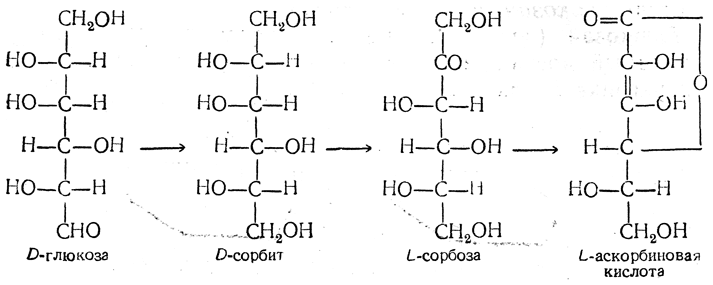
Синтетически получают из глюкозы. Синтезируется растениями из различных гексоз (глюкозы, галактозы) и большинством животных (из галактозы), за исключением приматов и некоторых других животных (например, морских свинок), которые получают её с пищей. Схема синтеза кислоты аскорбиновой:
Источники витамина С
Наиболее богаты аскорбиновой кислотой плоды барбадосской вишни(1000-3300 мг/100 г), свежегошиповника(650 мг/100 г),болгарского красного перца(250 мг/100 г),чёрной смородиныиоблепихи(200 мг/100 г),яблоки(содержат 165 мг/100 г),перец зелёный сладкийипетрушка(150 мг/100 г),брюссельская капуста(120 мг/100 г),укропичеремша(колба) (100 мг/100 г),киви(90 мг/100 г),земляника садовая(60 мг/100 г),цитрусовые(38-60 мг/100 г)[12], недозрелые плоды грецкого ореха,хвоя сосныипихты[31].
3. Свойства кислоты аскорбиновой.
По физическим свойствам аскорбиновая кислота представляет собой белый кристаллический порошок без запаха, кислого вкуса. Легко растворим в воде, растворим в спирте.tпл. 190-193°С (с разложением).
Из-за наличия двух асимметрических атомовсуществуют четыредиастереомерааскорбиновой кислоты. Две условно именуемыеL- иD- формы хиральныотносительно атома углерода вфурановомкольце, аизо- форма является D-изомером по атому углерода в боковой этиловой цепи.
Удельное вращение от +22° до +24° (2%-ный водный раствор).
Раствор кислоты аскорбиновой в буферном растворе (pH 7) имеет максимум поглощения при 265 нм [1].
Химические свойства [19, 28]:
Окислительно - восстановительные свойства. Аскорбиновая кислотав мягких условиях легко окисляется в дегидроаскорбиновую (лактон2,3-дикетогулоновойкислоты), могущую столь же легко вновь восстанавливаться:

Кислотнные свойства. Аскорбиновая кислота является у-лактоном, содержащим два спиртовых гидроксила в 5 и 6 положениях и два енольных гидроксила во 2 и 3 положениях. Енольные гидроксилы обладают кислотными свойствами, дают кислую реакцию на лакмус, взаимодействуют и с NaОН и с NaHCO3. Кислотные свойства более выражены у гидроксила в 3-ем положении:
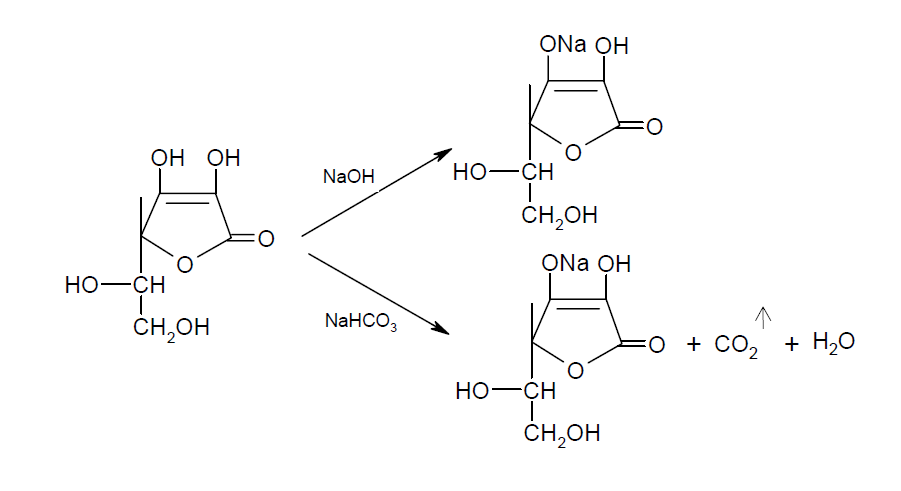 Следует
иметь в виду, что аскорбиновая кислота
является лактоном и
при действии
сильных щелочей лактонное кольцо
гидролизуется, а затем
образуется
фурфурол [28]:
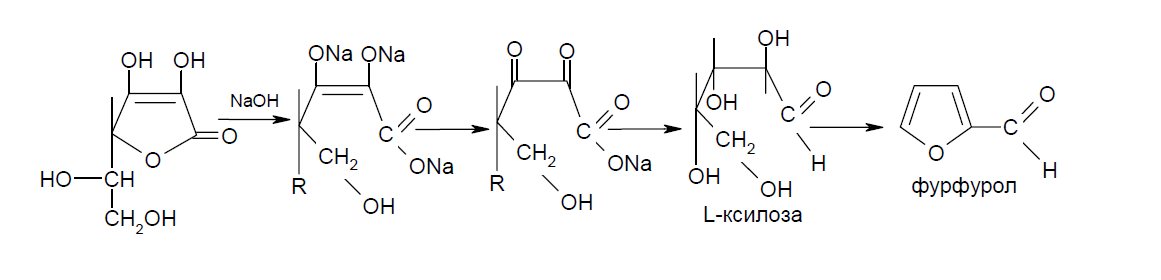
Следует
иметь в виду, что аскорбиновая кислота
является лактоном и
при действии
сильных щелочей лактонное кольцо
гидролизуется, а затем
образуется
фурфурол [28]:
Кислота аскорбиновая имеет характерный спектр поглощения в УФ-области и ИК области [3].
Инфракрасный спектр субстанции, снятый в диске с калия бро- мидом, в области от 4000 до 400 см-1 по положению полос поглощения должен соответствовать рисунку спектра аскорбиновой кислоты (рис. 1).

Рис. 1 ИК-спектр поглощения кислоты аскорбиновой.
Ультрафиолетовый спектр поглощения 0,001 % раствора субстанции в 0,1 М растворе хлористоводородной кислоты в области от 230 до 300 нм должен иметь максимум при 243 нм (рис. 2).

Рис. 2 УФ-спектр поглощения кислоты аскорбиновой.


