
Химия (Строение атома) (презентация)
.pdf
Структура учебного процесса
Очное обучение |
|
Дистанционное обучение |
|
|
|
лекции
лабораторные работы
практические занятия
самостоятельная аудиторная работа
самостоятельная домашняя работа (типовой расчет)
контроль (защиты, коллоквиумы, зачет, экзамен)
Учебники и учебные пособия
Н.В.Коровин. Общая химия
Курс общей химии. Теория и задачи (под ред. Н.В.Коровина, Б.И.Адамсона)
Н.В.Коровин и др. Лабораторные работы по химии
Календарный план
Число |
Нед |
|
Лаб. |
Практич. |
Число |
Нед |
|
|
|
Лаб. |
Практич. |
|||||||||
|
|
|
раб. |
занятия |
|
|
|
|
|
раб. |
|
|
раб. |
|||||||
01.09- |
1 |
|
|
|
|
|
09.11- |
11 |
|
Колл. |
|
Электролиты, |
||||||||
04.09 |
|
|
|
|
Хим.эквива |
13.11 |
|
|
||||||||||||
|
3(1) |
|
|
|
|
|
С. р. |
|
|
гидролиз, ПР |
||||||||||
07.09- |
2 |
|
|
16.11- |
12 |
|
|
|
|
|||||||||||
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
лент |
|
|
|
№ 2 |
|
|
|
|||||||||
11.09 |
|
|
|
|
|
20.11 |
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
14.09- |
3 |
4(1), |
|
|
Электр.форму- |
23.11- |
13 |
13(2) |
|
|
|
|
|
|
|
|||||
18.09 |
|
|
27.11 |
|
|
ГЭ, электролиз, |
||||||||||||||
|
27(13,16) |
|
|
|
|
14(2) |
|
|
||||||||||||
21.09- |
4 |
|
|
лы. |
30.11- |
14 |
|
|
||||||||||||
|
|
|
|
коррозия |
||||||||||||||||
25.09 |
|
|
|
|
|
Квант.числа |
04.12 |
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
07.12 |
15 |
17(2) |
|
|
|
Колл |
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
11.12 |
18(2) |
|
|
|
|
С.р. |
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
28.09- |
5 |
|
|
|
|
|
14.12- |
16 |
|
|
|
|
|
|
|
|
№3,4 |
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
02.10 |
|
5(1) |
|
|
Хим.связь |
18.12 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
05.10- |
6 |
|
|
21.12- |
17 |
|
|
|
|
|
|
|
|
|
|
|
|
|||
09.10 |
|
|
|
|
Комплексы |
25.12 |
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
12.10- |
7 |
|
|
|
|
|
28.12- |
18 |
|
|
|
|
|
|
|
|
|
|
|
|
16.10 |
|
Защита |
|
Термодинамика |
29.12 |
|
|
|
|
|
|
|
Зачет |
|||||||
8 |
|
|
|
|
|
|
|
|
|
|
||||||||||
19.10- |
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
С.р №1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
2310 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
26.10- |
9 |
|
|
|
|
|
Январь |
|
|
|
|
|
|
|
Экзамен |
|||||
30.10 |
|
|
|
|
Кинетика. |
|
|
|
|
|
|
|
||||||||
|
6(2,3) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
02.11- |
10 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
06.11 |
|
|
|
|
Равновесие |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Введение в курс химии
Химия в энергетическом институте – фундаментальная общетеоретическая дисциплина.
Химия – естественная наука, изучающая состав, строение, свойства и превращения веществ, а также явления, сопровождающие эти превращения.
М.В.Ломоносов |
(1741 |
г.) |
– |
Д.И.Менделеев |
(в |
|||
“Химическая |
|
|
наука |
|||||
|
|
“Основах химии” 1871 |
||||||
рассматривает |
свойства |
и |
||||||
г.) – “Химия – |
это |
|||||||
изменения |
тел, |
состав |
тел, |
|||||
учение об элементах и |
||||||||
объясняет |
причину |
того, |
что |
с |
||||
их соединениях”. |
|
|||||||
телами |
при |
|
химических |
|
||||
|
|
|
||||||
превращениях происходит”.
«Золотой век химии» (конец XIX начало XX веков)
Периодический закон Д.И.Менделеева (1896)
Понятие о валентности введенное Э.Франкландом (1853)
Теория строения органических соединений А.М.Бутлерова (1861-1863)
Теория комплексных соединений А.Вернера
Закон действующих масс М.Гультберга и Л.Вааге
Термохимия, разработанная в основном Г.И.Гессом
Теория электролитической диссоциации С. Аррениуса
Принцип подвижного равновесия А.Ле Шателье
Правило фаз Дж.В.Гиббса
Теория сложного строения атома Бора-Зоммерфельда (1913-1916)

Значение современного этапа развития химии
Понимание законов химии и их применение позволяет создавать новые процессы, машины, установки и приборы.
Получение электроэнергии, топлива, металлов, различных материалов, продуктов питания и т.п. непосредственно связано с химическими реакциями. Например, электрическую и механическую энергии в настоящее время в основном получают преобразованием химической энергии природного топлива (реакции горения, взаимодействия воды и ее примесей с металлами и т.п.). Без понимания этих процессов невозможно обеспечить эффективную работу электростанций и двигателей внутреннего сгорания.
Познание химии необходимо для:
-формирования научного мировоззрения,
-для развития образного мышления,
-творческого роста будущих специалистов.
Современный этап развития химии характеризуется широким использованием квантовой (волновой) механики для интерпретации и расчета химических параметров веществ и систем веществ и основан на квантово-механической модели строения атома.

Атом - сложная электромагнитная микросистема, являющаяся носителем свойств химического элемента.
СТРОЕНИЕ АТОМА
ЯДРО |
|
|
ЭЛЕТРОННАЯ |
протоны (р, р+) |
|
|
ОБОЛОЧКА |
нейтроны (n, no) |
|
|
электроны (е-) |
(нуклоны) |
|
|
∑ Zp = ∑Zе- |
Массовое число |
35Cl (17p+, 18n, 17e-) |
||
Заряд ядра |
17 |
||
|
|
||
Изотопы – разновидности атомов одного химического
элемента, имеющие одинаковый порядковый номер, но разные атомные числа
Мr(Cl)=35*0,7543 + 37*0,2457 = 35,491

Основные положения квантовой механики
Квантовая механика - поведение движущихся микрообъектов (в том числе и электронов) – это
одновременное проявление, как свойств частиц, так и свойств волн – двойственная (корпускулярноволновая) природа.
Квантование энергии: Макс Планк (1900 г., Германия) –
вещества испускают и поглощают энергию дискретными порциями (квантами). Энергия кванта пропорциональна частоте излучения (колебания) ν:
E = h·ν
h – постоянная Планка (6,626·10-34Дж·с); ν=с/λ, с – скорость света, λ – длина волны
Альберт Эйнштейн (1905 г.): любое излучение - это поток квантов энергии (фотонов) E = m·v2
Луи де Бройль (1924 г., Франция): электрон также характеризуется корпускулярно-волновой двойственностью - излучение распространяется как волна и состоит из мелких частиц (фотонов)
|
|
Частица – m, |
mv, E =mv2 |
|
|
|
|
|
|
1 |
|
|
Волна - , , |
|
E2 = h = hv/ |
|
|
|
Связал длину волны с массой и скоростью: |
||||
|
|
Е1 = Е2; |
|
=h/ mv |
|
Принцип |
неопределенности |
- |
Вернер Гейзенберг (1927г., |
||
Германия) |
- |
произведение |
неопределенностей |
положения |
|
(координаты) |
частицы х и |
импульса (mv) не |
может быть |
||
меньше h/2
х (mv) h/2 ( - погрешность, неопределенность) Т.е. положение и импульс движения частицы принципиально невозможно определить в любой момент времени с абсолютной точностью.
Электронное облако Атомная орбиталь (АО)
Т.о. точное нахождение частицы (электрона) заменяется понятием статистической вероятности нахождения ее в определенном объеме (около ядерного) пространства.
Движение е- имеет волновой характер и описывается
волновой функцией - |
= (х,у,z) |
|
2dv - плотность вероятности нахождения е- в определенном объеме около ядерного пространства. Это пространство называется атомной орбиталью (АО).
В 1926 г Шредингер предложил уравнение, которое математически описывает состояние е- в атоме. Решая его
находят волновую функцию . В простом случае она зависит от 3-х координат
Электрон несет отрицательный заряд, его орбиталь представляет собой определенное распределение заряда и называется электронное облако
КВАНТОВЫЕ ЧИСЛА
Введены для характеристики положения электрона в атоме в соответствии с уравнением Шредингера
1. |
2. |
3. |
4. |
Главное |
Орбитальное |
Магнитное |
Спиновое |
квантовое |
квантовое |
квантовое |
квантовое |
число (n) |
число (l) |
число (ml) |
число (ms) |
1.Главное квантовое число (n)
Определяет энергию электрона - энергетический уровень
показывает размер электронного облака (орбитали)
принимает значения – от 1 до
n (номер энергетического уровня): 1 2 3 4 и т.д.
K L M N
Ее увеличивается (чем дальше от ядра, тем энергия больше)
2.Орбитальное квантовое число (l) :
определяет – орбитальный момент количества движения электрона
показывает – форму орбитали
принимает значения – от 0 до (n-1)
Графически АО изображается 
 Орбитальное квантовое число: 0 1 2 3 4
Орбитальное квантовое число: 0 1 2 3 4
Энергетический подуровень : s p d f g
Е увеличивается
|
|
z |
l =0 |
s –подуровень s –АО |
x |
|
|
y |
l=1 |
p-подуровень р-АО |
х |
|
|
y |
Каждому n соответствует определенное число значений l, т.е. каждый энергетический уровень расщепляется на подуровни. Число подуровней равно номеру уровня.
1-ый энерг.уровень → 1 подуровень → 1s 2-ой энерг.уровень → 2 подуровня → 2s2p 3-ий энерг.уровень → 3 подуровня → 3s3p3d
4-ый энерг.уровень → 4 подуровня → 4s4p4d4f и т.д.
3.Магнитное квантовое число (ml)
определяет – значение проекции орбитального момента количества движения электрона на произвольно выделенную ось
показывает – пространственную ориентацию АО
принимает значения – от –l до + l
Любому значению l соответствует (2l+1) значений магнитного квантового числа, т.е. (2l+1) возможных расположений электронного облака данного типа в пространстве.
Любому значению l соответствует (2l+1) значений магнитного квантового числа, т.е. (2l+1) возможных расположений электронного облака данного типа в пространстве.
s-состояние – одна орбиталь (2 0+1=1) - 
 ml=0, т.к. l= 0
ml=0, т.к. l= 0
p-состояние – три орбитали (2 1+1=3)
ml: +1 0 -1, т.к. l=1
ml=+1 |
ml=0 |
ml = -1 |
Все орбитали, принадлежащие одному подуровню, имеют одинаковую энергию и называются вырожденными.
Вывод : АО характеризуется определенным набором n, l, ml, т.е. определенными размерами, формой и ориентацией в пространстве. 
4. Cпиновое квантовое число (ms)
«спин» - «веретено»
определяет - собственный механический момент электрона, связанный с вращением его вокруг своей оси
принимает значения – (-1/2· h/2 ) 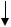 или (+1/2· h/2 )
или (+1/2· h/2 ) 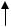
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Пример: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
n = 3 |
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
l = 1 |
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
3р |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ml = -1, 0, +1 |
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ms = + 1/2 |
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Принципы и правила
Принцип |
Правило |
минимальной |
Клечковского |
энергии |
|
Принцип |
Правило |
Паули |
Гунда |
Электронные конфигурации атомов
(в виде формул электронных конфигураций)
- указывают цифрами номер энергетического уровня
- указывают буквами энергетический подуровень (s, p, d, f);
- показатель степени подуровня означает число
электронов на данном подуровне
19К 1s22s22p63s23p64s1
Принцип
минимальной
энергии
Электроны в атоме занимают наиболее низкое энергетическое состояние, отвечающее наиболее устойчивому его состоянию.
1s 2s 2p 3s 3p 3d 4s 4p 4d 4f
Увеличение Е
Правило
Клечковского
(1958 г.)
Электроны размещаются последовательно на орбиталях, характеризуемых возрастанием суммы главного и орбитального квантовых чисел (n+l); при одинаковых значениях этой суммы раньше заполняется орбиталь с меньшим значением главного квантового числа n
1s <2s < 2p = 3s < 3p = 4s < 3d = 4p и т. д
|
|
|
1s |
2s |
2p |
3s |
3p |
3d |
4s |
4p |
|
n+l |
|
1+0=1 |
2+0=2 |
2+1=3 |
3+0=3 |
3+1=4 |
3+2=5 |
4+0=4 |
4+1=5 |
|
|
|
1 |
2 |
3 |
4 |
5 |
7 |
6 |
8 |
