
- •Лекция 6. Диаграммы состояния металлических систем
- ••Температуры, соответствующие фазовым превращениям, называются критическими точками
- •Виды диаграмм состояния сплавов
- •диаграммы состояния сплавов, образующих неограниченные твердые растворы
- •Правило отрезков • Линии mn называются коноды
- •диаграммы состояния сплавов, образующих механические смеси чистых компонентов
- •диаграммы состояния сплавов с ограниченной растворимостью в твердом состоянии
- •диаграммы состояния сплавов, образующих перитектику
- •диаграммы состояния сплавов, образующих химические соединения
- •Зависимость между свойствами сплавов и их диаграммами состояния
- •1.При образовании механических смесей свойства изменяются по линейному закону. Значения характеристик свойств сплава
- •Лекция 7. Диаграмма состояния железо –
- •Компоненты и фазы железоуглеродистых сплавов
- •2.Углерод
- •фазы в системе «железо – углерод»
- •Процессы при структурообразовании железоуглеродистых сплавов
- ••Линия AHJECF – линия солидус.
- ••На участке JЕ заканчивается кристаллизация аустенита.
- ••По линии HN начинается превращение феррита (δ) в аустенит, обусловленное полиморфным превращением железа.
- ••По линии PSK при постоянной температуре 727o С идет эвтектоидное превращение:
- •Структуры железоуглеродистых сплавов
- •Микроструктуры технического железа:
- •Микроструктуры сталей:
- •Микроструктуры белых чугунов:
Лекция 6. Диаграммы состояния металлических систем
•Это графическое изображение состояния сплава в зависимости от его концентрации и температуры.
•Диаграмма показывает равновесные (устойчивые состояния) сплава
жидкая фаза
Ж + α
Твердый раствор
•Температуры, соответствующие фазовым превращениям, называются критическими точками
•Температуры кристаллизации – точки ликвидуса
•Температуры конца кристаллизации – точки солидуса
Правило фаз (закон Гиббса) С=К-Ф+1
С - число степеней свободы (вариантность) - число факторов, которые можно менять, не изменяя фазового состава сплава
К- число компонентов
Ф- число фаз, находящихся в равновесии 1 – возможность изменения температуры
Если С=0, внешние факторы менять нельзя без изменения числа фаз в системе
Если С=1, возможно изменение одного фактора без изменения числа фаз в системе
Виды диаграмм состояния сплавов
1.Отсутствие растворимости (механические смеси чистых компонентов)
2.Полная растворимость (неограниченные твердые растворы)
3.Ограниченные растворы в твердом состоянии
•с образованием эвтектики
•с образованием перитектики 4. Химические соединения
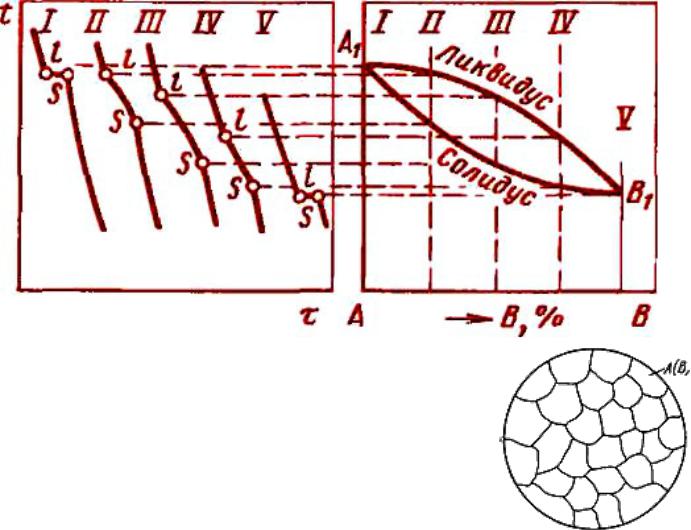
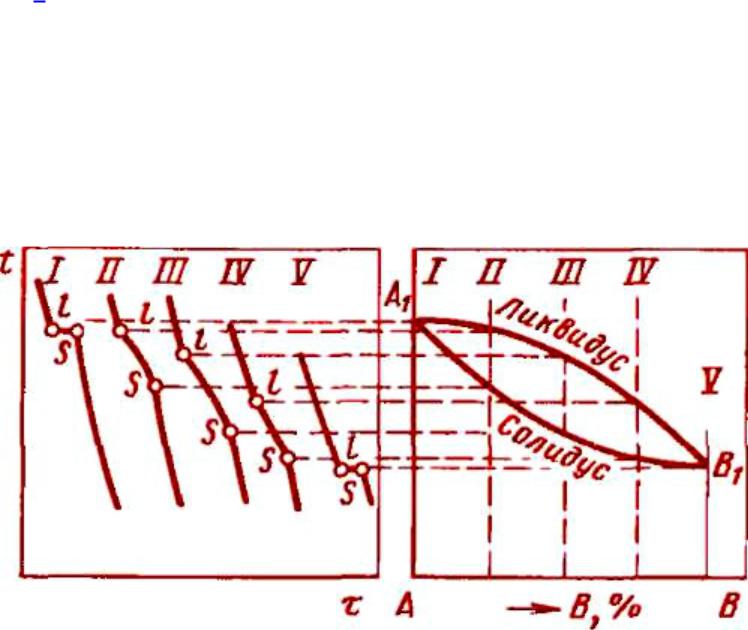
диаграммы состояния сплавов, образующих неограниченные твердые растворы
• |
Точки I и V |
С=1-2+1=0 |
• |
Точки II, III, IV |
С=2-2+1=1 |
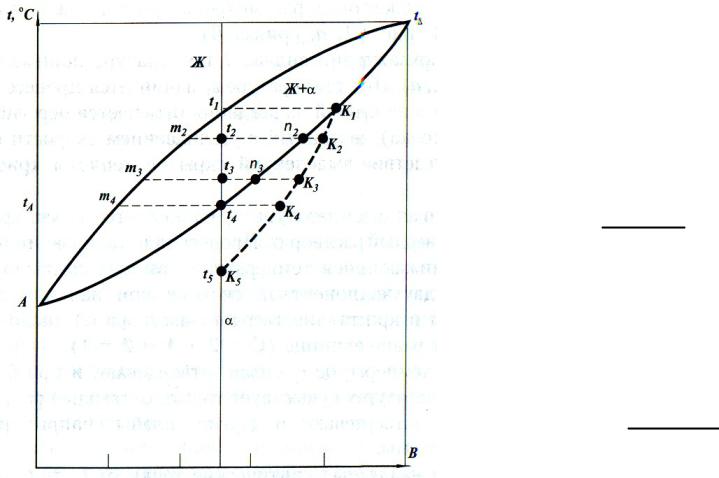
Правило отрезков • Линии mn называются коноды
• Количество твердой фазы (%) при температуре t2
t2m2 100% m2n2
Количество жидкой фазы
Ж t2n2 100% m2n2
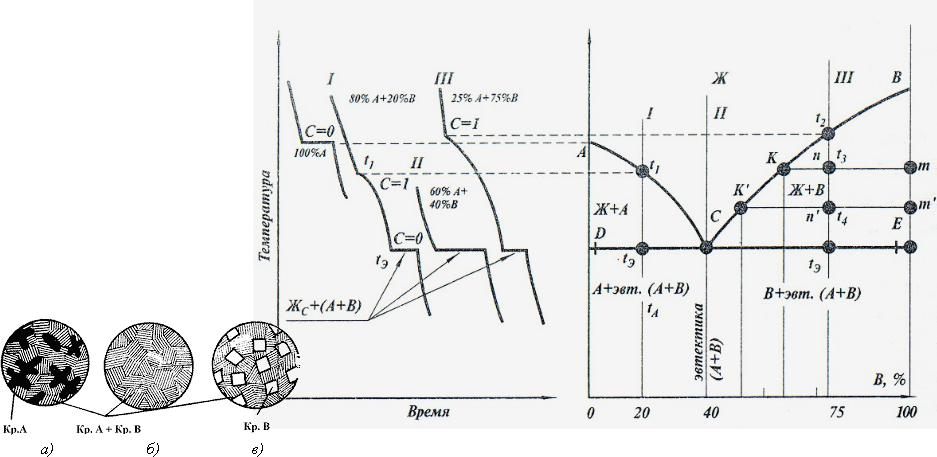
диаграммы состояния сплавов, образующих механические смеси чистых компонентов
(отсутствие растворимости в твердом состоянии)
К=2
Ф=3 Сс =2-3+1=0
Жс=А+В Ск =2-2+1=1
Механическая смесь двух или более разнородных кристаллов,
одновременно кристаллизующихся из жидкости при самой низкой Т, называется эвтектикой

диаграммы состояния сплавов с ограниченной растворимостью в твердом состоянии
с– эвтектика – механическая смесь фаз, кристаллизующихся одновременно при одной температуре из жидкого сплава
Вторичная
кристаллизация – процесс выделения новых кристаллов из кристаллов твердого раствора
К=2 Ф=3 (Ж,  ,
,  )
)
Кристаллы в чистом виде ни в одном из сплавов не присутствуют
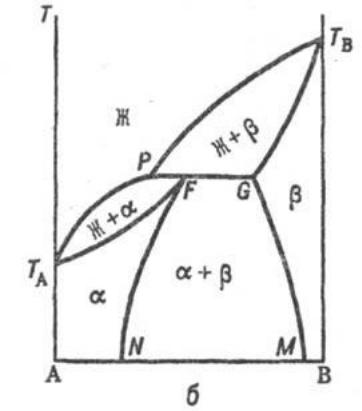
диаграммы состояния сплавов, образующих перитектику
•Перитектика (греч.) – окружение. Линия PFG
•В этой системе компоненты в жидком состоянии обладают полной растворимостью, а твердом растворимы частично.
•Выпавшие из жидкости кристаллы одного твердого раствора, реагируя с оставшейся жидкостью, образуют кристаллы другого твердого раствора, которые окружают первые
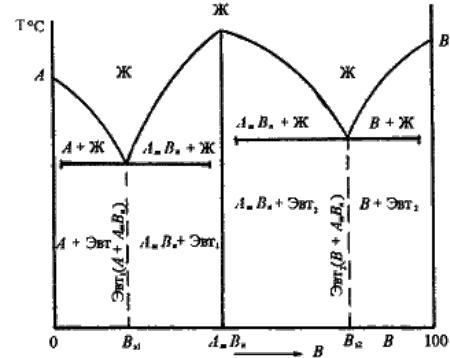
диаграммы состояния сплавов, образующих химические соединения
•Диаграмма состояния сложная, состоит из нескольких простых диаграмм. Число компонентов и количество диаграмм зависит от того, сколько химических соединений образуют основные компоненты системы.
•Число фаз и вид простых диаграмм определяются характером взаимодействия между компонентами.
•Эвт1 (кр. А + кр. AmBn);
•Эвт2 (кр. B + кр. AmBn).
