
коля / u_course
.pdf
(по прочности и пластичности: σв = 250–320 МПа; δ = 2-3 %) и ЛБС-1 (по технологическим характеристикам). Деформированные сплавы (ВБД) отличаются от литейных большей прочностью, жесткостью и пластично-
стью: σв = 350–370 МПа; δ = 2,5–6,0 %.
Особую группу (табл. 7.1) составляют высокомодульные сплавы систем Al–Be–Mg (типа АБМ) и Al–Be–Mg–Zn (типа АБМЦ).
Таблица 7.1
Химический состав и механические свойства высокомодульных сплавов
Сплав |
Химический состав*, % |
Механические свойства |
|||||
Be |
Mg |
Другие |
Е, ГПа |
σв, МПа |
δ, % |
||
|
|||||||
АМБ-1 |
28–32 |
4,2–5,5 |
– |
135 |
430–500 |
11–20 |
|
АМБ-2 |
18–22 |
7,0–8,0 |
– |
115 |
420–520 |
15–29 |
|
АМБ-3 |
67–72 |
1,5–2,5 |
– |
210 |
550–620 |
7–12 |
|
АМБ-4 |
43–47 |
2,8–4,0 |
(0,01–0,04) Ti |
170 |
520–590 |
9–15 |
|
АБМЦ |
18–22 |
4,8–5,2 |
(l,8–2,2)Zn |
115 |
570–670 |
7–10 |
|
*Остальное – алюминий.
Модуль упругости сплавов этой группы тем выше, чем больше в них бериллия. Все сплавы этой группы обладают значительной пластичностью. Они отличаются от других промышленных легких сплавов более высоким сопротивлением усталости, уникальной акустической выносливостью, меньшей скоростью роста усталостных трещин, повышенной вязкостью разрушения.
7.3.Применение бериллия
В50-е и начале 60-х гг. XX в. бериллий называли удивительным металлом и полагали, что он станет важнейшим конструкционным и ядерным материалом в авиации и атомной энергетике. Однако технологические трудности производства качественных полуфабрикатов, природные недостатки бериллия и его малая распространенность в земной коре привели к утрате иллюзий относительно возможностей его практического использования. Тем не менее и в настоящее время бериллий применяют в тех случаях, когда это оправдано в техническом и экономическом отношении.
250
Бериллий по своим физическим свойствам является весьма перспективным материалом в атомных реакторах для изготовления замедлителей и отражателей. Замедлители должны эффективно уменьшать скорость нейтронов и в то же время не поглощать их, так как в противном случае может прекратиться цепная реакция. По своим свойствам бериллий является наилучшим из всех металлов замедлителем. Отражатели способствуют более равномерному распределению нейтронов и тем самым уменьшают критическую массу реактора и увеличивают его мощность. Бериллий – один из лучших материалов для производства отражателей. Из бериллия изготавливают окна рентгеновских трубок, поскольку он слабо поглощает рентгеновские лучи. Его применяют в некоторых акустических приборах в качестве источника нейтронов.
Бериллий – также ценный конструкционный материал для авиации
иракетной техники. По удельной кратковременной прочности бериллий
превосходит все конструкционные материалы в интервале температур 430–650 оС. Опубликованы данные об успешном использовании бериллия для изготовления обтекателей сверхзвуковых самолетов, тяг управления, тормозных самолетных дисков, носовых конусов и оболочек ракет.
Из-за высокого модуля упругости амплитуда вибраций изделий из бериллия невелика. Поэтому опасность усталостного разрушения из-за подобных вибраций для бериллия меньше, чем для других металлов. Это свойство бериллия имеет большое значение для сверхзвуковых самолетов
иуправляемых снарядов. Высокая теплоемкость и теплопроводность в сочетании с большой теплотой плавления позволяют эффективно применять бериллий в качестве теплозащитных экранов космических аппаратов при вхождении их в плотные слои атмосферы.
Благодаря сочетанию высокой прочности с малым удельным весом бериллий является перспективным материалом для изготовления быстровращающихся деталей. В них из-за малой плотности возникают меньшие центробежные силы. Меньшая инерционность позволяет поддерживать или изменять вращение путем меньшей затраты энергии. По этой причине бериллий применяют в производстве инерциальных систем наведения.
Бериллиевые изделия, полученные из тонкого порошка, обладают большой стабильностью размеров во времени и поэтому являются незаменимым материалом в точном приборостроении. Из бериллия изготавливают детали гироскопов в системах ориентации и стабилизации ракет, космических кораблей и искусственных спутников Земли.
Бериллий применяют также в конструкции подводных лодок и торпед, что позволяет увеличить глубину их погружения при одинаковом внутреннем объеме [1, 5].
251
Контрольные вопросы
изадания
1.Каковы физико-химические свойства бериллия?
2.Охарактеризуйте основные недостатки бериллия.
3.Каковы механические свойства бериллия?
4.Почему создание сплавов на основе бериллия является сложной проблемой?
5.Перечислите элементы, которые имеют заметную растворимость в твердом бериллии.
6.Охарактеризуйте состав, структуру и свойства сплавов бериллия с алюминием.
7.Опишите химический состав и механические свойства высокомодульных сплавов систем Al–Be–Mg и Al–Be–Mg–Zr.
8.Перечислите области применения бериллия и его сплавов.
8. НИКЕЛЬ И ЕГО СПЛАВЫ
Никель открыл в 1751 г. шведский химик А. Кронштедт. В земной коре содержится 0,008 % (мас.) никеля [5].
8.1. Свойства никеля
Атомный номер никеля – 28. Температура плавления равна 1455 оС, а кипения 2823 оС. Никель имеет ГЦК решетку. Плотность никеля при 20 оС – 8,9 г/см3, поэтому никель относят к числу тяжелых цветных металлов. Удельная теплопроводность при 20 оС составляет 88,5 Вт/(с·К). Удельное электросопротивление при 20 оС – 0,0684 мкОм·м. Модуль нормальной упругости равен 203 ГПа. Никель относят к переходным металлам.
В зависимости от чистоты различают следующие марки никеля: НО, Н1У, HI, Н2, НЗ, Н4. Никель марки НО содержит не менее 99,9 % (Ni + Co), в том числе менее 0,005 % Co, а никель марки Н4 – не менее 97,6 % (Ni + Co), в
252
том числе менее 0,7 % Co. Содержание большинства примесей в никеле не превышает сотых и тысячных долей процента, лишь в марке Н4 допускается до 1 % Си и до 0,65 % С. Наиболее вредные примеси в никеле и его сплавах – Bi, Pb, Sb, As, P и Cd.
Висмут и свинец вызывают красноломкость никеля, т.к. они нерастворимы в нем и при сравнительно низких температурах приводят к появлению жидкой фазы. Допустимое содержание этих примесей в жаропрочных никелевых сплавах составляет, %: 0,0001 Bi; по 0,001 As, Pb, Sb, Sn; 0,007 S; 0,015 P. Сурьма и мышьяк ухудшают обрабатываемость давлением никеля и его сплавов. Фосфор и кадмий резко снижают механические, физические и технологические свойства никеля.
Никель отличается высокой коррозионной стойкостью, и его применяют как коррозестойкий материал в виде листов, лент, прутков, труб и проволоки. Полуфабрикатный никель маркируют буквами НП и цифрой, дающей характеристику металла: НП1 – никель полуфабрикатный, полученный электровакуумной плавкой, содержание (Ni + Со) не менее 99,9 %; НП2, НПЗ и НП4 – никель полуфабрикатный, содержащий не менее 99,5; 99,3 и 99,0 % (Ni + Co) соответственно; НПАН – никель полуфабрикатный, анодный непассивирующийся, (Ni + Со) ≥ 99,4 %; НПА1 и НПА2 – никель полуфабрикатный, анодный с содержанием не менее 99,7 и 99,0 % (Ni + Со) соответственно.
Чистейший никель имеет следующие механические свойства: σв = 280–300 МПа; δ = 40–50 %, а полуфабрикатный отожженный никель НП4
σв = 400–500 МПа; σ0,2 = 220 МПа; δ = 35–40 %; ψ = 70 %; KCU = 1,8 МДж/м2.
Нагартовкой можно повысить временное сопротивление разрыву никеля до 750–900 МПа; относительное удлинение при этом падает до 4–2 %. Температура начала рекристаллизации нагартованного никеля НЗ составляет около 525 оС; температура полного рекристаллизационного отжига – 700–800 оС; низкотемпературного (для уменьшения остаточных напряжений) 300 оС
Никель – ферромагнитный металл, но его ферромагнетизм выражен менее сильно, чем у железа и кобальта. Точка Кюри для никеля составляет 358 оС, вышеэтойтемпературыникельпереходитвпарамагнитноесостояние.
Чистый никель – металл серебристого цвета. При высокотемпературном окислении никеля образуются два оксидных слоя: внутренний – светло-зеленый и внешний – темно-зеленый. Оба этих слоя состоят из оксида NiO, но отличаются количеством кислорода.
Никель имеет более высокую коррозионную стойкость в атмосферных условиях по сравнению с другими техническими металлами, что обусловлено образованием на его поверхности тонкой и прочной защитной пленки. Никель обладает достаточной устойчивостью не только в пресной, но и в морской воде. Минеральные кислоты, особенно азотная, сильно действуют на никель. Щелочные и нейтральные растворы солей на никель
253
влияют незначительно даже при нагревании, в кислых растворах солей он корродирует довольно сильно. В концентрированных растворах щелочей никель устойчив даже при высоких температурах.
Никель при комнатной температуре не взаимодействует с сухими газами (галогенами, оксидами азота, сернистым газом, аммиаком), но присутствие влаги заметно повышает скорость его коррозии в этих средах. Никель, загрязненный кислородом, склонен к водородной болезни [1].
8.2. Взаимодействие никеля с легирующими элементами и примесями
Никель образует непрерывные твердые растворы с ближайшими к нему в первом длинном периоде соседями: медью, кобальтом, железом и марганцем. При высоких температурах в никеле в больших концентрациях (до 35–40 %) растворяются многие тугоплавкие металлы (Сr, V, Мо, Та, W); значительной максимальной растворимостью в никеле (от 2,5 до 20 %) обладают алюминий, титан, ниобий, бериллий и кремний. С понижением температуры растворимость легирующих элементов, образующих с никелем ограниченные растворы, уменьшается, что создает предпосылки дисперсионного упрочнения. Твердые растворы на основе никеля часто называют аустенитом по аналогии с твердыми растворами на основе γ-железа с ГЦК-структурой.
Вбольшинстве практически важных систем со стороны никеля наблюдается эвтектическое равновесие, так что температура плавления никеля понижается; из перечисленных лишь два элемента несколько повышают температуру плавления никеля: кобальт и вольфрам.
Из двойных систем на основе никеля наибольший интерес представ-
ляют Ni–Cr, Ni–Al и Ni–Ti.
Всистеме Ni–Cr (рис. 8.1), относящейся к эвтектическому типу, образуются довольно обширные твердые растворы как на основе никеля, так
ихрома. С понижением температуры области ограниченных растворов уменьшаются, но даже при комнатной температуре растворимость хрома в никеле сохраняется довольно большой (~30 % Сr).
Всистеме Ni–Al со стороны никеля наблюдается эвтектическое рав-
новесие (рис. 8.2). Растворимость алюминия в никеле уменьшается с 11 % при эвтектической температуре (1385 оС) до примерно 6 % А1 при темпе-
254
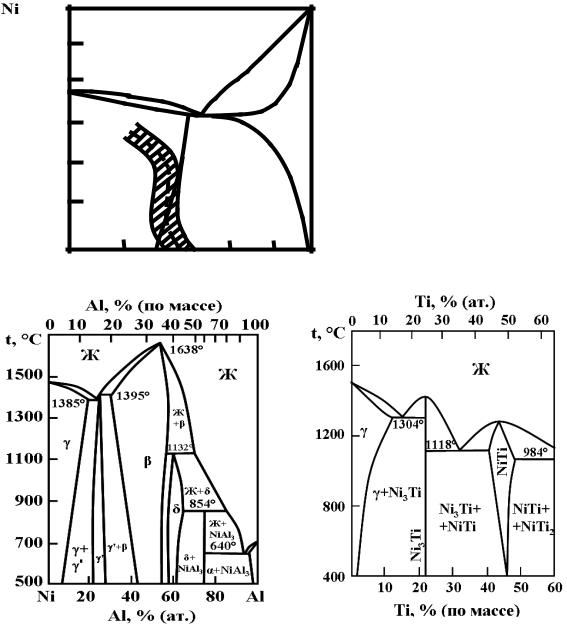
ратуре 750 оС. В этой системе в равновесии с γ-твердым раствором на основе никеля находится γ'-фаза, представляющая раствор на основе интерметаллида Ni3Al с ГЦК-решеткой.
t, oC |
|
|
|
|
|
1700 |
|
Ж |
|
|
|
|
|
|
|
|
|
1500 |
|
|
|
|
|
1300 |
|
|
|
α |
|
1100 |
|
|
|
|
|
900 |
γ |
|
α + γ |
|
Рис. 8.1. Диаграмма состояния систе- |
|
|
|
|
|
мы Ni–Cr (И.И. Корнилов). Заштри- |
700 |
|
|
|
|
хована область сплавов с максималь- |
|
|
|
|
ным сопротивлением ползучести при |
|
|
|
|
|
|
|
Ni |
20 |
40 |
60 |
80 Cr |
разных температурах |
|
|
% (по массе) |
|
|
|
|
|
|
Рис. 8.2. Диаграмма состояния |
Рис. 8.3. Диаграмма состояния |
|
системы Ni–Al |
|
системы Ni–Ti |
В системе Ni–Ti (рис. 8.3) при температуре 1304 оС также происходит эвтектическое превращение. Растворимость титана в никеле уменьшается с 11,6 % Ti при эвтектической температуре до 8 % Ti (по массе) при температуре 750 оС. В равновесии с γ-раствором находится η-фаза – твердый раствор на основе интерметаллида Ni3Ti с гексагональной решеткой.
255
При дополнительном легировании сплавов системы Ti–Al–Ni хромом в концентрациях до 20 % характер фазовых равновесий, свойственных тройной системе, не меняется, но совместная растворимость алюминия и титана уменьшается.
Помимо хрома, алюминия и титана жаропрочные сплавы на никелевой основе могут содержать еще 9-10 легирующих элементов, которые по характеру взаимодействия с никелем можно разбить на три группы.
Первая группа состоит из элементов, входящих в γ-твердый раствор (их называют γ-стабилизирующими элементами): к этим элементам относят металлы V–VIIIA подгрупп периодической системы (V, Nb, Cr, Mo, W, Re, Fe, Co). Вторую группу составляют элементы, способствующие образованию γ'-фазы (γ'-образующие элементы): в нее входят элементы III–VA подгрупп (Al, Ti, Nb, Та). Вместе с тем алюминий и титан в определенной степени растворяются и в γ-фазе. Тантал и ниобий, как и титан, могут замещать алюминий в соединении Ni3Al. Третья группа представлена элементами, сегрегирующими на границах зерен; это элементы подгрупп IIA, IIIA, IVB, сильно отличающиеся от никеля по размерам атомов, а именно, магний, бор, углерод, цирконий, церий.
Кроме того, в никелевых сплавах различают карбидообразуюшие
элементы (Ti, Zr, Hf, V, Nb, Та, Cr, Mo, W) и элементы, образующие стой-
кие оксиды (Al, Сr), защищающие металл от воздействия окружающей среды. Карбидообразующие элементы образуют карбиды типа МеС, Ме6С, Me23C6 и др. В структуре жаропрочных никелевых сплавов встречаются также карбонитриды, бориды типа Ме3В2 и некоторые другие соединения. Никель не образует устойчивых карбидов. Растворимость углерода в никеле составляет 0,65 % при температуре эвтектики (1318 оС) и резко уменьшается с понижением температуры.
В никеле встречается довольно много примесей, которые можно разбить на две группы: а) растворимые в никеле (Al, Mn, Fe, Cu, Zr, Sn, Si, Sb, As); б) практически нерастворимые в твердом никеле (S, O, P, Bi, Pb, Mg, Cd).
8.3. Никелевые сплавы
Промышленные сплавы на основе никеля можно разделить на следующие группы: а) жаростойкие; б) жаропрочные; в) конструкционные; г) электротехнические; д) сособымифизическими ихимическими свойствами.
Жаропрочные сплавы разбивают на три подгруппы: деформируемые; литейные; дисперсно-упрочненные.
256
|
|
|
|
|
|
|
|
|
|
Таблица 8.1 |
|
Химический состав, %, жаропрочных деформируемых сплавов |
|
|
|||||||
|
|
|
на никелевой основе |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
Условное |
Марка |
С, не бо- |
|
|
|
|
|
|
|
Другие |
обозначе- |
Cr |
Co |
Ti |
Al |
W |
|
Mo |
|||
по ГОСТу |
лее |
|
элементы* |
|||||||
ние |
|
|
|
|
|
|
|
|
|
|
ЭИ437А |
ХН77ТЮ |
0,06 |
19–22 |
– |
2,3–2,7 |
0,55–0,95 |
– |
|
– |
– |
ЭИ437Б |
ХН77ТЮР |
0,07 |
19–22 |
– |
2,4–2,8 |
0,60–1,00 |
– |
|
– |
– |
ЭИ437БУ |
ХН77ТЮР |
0,04–0,08 |
19–22 |
– |
2,65–2,9 |
0,70–1,00 |
– |
|
– |
– |
ЭИ617 |
ХН70ВМТЮ |
0,08 |
13–16 |
– |
1,8–2,3 |
1,7–2,3 |
5–7 |
|
2–4 |
(0,1–0,5) V |
ЭИ826 |
ХН70ВМФТЮ |
0,08 |
13–16 |
– |
1,7–2,2 |
2,4–2,9 |
5–7 |
|
2,5–4,0 |
0,3 V |
ЭИ929 |
ХН55ВМТФКЮ |
0,08 |
9–12 |
12–16 |
1,4–2,0 |
3,6–4,5 |
4,5–6,5 |
|
4–6 |
(0,2–0,8) V |
ЭИ698 |
ХН73МБТЮ |
0,03–0,07 |
13–16 |
– |
2,35–2,75 |
1,45–1,80 |
– |
|
2,8–3,2 |
(1,8–2,2) Nb |
ЭИ867 |
ХН62МВКЮ |
0,08 |
8,5–10,5 |
4–6 |
– |
4,2–4,9 |
4,3–6,0 |
|
9–11,5 |
– |
ЭП109 |
ХН56ВМКЮ |
0,08 |
8,5–10,5 |
11–13 |
– |
5,4–6,2 |
6,5–7,5 |
|
6,5–7,5 |
– |
ЭП741НП |
ХН57ВБМКТЮ |
0,02–0,06 |
8–10 |
15–16,5 |
1,6–2,0 |
4,85–5,25 |
4,8–5,9 |
|
3,5–4,2 |
(2,4–2,8) Nb |
ЭП742 |
ХН62БМКТЮ |
0,04–0,08 |
13–15 |
9–11 |
2,4–2,8 |
2,4–2,8 |
– |
|
4,5–5,5 |
2,6 Nb |
ЭК79 |
ХН53КМБВТЮ |
0,04–0,08 |
10–12 |
12,5–16,0 |
2,4–3,0 |
2,8–3,3 |
2,0–3,0 |
|
4,0–5,0 |
0,6 V |
ЭП109 |
ХН58КВМЮ |
≤0,08 |
10 |
12 |
– |
6 |
7 |
|
7 |
– |
ЭП220 |
ХН54КМВТЮ |
≤0,08 |
10,5 |
15 |
2,5 |
4,5 |
6 |
|
7 |
0,5 V |
*Все сплавы, кроме ЭИ437А, содержат микродобавки бора (~0,005–0,02 %) или церия (≤ 0,005–0,025 %), или того и другого элемента одновременно.
Жаропрочные сплавы представляют наиболее важную группу сплавов на основе никеля. Химический состав жаропрочных деформируемых и литейных сплавов дан в табл. 8.1, 8.2.
Таблица 8.2
Типичный химический состав*, %, основных литейных жаропрочных никелевых сплавов
Сплав |
C |
Cr |
Co |
Mo |
W |
Ta |
Nb |
Al |
Ti |
|
Zr |
B |
Другие |
|
элементы |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Сплавы для равноосного литья |
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ЖС6К |
0,16 |
11,3 |
4,5 |
4,0 |
5,0 |
– |
– |
5,5 |
2,85 |
|
0,04 |
0,02 |
– |
ЖС6У |
0,17 |
8,8 |
9,8 |
1,8 |
10,3 |
– |
1,0 |
5,6 |
2,4 |
|
0,04 |
0,035 |
– |
ВЖЛ12У |
0,17 |
9,5 |
14,0 |
3,1 |
1,4 |
– |
0,8 |
5,3 |
4,5 |
|
0,02 |
0,035 |
0,7 V |
|
|
|
Сплавы для направленной кристаллизации |
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ЖС6Ф |
0,15 |
5,5 |
9,5 |
1,0 |
12,0 |
– |
1,6 |
5,5 |
1,1 |
|
0,08 |
0,015 |
1,2 Hf; 1,0 V |
ЖС26 |
0,13 |
4,4 |
8,5 |
1,1 |
11,9 |
– |
1,7 |
5,9 |
0,9 |
|
0,05 |
0,015 |
0,9 V |
ЖС30 |
0,16 |
7,0 |
8,5 |
0,7 |
11,8 |
– |
0,9 |
5,3 |
1,9 |
|
– |
0,015 |
0,8 Hf |
ЖС32 |
0,15 |
4,9 |
9,0 |
1,0 |
8,5 |
4,0 |
1,6 |
5,9 |
– |
|
– |
0,015 |
4,0 Re |
|
|
|
Сплавы для монокристального литья |
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ЖС30М |
– |
7,0 |
7,5 |
0,6 |
11,7 |
– |
1,1 |
5,1 |
1,8 |
|
– |
– |
0,1 Hf |
ЖС36 |
– |
4,0 |
7,0 |
1,6 |
11,7 |
– |
1,1 |
5,8 |
1,1 |
|
– |
– |
2,0 Re |
ЖС40 |
– |
6,3 |
0,5 |
4,2 |
7,0 |
7,0 |
0,2 |
5,3 |
– |
|
– |
– |
– |
ЖС32М |
0,05 |
4,5 |
8,5 |
1,3 |
5,0 |
4,5 |
– |
5,5 |
– |
|
– |
– |
5,5 Re |
|
|
|
Сплавы на основе алюминида Ni3Al |
|
|
|
|||||||
ВКНА-1В |
0,04 |
5,5 |
– |
3,5 |
3,5 |
– |
– |
8,5 |
1,5 |
|
– |
– |
– |
ВКНА-4У |
0,02 |
5,0 |
4,0 |
5,0 |
2,0 |
– |
– |
8,5 |
0,9 |
|
– |
– |
– |
*Остальное – никель.
Никелевые сплавы маркируют условными обозначениями, не имеющими никакого отношения к их химическому составу (например, ЭИ437Б, ЭП742), или применяют систему обозначений, сходную с принятой для сталей. В последнем случае марка сплава состоит из букв, обозначающих элементы, входящие в состав сплава: Н – никель; X – хром; Т – титан; Ю – алюминий; Р – бор; В – вольфрам; М – молибден; Б – ниобий; К
– кобальт. Обозначение сплава начинается с буквы X, затем идет Н и число, отражающее среднее содержание никеля, а далее буквы, обозначающие остальные легирующие элементы в порядке уменьшения их содержания.
Жаростойкость – способность сопротивляться газовой коррозии при высоких температурах.
257
Жаропрочность – способность металлического материала сопротивляться деформации и разрушению при кратковременном или длительном воздействии нагрузок при повышенных температурах.
Жаростойкие никелевые сплавы
Никель отличается лучшей жаростойкостью по сравнению с медью и железом, т.к. оксид NiO обладает лучшими защитными свойствами по сравнению с оксидами меди и железа. Это обусловлено, во-первых, значительно меньшей концентрацией вакансий в оксиде NiO по сравнению со многими другими оксидами, так что диффузионный рост оксидной пленки на никеле происходит медленно; во-вторых, хорошим сцеплением оксида с металлом, и, в-третьих, близким коэффициентом линейного расширения оксида NiO и никеля, в связи с чем теплосмены не вызывают отслаивания оксидного слоя от металла.
Основой многих жаростойких никелевых сплавов является система Ni–Cr (см. рис. 8.1) поскольку легирование никеля хромом приводит к сильному повышению стойкости против окисления при высоких температурах. Критическое минимальное количество хрома, необходимое для существенного повышения жаростойкости никеля и никелевых сплавов, составляет 20–25 %, максимальная жаростойкость в сплавах системы Ni–Сr отмечается при 40 % хрома.
Высокая жаростойкость сплавов никеля с хромом обусловлена образованием под тонким внешним слоем оксида NiO второго оксидного слоя Сr2О3, отличающегося малой скоростью роста, а также промежуточного слоя шпинели NiCr2O4.
Сплавы никеля с хромом получили название нихромов, к ним относятся сплавы Х10Н90, Х20Н80, Х30Н70, Х40Н60, Х50Н50. Структура первых двух сплавов однофазна и представлена γ-твердым раствором (см. рис. 8.1); последние два сплава двухфазны (γ + α). Жаростойкие никелехромовые сплавы дополнительно легируют железом и вольфрамом, входящими в γ-твердый раствор, а также кремнием, алюминием, титаном, церием и барием, образующими избыточные фазы или сегрегирующими на границах зерен. Алюминий и кремний в эти сплавы вводятся не для повышения механических свойств, а, главным образом, для улучшения окалиностойкости. Микродобавки церия и бария весьма эффективно «залечивают» вакантные места в кристаллической решетке оксидов и в связи с этим затрудняют рост оксидной пленки.
Жаростойкие никелевые сплавы не отличаются высокой прочностью и жаропрочностью. При комнатной температуре их временное сопро-
258
