- •Генерация и распространение электромагнитных волн в космосе
- •Общая классификация механизмов излучения
- •Излучение с непрерывным спектром и спектральные линии
- •Тепловое и нетепловое излучение
- •Когерентные и некогерентные механизмы излучения
- •Сужение диаграммы
- •«Сверхсветовые» скорости
- •Плотность потока от движущегося источника
- •Собственное излучение астрофизической плазмы
- •Тормозное излучение
- •Тормозное излучение
- •Тормозной механизм излучения в астрофизике
- •Черенковское излучение
- •Магнитотормозное излучение
- •Частотный спектр циклотронного излучения электрона в пустоте
- •Роль циклотронного излучения в астрофизике
- •Расположение гирорезонансных слоев в активной области на Солнце
- •Циклотронная линия в спектре рентгеновского пульсара Her X-1.
- •Синхротронное излучение
- •Synchrotron Radiation
- •При выводе выражения для Δt учитывалось, что
- •Спектр синхротронного излучения состоит из гармоник частоты ΩH/sin2α. Максимум приходится на частоту
- •Поляризация синхротронного излучения
- •Влияние среды на характер синхротронного излучения
- •Потери энергии при синхротронном излучении
- •Синхротронное излучение ансамбля частиц
- •II. Степенной энергетический спектр
- •Самопоглощение синхротронного излучения
- •Интерпретация синхротронных спектров
- •Магнитодрейфовое (изгибное) излучение
- •Плазменный механизм генерации радиоизлучения
- •Рассеяние на свободных частицах. Обратный эффект Комптона
- •Потери энергии за счет обратного комптон-эффекта:
- •Роль обратного комптоновского рассеяния в астрофизике
- •Комбинационное рассеяние волн
- •Эффекты распространения волн в плазме
- •Эффект группового запаздывания сигналов
- •Эффект Фарадея
- •Эллипс поляризации повернется на угол:
- •«Мера вращения»
- •Излучение в спектральных линиях
- •Основы
- •Коэффициенты вероятности Эйнштейна
- •Соотношения между коэффициентами Эйнштейна
- •Коэффициент поглощения в линии
- •Населенность уровней
- •Уравнение баланса
- •«Критическая плотность»
- •Профиль линии: доплеровское уширение (профиль Гаусса)
- •Профиль линии: столкновительное уширение (профиль Лоренца)
- •Переходы между компонентами тонкой и сверхтонкой структуры атомов
- •Spectral Line emission: hyperfine transition of neutral Hydrogen
- •Why can we see 21cm line of neutral Hydrogen?
- •Переходы между
- •Линия нейтрального углерода на частоте 492 ГГц в туманности Ориона.
- •Рекомбинационные линии
- •Частоты переходов для водородоподобных атомов:
- •Spectral Line emission: molecular rotational and vibrational modes
- •Межзвездные молекулы: январь
- •Спектры молекул
- •Колебательно-вращательные спектры молекул
- •Вращательные спектры
- •Вращательные спектры
- •Структура энергетических уровней метил ацетилена (CH3CCH).
- •Вращательные спектры
- •Что дают наблюдения молекулярных линий?
- •Распределение молекулярного
- •Astrochemistry and chemical evolution in star forming regions
- •Космические мазеры
- •Признаки мазерного излучения
- •Ненасыщенный мазер
- •Насыщенный мазер
- •Накачка мазеров
- •Основные виды космических мазеров
- •Излучение пыли
- •abs a2Qabs
- •Величина и частотная зависимость коэффициента поглощения
- •Polarization of dust emission and magnetic fields in star forming regions
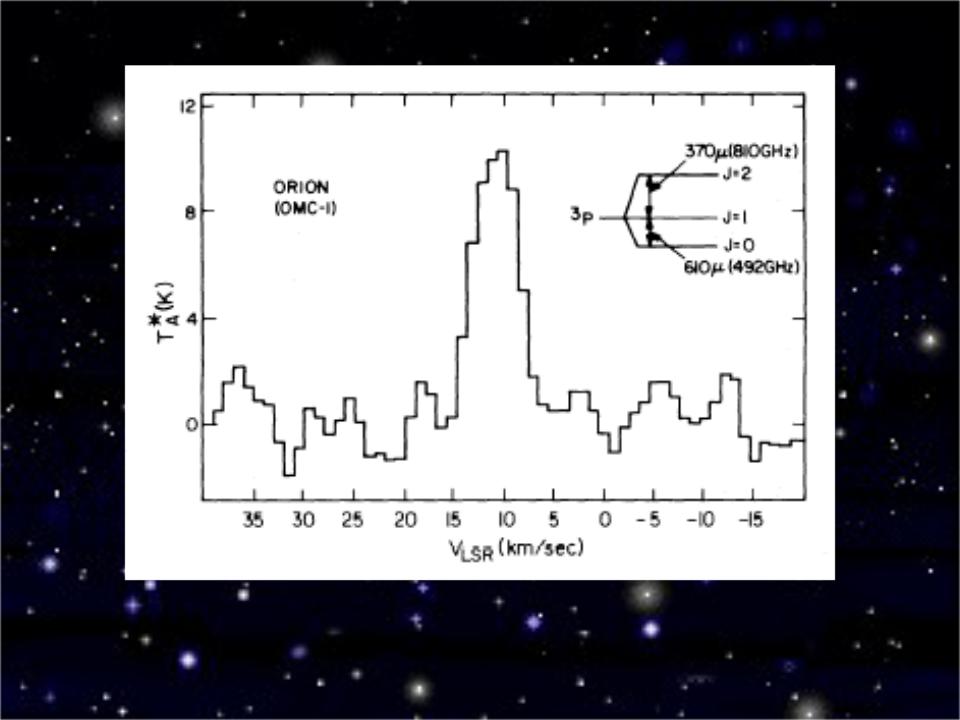
Линия нейтрального углерода на частоте 492 ГГц в туманности Ориона.

Рекомбинационные линии
В процессе рекомбинации возможен захват электрона на высоковозбужденные уровни атома. При последующих каскадных переходах испускаются кванты, частота которых попадает в радиодиапазон. Возникают рекомбинационные радиолинии.
Такие линии от областей ионизованного водорода, гелия и углерода наблюдаются в широком диапазоне частот и служат важным средством диагностики физических условий.

Частоты переходов для водородоподобных атомов:
|
|
|
|
1 |
|
|
1 |
|
|
|
|
m n |
|
|
|
Эффективный |
|
|||||||||||
|
|
2 |
|
|
|
|
2 |
|
|
|
заряд ядра (заряд |
|
||||||||||||||||
mn cRAZ |
|
|
|
|
|
|
|
|
|
|
2cRAZ |
|
|
|
3 |
|
|
|
|
|
|
|
|
|
||||
|
|
|
2 |
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
иона) |
|
|||||||||||||||
|
|
|
n |
|
|
|
|
m |
|
|
|
|
|
n |
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Атомная |
|
||||
|
|
|
|
|
m |
|
|
|
1 |
|
|
|
m |
|
|
|
|
|
|
постоянная |
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
RA R 1 |
|
|
|
e |
|
|
|
R 1 |
|
e |
|
|
|
|
|
|
Ридберга |
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Масса |
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
M A |
|
|
|
|
|
M A |
|
|
|
|
электрона |
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
2 2m e4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Масса атома |
|
|
||||||||
R |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
e |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Постоянная Ридберга |
|
|||||||||
ch3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
для бесконечной |
|
|||||||||
Приняты следующие обозначения |
|
|
|
массы |
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
рекомбинационных линий: наименование |
||||||||||||||||||||||||||||
элемента, номер уровня, на который происходит переход (n), порядок перехода (m-n), обозначаемый греческой буквой. Например, H114β
– переход с уровня 116 на уровень 114 водорода.
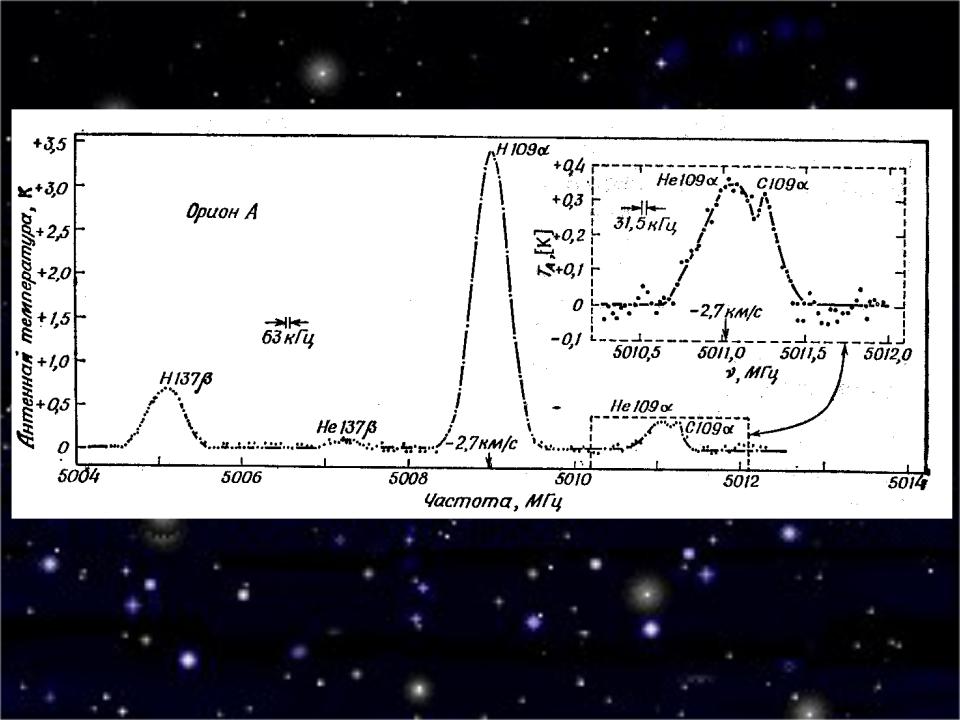

Spectral Line emission: molecular rotational and vibrational modes
•Commonly observed molecules in space:
Carbon Monoxide (CO)
Water (H2O), OH, HCN, HCO+, CS
Ammonia (NH3), Formaldehyde (H2CO)
•Less common molecules:
Sugar, Alcohol, Antifreeze (Ethylene Glycol), …
malondialdyde

Межзвездные молекулы: январь
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
3 |
|
4 |
5 |
6 |
|
20017 |
|
8 |
|
|
9 |
|
10 |
11 |
12 |
13 |
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
(number of atoms) |
|
|
||||
H2 |
NS |
H2O |
H3+ |
NH3 |
SiH4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HD |
HCl |
H2S |
H3O+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
NaCl |
N2H+ |
|
|
|
|
|
Possible detections (?) |
|
|
|
|
|
||||||
SO |
KCl |
SO2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NO |
AlCl |
HNO |
|
|
|
|
|
NH2CH2COOH (glycine) |
|
|
|
|
|||||||
SiO |
AlF |
SiH ? |
|
|
|
|
|
C + |
|
(ionized fullerene) |
|
|
|
|
|||||
|
|
2 |
|
|
|
|
|
60 |
|
|
|
|
|
|
|
|
|
|
|
SiS |
PN |
H2D+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
SiN |
NH |
NH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
SO+ |
HF |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH+ |
HCN |
H2CO |
HC3N |
CH3OH |
|
HC5N |
HCOOCH3 |
|
HC7N |
|
CH3C5N |
HC9N |
C6H6 |
HC11N |
|||||
CH |
HNC |
HNCO |
C4H |
CH3CN |
|
CH3CCH |
CH3COOH |
(CH3)2O |
(CH3)2CO |
|
|
|
|||||||
CC |
C2H |
H2CS |
H2CNH |
CH3NC |
|
CH3NH2 |
CH3C3N |
CH3CH2OH |
|
|
|
|
|
||||||
CN |
C2S |
HNCS |
H2C2O |
CH3SH |
|
CH3CHO |
C7H |
|
|
CH3CH2CN |
|
|
|
|
|
||||
CO |
SiC2ring |
C3N |
NH2CN |
NH2CHO |
H2CCHCN |
CH3COOH |
CH3C4H |
|
|
|
|
|
|||||||
CSi |
HCO |
C3Hlin |
HCOOH |
H2CCH2 |
|
C6H |
H2C6 |
|
|
|
C8H |
|
|
|
|
|
|||
CS |
HCO+ |
C3Hring |
CH4 |
C5H |
|
C2H4Ocy c |
HC6Hlin |
|
|
|
|
|
|
|
|||||
CP |
HOC+? |
C3O |
H2C3ring |
C5N |
|
C2H3O2? |
|
|
|
|
|
|
|
|
|
|
|
||
CO+ |
OCS |
C3S |
H2C3lin |
HC2CHO |
C7-? |
|
|
|
|
|
|
|
|
|
|
|
|||
SH |
|
HCS+ |
HOCO+ |
CH2CN |
H2C4lin |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CO2 |
HCCH |
C4Si |
HC3NH+ |
|
|
Evidence (by low res. IR) for: |
|
|
|
||||||||
|
|
C2O |
HCNH+ |
HCCNC |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
MgNC |
HCCN |
HNCCC |
|
|
|
- PAHs |
(Polycyclic aromatic hydrocarbons) |
|
|
||||||||
|
|
MgCN |
H2CN |
CCCCC |
|
|
|
- Dust: Silicate CORE + MANTLE (CO, CH4, H2O) |
|
||||||||||
|
|
CCC |
CH2D+ |
H2COH+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
CH3 |
|
|
|
|
|
|
|
|
|
CO |
|
|
|
|
|
|
|
|
NaCN |
SiCCC |
|
|
|
|
|
|
|
|
|
CH4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
N2O |
HNCS |
|
|
|
|
|
|
|
|
|
H2O |
|
|
|
|
|
|
|
|
SiCN |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|

Спектры молекул
 Колебательно-вращательные спектры
Колебательно-вращательные спектры
 Λ–удвоение
Λ–удвоение  Инверсионные спектры
Инверсионные спектры

Колебательно-вращательные спектры молекул
Энергию молекулы E можно представить в виде суммы энергии электронов, колебательной энергии и вращательной энергии:
E = Eel + Evib + Erot
Возможны колебательно-вращательные переходы (без изменения электронного состояния) и чисто вращательные переходы, когда меняется только Erot, а Eel и Evib остаются без изменения. Переходы между электронными состояниями лежат в видимой и УФ-области спектра, между колебательными – в ближней ИК-области, между вращательными
– в дальней ИК-области, в субмиллиметровом диапазоне и в радиодиапазоне.

Вращательные спектры
Для жестких двухатомных и линейных многоатомных молекул:
|
|
|
h2 |
|
|
|
Вращательное |
|
|||
|
|
|
J 1 hBJ (J 1) |
|
квантовое число |
|
|||||
Erot |
|
|
|
J |
|
|
|
||||
8 2 I |
|
|
|
||||||||
|
|
|
|
||||||||
|
|
|
|
|
|
|
Момент инерции |
|
|||
I |
r2 m m |
|
|
|
|
||||||
|
|
|
|
|
|||||||
|
|
|
|
|
|||||||
12 |
1 2 |
|
|
|
|
|
|
|
|||
m m |
|
|
|
|
|
||||||
|
|
|
|
|
|
||||||
1 |
2 |
|
|
|
|
|
Правила отбора |
|
|||
J 1 |
|
|
|
|
|||||||
|
|
|
|
|
|||||||
|
|
|
|
|
|||||||
J 1 J |
|
EJ 1 |
EJ |
2B(J 1) |
|
|
|
||||
|
Частоты |
|
|||||||||
|
|
|
|||||||||
|
|
|
|
|
|
h |
|
|
переходов |
|
|
|
|
|
|
|
|
|
|
|
|||