
Органическая химия / Каток_Органическая химия_ссылки
.pdf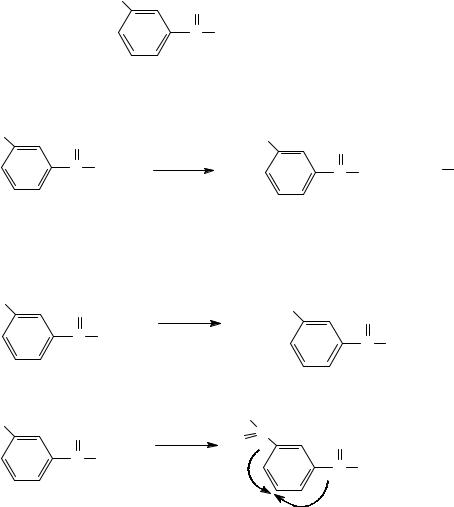
1)HOCH2
2)HOCH2
3)HOCH2
HOCH2 |
O |
|
|
|
|
|
C OC2H5 |
|
|
||
этиловый эфир |
|
|
|
||
3-(гидроксиметил)бензойной кислоты |
|
||||
O |
NaOH |
HOCH2 |
O |
|
|
C OC2H5 |
|
|
C ONa + HO C2H5 |
||
t, oC |
|
|
|||
|
|
|
|
этанол |
|
|
|
|
|
|
|
|
|
|
натриевая соль |
|
|
|
|
|
3-(гидроксиметил)- |
|
|
|
|
бензойной кислоты |
|
||
O |
Na |
NaOCH2 |
O |
+ H2 |
|
C OC2H5 |
|
|
|
||
|
|
|
|
||
|
|
|
C OC2H5 |
||
|
[O] |
HO |
II рода |
|
|
O |
O |
C |
O |
|
|
|
|
||||
C OC2H5 |
|
|
|
C OC2H5 |
|
|
|
|
|
II рода |
|
С10Н10О4
согласованная ориентация заместителей
ПРИМЕР РЕШЕНИЯ ЗАДАЧИ 31
I. Приведите формулу соединения D-псикоза, назовите его в соответствии с классификацией углеводов (например, кетотетроза). Запишите его аномерные формы в виде формул Хеуорса, укажите в них гликозидные гидроксилы. Сколько стереоизомеров можно построить для оксо- и циклической форм?
II. Приведите для соединения D-псикоза формулы энантиомера, диастереомера и эпимера. Дайте определение этих понятий.
III. Для соединения D-псикоза напишите уравнения реакций с реагентами NH2NH2, H ; NaOH, H2O; ангидрид уксусной кислоты.
231

Для выполнения задачи рассматриваем классификацию, номенклатуру и химические свойства моносахаридов.
Углеводы − природные вещества, которые в соответствии с химической классификацией являются полиоксиальдегидами или полиоксикетонами либо продуктами их конденсации.
Углеводы делят на 3 группы.
1.Моносахариды, илимонозы, − неподвергаютсягидролизуинераспадаютсянаболеепростыесахара. Примеры: глюкоза, фруктоза, ксилоза.
2.Олигосахариды − при гидролизе распадаются на несколько моносахаридов:
C12H22O11 |
H2O |
C H O |
6 |
+ C H O |
6 |
||
|
|||||||
сахароза |
|
6 |
12 |
6 |
12 |
||
|
глюкоза |
фруктоза |
|||||
3. Полисахариды – высокомолекулярные вещества, распадающиеся при гидролизе на n молекул моносахаридов:
(C6H10O5)n n H2O nC6H12O6
целлюлоза глюкоза
Моносахариды (монозы), классификация
1.В зависимости от числа атомов углерода в молекуле моносахарида различают триозы (три атома углерода), тетрозы, пентозы, гексозы, гептозы и т. д.
2.В зависимости от характера карбонильной группы (альдегидная или кетонная) моносахариды могут быть альдегидоили кетоноспиртами. Моносахариды, содержащие альдегидную группу, называются
альдозами, кетонную группу – кетозами.
|
O |
|
|
CH2OH |
||
С |
|
|||||
C |
|
O |
||||
|
H |
|
||||
|
|
|||||
|
|
|||||
|
|
|
|
|
|
|
|
CHOH |
|
|
|
||
|
CHOH |
|||||
|
CHOH |
|
|
CHOH |
||
|
|
|||||
|
CHOH |
|
|
CHOH |
||
|
|
|||||
|
CH2OH |
|
|
CH2OH |
||
|
|
|||||
альдопентоза |
кетогексоза |
|||||
Большинство моносахаридов имеют тривиальные названия: ксилоза, рибоза, глюкоза, фруктоза и т. д. (см. табл. 49). Эти названия
232

имеют суффикс «оза». Тривиальные названия применяют в систематической номенклатуре производных этих углеводов. Например, рибоза: рибуроновая кислота, рибаровая кислота, рибит.
Немецкий химик Э. Фишер для изображения моносахаридов предложил проекционные формулы, которые отражают их пространственное строение. Атомы углерода, связанные с гидроксильными группами, в формуле Фишера (кроме первичного –СН2ОН) не изображаются. Нумерация главной цепи начинается от атома углерода альдегидной группы либо с той стороны, где ближе находится кетогруппа. Так как данные монозы содержат карбонильную группу, то называют такую форму изображения оксоформой.
|
|
|
O |
|
|
|
|
|
|
|
O |
||
С |
|
|
|
|
|
|
|
||||||
|
|
|
С |
||||||||||
|
|
|
H |
|
|
|
|||||||
|
|
CH |
|
|
|
|
|
|
|
H |
|||
|
|
|
|
OH |
|
|
|
|
|
|
|
||
|
|
|
|
H |
|
|
|
|
OH |
||||
|
|
|
|||||||||||
|
|
|
|
|
|
|
|||||||
|
|
CH |
|
OH |
HO |
|
|
|
|
|
|
H |
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|||||
|
|
||||||||||||
|
|
CH |
|
OH |
H |
|
|
|
|
|
OH |
||
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
||||||
|
|
CH |
|
OH |
H |
|
|
|
|
|
OH |
||
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|||||||||||
|
|
CH2OH |
|
|
|
|
|
CH2OH |
|||||
|
|
|
|
|
|
||||||||
формула Фишера
Все монозы содержат асимметрические атомы углерода (при атоме углерода есть четыре разных заместителя) и существуют в виде нескольких оптических (пространственных) изомеров, количество которых можно определить по формуле Фишера: N = 2n, где n – число асимметрических атомов углерода. Например, в приведенной ниже монозе асимметрические атомы углерода обозначены звездочками. Количество таких атомов – 4. Следовательно, подставив в формулу Фишера данное число, получаем количество пространственных изомеров – 16.
|
O |
|
|
|
|
С |
|
|
|
H |
H |
|
|
|
OH |
n = 4 |
|
||
HO |
H |
|
||
N = 24 |
= 16 |
|||
H |
OH |
|||
|
|
|||
H |
OH |
|
|
CH2OH
Для всех моноз установлены относительные конфигурации, т. е. пространственное расположение гидроксильных групп у асимметрических атомовуглеродаотносительноконфигурацииD-глицериновогоальдегида.
233

Принадлежность моносахарида к тому или иному генетическому ряду определяется по конфигурации его последнего, считая от альдегидной группы, асимметрического атома углерода. Если она соответствует конфигурации D-глицеринового альдегида (группа −OH стоит справа от вертикальной линии), то моноза относится к D-ряду. Если группа −OH стоит слева, то соответствует конфигурации L-глицери- нового альдегида, и моноза относится к L-ряду.
|
|
|
|
|
|
|
|
O |
|
|
|
|
С |
O |
||||||||
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
С |
|
|
|
|
H |
||||||||||||
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
H |
|
|
|
OH |
|
|
|
HO |
|
|
H |
|||||||||||
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
CH2OH |
||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
CH OH |
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
D |
L |
|
|
|
|
|
|||||||||
|
|
|
глицериновый альдегид |
|||||||||||||||||||
|
|
|
|
|
|
|
|
Пример |
|
|
|
|
|
|
|
|
O |
|||||
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
С |
|
|
|
|
|
|
С |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
H |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
H |
|
|
|
|
OH |
|
|
HO |
|
|
|
|
H |
|||||||||
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
HO |
|
|
|
|
|
H |
|
|
H |
|
|
|
|
|
OH |
|||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
H |
|
|
|
|
|
OH |
|
|
HO |
|
|
|
|
|
|
H |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
H |
|
|
|
|
|
OH |
|
|
HO |
|
|
|
|
|
H |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
CH2OH |
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
CH2OH |
||||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||||
D-глюкоза L-глюкоза
Монозы, отличающиеся друг от друга конфигурацией лишь одного асимметрического атома углерода, называются эпимерами. Например, D-глюкоза и D-манноза.
|
O |
|
O |
|
С |
|
С |
H |
H |
HO |
H |
OH |
H |
||
HO |
H |
HO |
H |
H |
OH |
H |
OH |
H |
OH |
H |
OH |
CH2OH CH2OH
D-глюкоза D-манноза
эпимеры
234
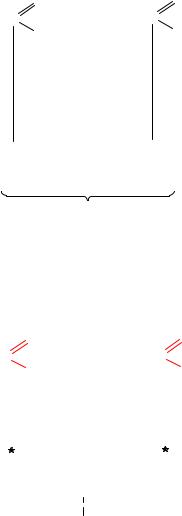
Монозы, отличающиеся друг от друга конфигурацией нескольких асимметрических атомов углерода, называются диастереомерами. Например, D-глюкоза и D-талоза.
|
|
|
|
|
|
O |
|
|
|
|
O |
|
|
|
С |
|
|
С |
|||||
|
|
|
|
|
|
H |
|
|
|
|
H |
H |
|
|
OH |
HO |
|
|
|
H |
|||
|
|
|
|||||||||
|
|
|
|
||||||||
HO |
|
|
|
|
|
H |
HO |
|
|
|
H |
|
|
|
|||||||||
|
|
|
|
|
|
|
|||||
H |
|
|
|
|
OH |
HO |
|
|
|
H |
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|||||
H |
|
|
|
OH |
H |
|
|
OH |
|||
|
|||||||||||
|
|
|
|
|
|||||||
CH2OH CH2OH
D-глюкоза D-талоза
диастереомеры
Монозы, которые имеют противоположную конфигурацию всех асимметрических атомов углерода и относятся друг к другу как предмет к своему зеркальному изображению, называют энантиомерами. Например, D-глюкоза и L-глюкоза.
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
С |
|
|
|
|
С |
|||||||
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
H |
|
|
|
OH |
|
HO |
|
|
|
|
H |
||||
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
||||||||
HO |
|
|
|
|
H |
|
H |
|
|
|
|
|
OH |
||
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|||||
H |
|
|
|
|
OH |
|
HO |
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|||||
H |
|
|
|
|
OH |
|
HO |
|
|
|
|
|
H |
||
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
CH2OH |
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
CH2OH |
|||||||
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
||||||||
D-глюкоза L-глюкоза
Хеуорс установил свойства моносахаридов, которые не объясняются предложенными выше оксоформами:
а) медленная реакция с NaHSO3;
б) повышенная реакционная способность одной из ОН-групп; в) наличие в 2 раза большего числа изомеров, чем предсказывает
формула Фишера; г) явление мутаротации.
Было установлено, что моносахариды могут иметь двоякое строение:
а) альдегидо- и кетоноспиртов − оксоформа; б) внутренних циклических полуацеталей – циклическая форма.
235
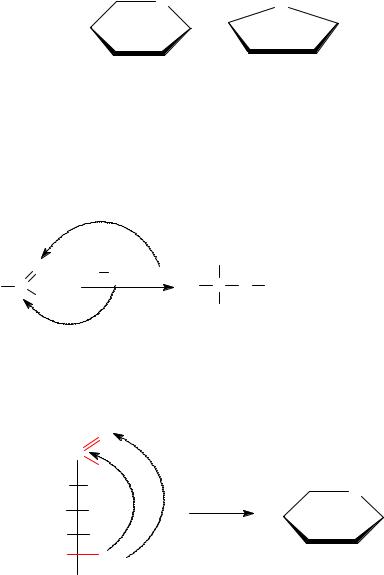
Последняя не содержит свободной альдегидной или кетонной группы, но легко может образовывать оксоформу путем разрыва цикла.
В кристаллическом состоянии моносахариды имеют циклическое строение, а в растворах могут быть циклическими и открытыми оксоформами.
Для циклических форм моносахаридов принято их изображение в виде формул Хеуорса: пиранозной и фуранозной.
O O
пиранозная фуранозная
Циклическая форма моноз образуется при внутримолекулярном взаимодействии карбонильной группы и гидроксильной, связанной с пятым (С–5) или четвертым (С–4) атомами углерода. Данная реакция приводит к образованию простой эфирной связи и появлению новой гидроксильной группы – полуацетальной, или гликозидной.
|
O |
R1 |
CH2OH |
OH полуацетальныйгидроксил |
||
R C |
R C O |
CH2R1 |
||||
H |
|
|
||||
|
|
|
H |
|
||
|
|
|
|
|
||
полуацеталь
Взаимодействие карбонильной группы с гидроксильной при С–5 приводит к образованию шестичленного цикла: 5 атомов углерода и 1 атом кислорода. Следовательно, цикл образуется пиранозный:
|
O |
|
1С |
|
|
|
H |
|
H |
OH |
O |
HO |
H |
|
H |
5 OH |
|
H |
OH |
пиранозный |
|
|
|
CH2OH
D-глюкоза
Взаимодействие карбонильной группы с гидроксильной при С–4 приводит к образованию пятичленного цикла: 4 атома углерода и 1 атом кислорода. Следовательно, цикл образуется фуранозный:
236

|
O |
|
1С |
|
|
H |
H |
O |
OH |
|
|
HO |
4 H |
|
H |
OH |
фуранозный |
H |
OH |
|
|
CH2OH |
|
D-глюкоза
Пиранозный и фуранозный циклы изображаются в горизонтальной плоскости. Связи, расположенные ближе к наблюдателю, отмечают жирной линией. Атом кислорода в пиранозном цикле располагают в правом верхнем углу, в фуранозном – за плоскостью цикла в верхнем углу. Атомы углерода, которые находятся в цикле, не пишут. Нумерацию атомов углерода начинают от кислорода по часовой стрелке.
5 |
O |
|
O |
|
|
||
|
1 |
4 |
1 |
4 |
2 |
2 |
|
3 |
3 |
пиранозный фуранозный
Гидроксильные группы располагают в цикле по определенному правилу: если гидроксильная группа при соответствующем углероде в оксо-форме (в проекции Фишера) находится слева от вертикальной линии, то в циклической форме ее изображают над плоскостью цикла при данном атоме углерода (вверх), и наоборот, справа − под плоскостью (вниз).
Положение полуацетального гидроксила в циклической форме определяет принадлежность монозы к одной из аномерных форм − α или β. Аномеры − диастереомеры, которые отличаются конфигурацией полуацетального гидроксила при атомах углерода С–1 (для альдоз) или С–2 (для кетоз). Для моноз D-ряда у α-аномера гидроксильная группа находится под плоскостью цикла, у β-аномера − над плоскостью. Для моноз L-ряда наоборот. Добавление еще одного дополнительного асимметрического атома углерода для циклических форм моноз приводит к увеличению количества стереоизомеров в два раза. Например, для глюкозы в оксоформе количество стереоизомеров – 16, в циклической − 32.
237
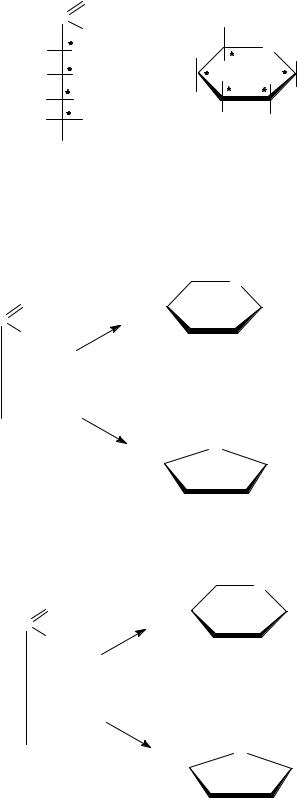
O
|
С |
|
CH2OH |
H |
H |
|
O |
OH |
|
||
HO |
H |
|
OH |
H |
OH |
OH |
OH |
H |
OH |
|
OH |
|
CH2OH |
|
n = 5 |
n = 4 |
N = 25 = 32 |
||
N = 24 = 16
Приводим примеры образования циклических пиранозных и фуранозных формул Хеуорса для некоторых альдоз и кетоз:
|
|
1С |
|
|
O |
|
|
|
|
|
H |
||
|
|
2 |
|
|
||
H |
|
OH |
||||
3 |
||||||
HO |
|
H |
||||
|
|
|||||
H |
4 |
|
|
OH |
||
|
|
|
||||
5 CH2OH
D-ксилоза
|
1С |
O |
|
|
H |
||
|
2 |
||
H |
OH |
||
|
HO |
3 |
|
H |
|||
4 |
||||||
H |
|
|
OH |
|||
|
5 |
|
||||
H |
|
|
|
OH |
||
|
|
|
|
|||
6 CH2OH
D-глюкоза
|
|
5 |
|
|
|
|
|
|
|
|
|
O |
1 |
OH, H |
||||
4 |
|
|
|
|
OH |
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
гликозидный |
||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|||||||||||
|
|
OH |
|
|
3 |
|
|
|
|
|
2 |
|
|
|
гидроксил |
|||
|
|
|
|
|
|
|
|
|
|
|
OH |
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
α-, β-D-ксилопираноза |
||||||||||||||||||
5 CH OH |
|
|
|
|
|
|
|
|
|
|
||||||||
4 |
|
2 |
|
|
|
|
O |
|
|
|
OH, H |
|||||||
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
OH |
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
1 |
|
|||||||
|
|
|
|
|
3 |
|
|
|
|
|
|
|
2 |
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
OH |
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
α-, β-D-ксилофураноза |
||||||||||||||||||
|
|
|
|
|
|
|
|
6 CH OH |
|
|||||||||
|
|
|
|
|
5 |
|
|
|
|
2 |
O |
1 OH, H |
||||||
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
4 |
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
OH |
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
OH |
|
|
3 |
|
|
|
2 |
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
α-, β-D-глюкопираноза |
||||||||||||||||
|
|
6CH OH |
|
|
|
|
||||||||||||
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
OH O |
|
|
|
|
||||||
|
|
5 |
|
|
|
|
|
|
|
OH, H |
||||||||
|
|
4 |
|
|
|
|
|
OH |
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
||||
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
2 |
||||
|
|
|
|
|
|
|
|
|
|
|
|
OH |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
α-, β-D-глюкофураноза |
||||||||||||||||||
238
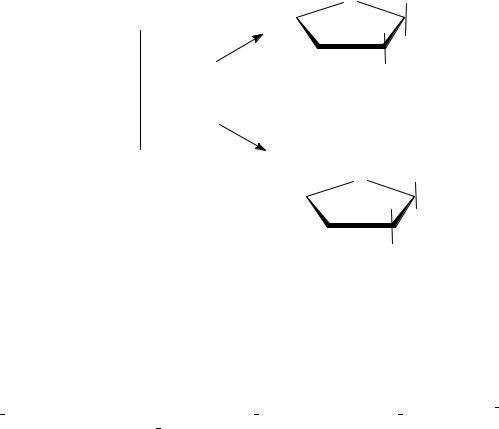
|
|
|
|
|
|
|
6 CH OH |
|
1 |
|
||||||
|
|
|
|
|
|
|
5 |
|
2 |
|
O |
CH2OH |
||||
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
1 СH OH |
|
|
|
|
|
|
|
HO |
2 |
|||||||
2 |
|
2 |
4 |
|
|
|
OH |
|||||||||
|
|
O |
|
|
|
3 |
||||||||||
|
|
|
|
|
|
|||||||||||
|
|
|
|
|||||||||||||
|
3 |
|
|
|
|
|
|
OH |
|
|
||||||
HO |
|
H |
|
|
|
|
|
|
|
|||||||
|
|
α-D-фруктофураноза |
||||||||||||||
H |
4 |
|
|
|
OH |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
H |
5 |
|
|
OH |
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
6CH2OH |
6 CH OH |
|
|
||||||||||||
D-фруктоза |
|
|
2 |
|
O |
OH |
||||||||||
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|||||||||
5 |
|
|
|
|
|
HO |
2 |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
4 |
|
|
|
|
2 |
||||
|
|
|
|
|
|
|
|
|
|
3 |
1 |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
OH |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
β-D-фруктофураноза |
|||||||
Названия циклических формул моносахаридов состоят из:
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
префикса |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
конфигура- |
|
|
|
|
|
названия |
|
|
суффикса |
|
||
|
префиксааномерной |
|
|
|
|
тривиального |
|
|
цикла |
|
|
|
|||||
|
формыα |
илиβ |
|
|
ционной |
|
|
названиямонозы |
|
|
|
|
-оза |
|
|||
|
|
|
|
|
|
|
фуран, пиран |
|
|
|
|||||||
|
|
|
формыD, L |
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
например, β-D-фруктофураноза.
Химические свойства моносахаридов
1. Реакции моносахаридов по карбонильной группе:
а) явление мутаротации − самопроизвольное изменение угла вращения плоскости поляризации света при стоянии свежеприготовленного раствора углевода (физический смысл этого значения). Например, величина удельного вращения для α-D-глюкозы [α]D20 = +112о. При стоянии раствора эта величина снижается до +52,5о. Для β-глюкозы угол вращения повышается с +18,7о до +52,5о. Таким образом достигается равновесная концентрация аномерных α- и β-форм в растворе.
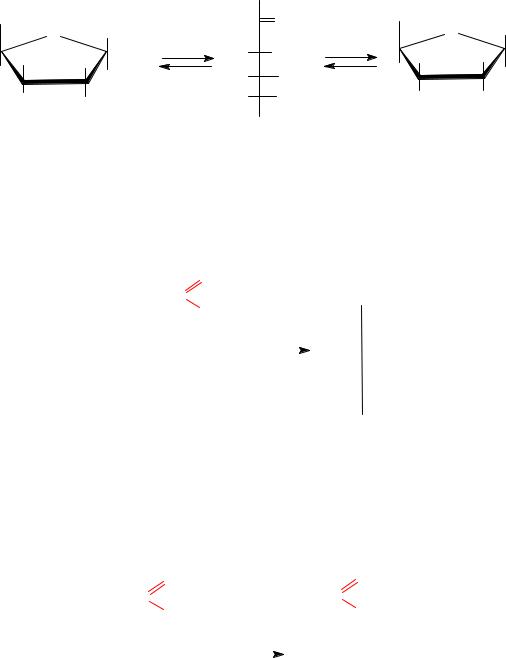
Химический смысл явления мутаротации − взаимное превращение α- и β-форм моноз через промежуточное образование оксоформы:
239
CH2OH |
|
|
СH2OH |
CH2OH |
|
CH2OH |
|
O |
OH |
||
O |
HO |
H |
O |
||
|
HO |
|
HO |
||
|
H |
OH |
|
||
|
OH |
|
CH2OH |
||
OH |
|
H |
OH |
OH |
|
α-D-фруктофураноза |
|
CH2OH |
β-D-фруктофураноза |
||
D-фруктоза
б) реакции восстановления моносахаридов приводят к образованию многоатомных спиртов − альдитов (альдитолов). В качестве восстановителей применяют H2, Ni; H2, Pd; NaBH4; Na, спирт и т. д.:
O
|
С |
|
|
|
CH2OH |
||||||||
|
|
|
|
|
H |
|
H |
|
|
OH |
|||
H |
|
|
OH |
H2, Ni |
|
|
|||||||
|
|
|
|||||||||||
|
|
||||||||||||
HO |
|
|
|
H |
HO |
|
|
|
H |
||||
|
|
|
|
|
|
|
|||||||
|
|
|
|
||||||||||
H |
|
|
|
OH |
|
H |
|
|
|
|
OH |
||
|
|
|
|
|
|
|
|
||||||
|
|
|
|
||||||||||
H |
|
|
|
|
OH |
|
H |
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|||||||||
|
|
|
|
|
|
CH2OH |
|||||||
|
CH2OH |
|
|
|
|||||||||
D-глюкоза |
|
D-глюцит |
|||||||||||
в) реакции окисления моносахаридов действием мягких окислителей (аммиачный раствор оксида серебра Ag(NH3)2OH; щелочной раствор гидроксида меди Cu(OH)2; бромная вода Br2, H2O) приводят к образованию альдоновых кислот.
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
O |
|
|
|
С |
|
|
|
|
|
С |
||||||||
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
OH |
HO |
|
|
|
H |
Cu(OH) , t, oC HO |
|
|
|
H |
||||||||
|
|
|
|
|
|
||||||||||||
|
|
|
|||||||||||||||
HO |
|
|
|
|
H |
2 |
HO |
|
|
|
|
H + Cu2O |
|||||
|
|
|
|
|
|
|
|
|
|
||||||||
H |
|
|
|
|
OH |
|
|
H |
|
|
|
|
|
OH |
|||
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
||||||||||||
H |
|
|
|
|
|
OH |
|
|
H |
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
CH OH |
|
|
|
|
|
CH2OH |
|||||||
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
||||
D-манноза |
D-манноновая кислота |
|
Кетозы в щелочной среде изомеризуются с образованием альдоз (эпимеризация), которые дальше окисляются с образованием альдоновых кислот.
240
