
- •Биоорганическая химия
- •Изомерия органических соединений
- •Классификация изомерии
- •Структурная изомерия
- •Пространственная изомерия (стереоизомерия)
- •Конфигурационные изомеры.
- •Лекция 2 Сопряженные системы
- •Классификация органических реакций
- •Лекция 3 Кислотность и основность
- •Кислоты Бренстеда
- •Лекция 4 Спирты
- •Одноатомные спирты Номенклатура:
- •Физические св-ва
- •Карбокатион
- •Лекция 5 Фенолы
- •Строение молекулы амина
- •Замещенный имин
- •Лекция 8
- •Лекция 9 Карбоновые кислоты
- •Мочевина
- •Лабораторно-семинарское занятие № 4 Тема: «Монофункциональные соединения» Свойства спиртов альдегидов, кетонов и фенолов.
- •Лекция 10 Оксо – окси - фенолокислоты
- •Лекция 11 Аминофенолы, аминоспирты, липиды.
- •Классификация
- •Фосфатидная кислота. Фосфатиды
- •Лекция 12. Углеводы (ув)
- •Лекция Аминокислоты (ак)
- •Лекция 14 Белки
- •Лекция 15 Гетероциклические соединения
- •Лекция 16 Нуклеиновые к-ты
- •Лабораторно-семинарское занятие № 5 Тема: «Гетерофункциональные соединения» Свойства спиртов альдегидов, кетонов и фенолов.
- •Примерные тесты по органической химии
- •Билет № 5
- •Билет № 7
- •Билет № 10
- •Билет № 15
- •Билет № 19
- •Билет № 20
- •Раздел III Биоорганическая химия. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 3
Лекция 5 Фенолы
Это производные ароматических УВ, в которых один или несколько атомов Н замещены на –ОН группу.
|
|
|
|
|
|
|
Ф |
I-Гидрокси- 2-метилбензол, О-крезол |
I-Гидрокси-3-метилбензол, М-крезол |
I-Гидрокси-4-метилбензол, n-крезол |
Бензиловый спирт |
Изомеры положения
Двухатомные фенолы:
|
|
|
|
|
|
|
Пирокатехин, 1,2-Дигидрокси- бензол |
|
Резорцин, 1,3-Дигидрокси- бензол |
|
Гидрохинон, 1,4-Дигидрокси- бензол |
|
| ||||
Каждый фенол дает свое характерное окрашивание в качественной реакции с FеС13:
Фенол Фиолетовое, Гидрохинон Грязно-зеленое,
Пирокатехин Зеленое, Резорцин Фиолетовое,
С
Связь
очень прочная  троение
молекулы
троение
молекулы
 .
.
.
.
. . ..
Связь
менее прочная
–ОН группа проявляет + М >, чем –I, являясь ЭД.
Р-ции SЕ протекают легко за счет +М гр. –ОН, р-ции SN не характерны.
Химические свойства
I. Реакции замещения Н в группе –ОН.
Это проявляется при образовании фенолятов, простых и сложных эфиров.
1) Фенолы за счет р, -сопряжения являются более сильными к-тами, чем спирты (одноатомные и многоатомные) и образуют соли (феноляты) в р-циях с Ме, МеОН и даже солями: Реакция с солями отличает их от одноатомных и многоатомных спиртов.
С6Н5ОН + NаОН С6Н5ОNа + Н2О
Фенолят натрия
Однако фенолы более слабые к-ты, чем Н2СО3, поэтому при действии Н2СО3 (СО2 + Н2О) и др. к-т феноляты легко разлагаются и обратная р-ция не возможна.
С6Н5ОNа + СО2 + Н2О С6Н5ОН + NаНСО3
3С6Н5ОН + FеС13 (С6Н5О)3Fе + 3НС1
Фиолетовое окрашивание
|
2) |
|
На практике используют феноляты.
|
3) |
Сложный
эфир |
|
|
|
4) Р-ция восстановления с цинковой пылью при нагревании:
С6Н5ОН
+ 3Н2
![]() С6Н12
+ ZnО
Р-ции по –ОН группе не характерны!
С6Н12
+ ZnО
Р-ции по –ОН группе не характерны!
Р-ции по бензольному кольцу (SЕ)
–ОН группа – ориентант I рода, облегчает реакции по бензольному кольцу, направляя атаку электрофильного реагента преимущественно в орто- и пара- положения:
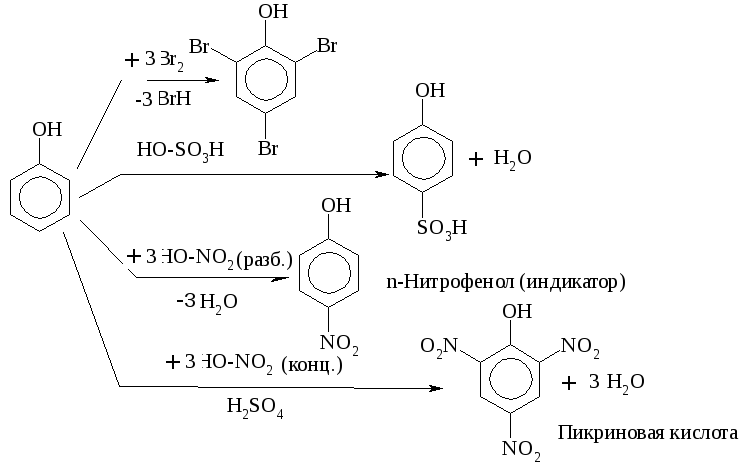
Пикриновая к-та близка по силе (степени диссоциации) к соляной к-те, т.к. содержит три ЭА группы, усиливающие кислотность.
Р-ция гидрирования

Из фенолята натрия легко получается салициловая к-та (важный продукт фармацевтической промышленности):
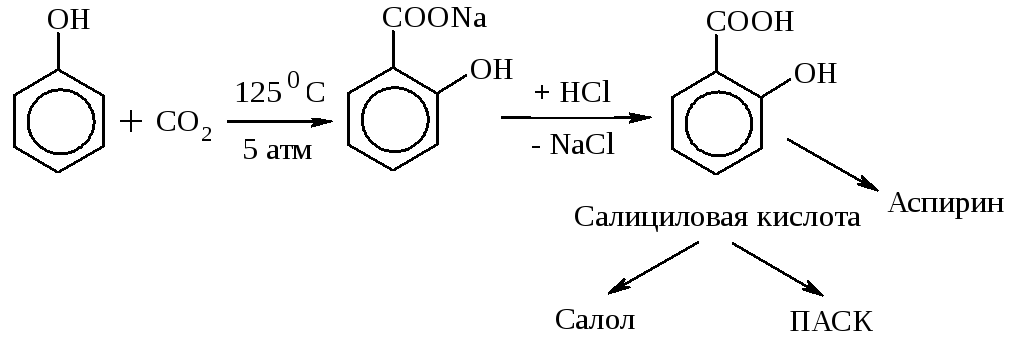
Фенол и его производные обладают дезинфицирующим свойством. Резорцин – антисептик при кожных заболеваниях. Карболовая к-та – 3%-ный раствор фенола – для дезинфекции хирургических инструментов. Пирокатехин применяется для синтеза адреналина – гормона надпочечников. В промышленности фенол используют для получения фенолоформальдегидных смол и ряда красителей.
Увеличение групп –ОН в фенолах увеличивает их активность в р-циях SЕ. Такие фенолы очень легко окисляются, являясь хорошими восстановителями (гидрохинон в фотографии). Двухатомные фенолы легко окисляются под действием слабых окислителей [FеС13, Аg2О, Сu(ОН)2] и даже кислородом воздуха, образуя хиноны. Последние легко восстанавливаются в дигидрохиноны:

Многие биологические вещества содержат «хиноидную» систему: витамин К2 (фактор свертываемости крови), окислительно-восстановительные ферменты тканевого дыхания – убихиноны.
Л и т е р а т у р а:
1.Тюкавкина С. 153-158, 242-246.
Контрольные вопросы к теме «Фенолы»
Какие органичекие соединения называются фенолами?
Изобразите электронное строение молекулы фенола.
Какие виды сопряжения имеются в молекуле фенола?
Какое влияние оказывает группа ОН на бензольное кольцо?
Упражнения и ситуационные задачи:
Напишите реакции фенола с хлорангидридом уксусной кислоты.
Напишите качественную реакцию на фенол.
Напишите реакции фенола с бромом и азотной кислотой.
Напишите реакцию окисления диоксибензола.
Напишите реакцию взаимодействия фенола с гидроксидом натрия и объясните, почему фенол реагирует сщелочами, а одноатомные спирты нет.
Салициловая кислота частично выделяется из организма почками и оказывает некоторое дезинфицирующее влияние в мочевых путях. Напишите реации образования её из фенола.
Пикриновая кислота входит в состав взрывчатых веществ. Напишите реакцию её образования.
Лекция 6
Амины
Это производные аммиака NH3, где один, два или три атома Н замещены на радикал R (алифатический или ароматический).
В зависимости от числа атомов Н, замещенных на R, различают первичные, вторичные и третичные амины. NH2 – аминогруппа, –NH – иминогруппа.
Номенклатура
Рациональная – название радикала (R) + «амин»:
СН3 – СН2– СН2– NН2 СН3 – NН– СН3
Пропиламин Диметиламин
МН рассматривает гр. –NH2 как заместитель в первичных аминах и ее название ставят в приставке перед названием основной цепи (корня):
![]() 2-Аминопропан
2-Аминопропан
Изомерия
Для первичных аминов – изомерия углерод-углеродной цепи (3, 4) и положения гр. – NH2 (1, 2); для вторичных и третичных аминов – изомерия радикала (5, 6) – метамерия:
СН3 – СН2– СН2– NН2

Пропиламин Изопропиламин
СН3 – СН2– СН2– СН2– NН2
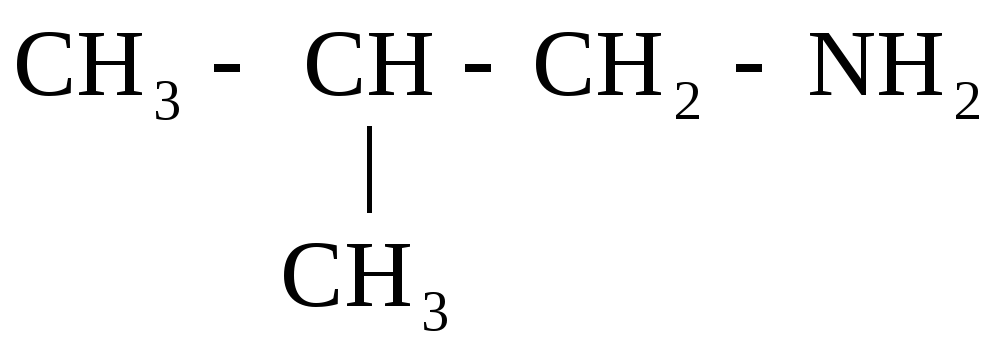
Бутиламин Изобутиламин
СН3 – СН2– СН2–NН–СН3 СН3 – СН2–NН – СН2–СН3
Метилпропиламин Диэтиламин
Физические св-ва
Метиламин, диметиламин, триметиламин – газы, хорошо растворимые в воде; средние члены гомологического ряда аминов – жидкости, высшие – твердые вещ-ва.
Амины в заметных количествах образуются при гниении органических остатков, содержащих белки. Ряд аминов образуется в организме человека и животных из -аминокислот под действием ферментов. Такие амины принято называть биогенными аминами.
Связи N – H, C – N полярны, однако полярность NH связи больше, чем CN согласно различной ЭО атомов N, С, Н. Поэтому первичные и вторичные амины, подобно спиртам, склонны к образованию Н-связей.






 енол
енол


 простой
эфир
простой
эфир