
- •Глава 8. Алициклические углеводороды и их производные
- •8.1. Номенклатура моно- и бициклических соединений
- •8.2. Пространственное строение и изомерия циклоалканов
- •8.2.1. Циклопропан
- •8.2.2. Циклобутан
- •8.2.3. Циклопентан
- •8.2.4. Циклогексан
- •8.3. Химические свойства
- •8.3.1. Реакции циклопропана, циклопропена и их производных
- •8.3.2. Реакции циклобутана и его производных
- •8.3.3. Реакции средних циклов
- •8.3.4. Реакции изомеризации цикла
- •8.4. Способы получения циклоалканов
- •8.5. Терпены и терпеноиды. Каротиноиды
- •8.5.1. Ациклические терпены и терпеноиды
- •3,7-Диметилоктадиен-2,6-ол-1
- •8.5.2. Моноциклические терпены и терпеноиды
- •8.5.3. Бициклические терпены и терпеноиды
- •8.5.4. Каротиноиды
- •8.6. Физиологическая роль и важнейшие представители
- •8.7. Стероиды
- •Вопросы и упражнения
8.3. Химические свойства
Циклоалканы с разным размером цикла имеют разную энергию напряжения и поэтому должны по-разному вести себя в химических реакциях. Так, для малых циклов, у которых энергия напряжения оценивается в 110—115 кДж/моль, могут быть характерны реакции присоединения с раскрытием кольца.
Нормальные циклы (5—7-членные) имеют незначительную энергию напряжения или не имеют её совсем (для циклогексана). Для таких соединений характерны те же реакции, что и для алифатических углеводородов и их производных. Поэтому в данной главе их химические свойства рассматриваться не будут.
Однако в макроциклах имеется трансаннулярное напряжение, что отражается на химическом поведении таких веществ.
Идентификация циклоалканов, как и алканов, с помощью производных почти невозможна. Исключение составляет циклопропан, который способен к превращениям в многообразные соединения за счёт раскрытия цикла.
8.3.1. Реакции циклопропана, циклопропена и их производных
Для циклопропана и его производных характерны реакции: 1) присоединения с раскрытием цикла, 2) замещения с сохранением структуры трёхчленного кольца, а также реакции изомеризации, которые будут рассмотрены отдельно.
Такое разнообразие свойств обусловлено природой -связей между атомами углерода, которые как по геометрии, так и по прочности занимают промежуточное положение между - и -связями.
Циклопропановое кольцо устойчиво к действию озона и разбавленного раствора перманганата калия. Это отличает его от алкенов:

Однако циклопропан подвергается каталитическому гидрированию, но в более жёстких условиях, чем алкены:

Присоединение с раскрытием кольца происходит также при нагревании с водными растворами галогеноводородов:

Механизм в данном случае электрофильный (АdЕ), направление реакции определяется стабильностью образующегося карбокатиона или распределением электронной плотности в исходной молекуле:

метилциклопропан -комплекс
![]()
2-бромбутан
Однако сухой бромоводород не расщепляет циклопропановое кольцо даже при нагревании.
Возможно также присоединение галогенов к циклопропану на свету. Это реакции радикального присоединения. При этом при бромировании других побочных продуктов не образуется:
![]()
1,3-дибромпропан
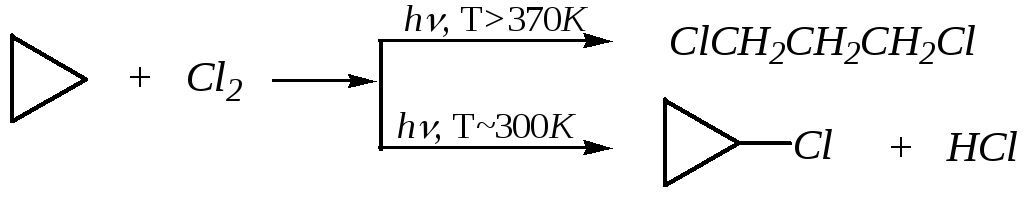
А при хлорировании в зависимости от температуры процесса может идти как присоединение с раскрытием кольца (АdR), так и замещение (SR), с сохранением циклической структуры субстрата:
Циклопропен, в отличие от циклопропана, значительно менее стабилен. Его энергия напряжения составляет примерно 280 кДж/моль. В обычных условиях он быстро разрушается. Одно из направлений такой реакции — полимеризация, которая протекает уже при температуре около 200К. Циклопропен стабилен только в твёрдом виде, он хранится в жидком азоте (при температуре 77К). Стабильность молекулы возрастает при введении заместителей ко всем трём углеродным атомам.
Своеобразным свойством циклопропена является образование стабильного карбокатиона циклопропенилия:

Этот катион является самой простой циклической сопряжённой системой и, в соответствии с рассмотренными далее критериями ароматичности, является ароматической системой (гл. 9.1, 9.8).
