
- •Глава 12. Гетероциклические соединения
- •12.1. Классификация и номенклатура
- •12.2. Пятичленные гетероциклические
- •12.2.1. Номенклатура пиррола, фурана и тиофена и их производных
- •12.2.2. Строение пиррола, фурана и тиофена
- •12.2.3. Физические и химические свойства пиррола, фурана и тиофена
- •12.2.4. Особенности индола
- •12.2.5. Способы получения пиррола, фурана, тиофена, индола
- •12.2.6. Важнейшие представители и медико-биологическое значение
- •12.3. Пятичленные гетероциклические
- •12.3.1. Номенклатура имидазола и пиразола
- •12.3.2. Строение имидазола и пиразола
- •12.3.3. Физические и химические свойства имидазола и пиразола
- •12.3.4. Способы получения
- •12.3.5. Важнейшие представители и медико-биологическое значение
- •12.4. Шестичленные гетероциклические
- •12.4.1. Номенклатура пиридина и его производных
- •12.4.2. Строение пиридина
- •12.4.3. Химические свойства пиридина
- •Но если оба -положения заняты, то замещается водород в-положении. При нагревании с избытком амида натрия можно получить 2,6-диаминопиридин.
- •12.4.4. Особенности химического поведения пиколинов и функциональных производных пиридина
- •12.4.5. Хинолин и изохинолин
- •12.4.6. -Пиран и -пиран и их производные
- •12.4.7. Способы получения
- •Реакция аналогична получению бензола, протекает при высоких температурах, но представляет только теоретический интерес.
- •12.4.8. Важнейшие представители и медико-биологическое значение
- •12.5. Шестичленные гетероциклические
- •12.5.1. Строение и свойства диазинов
- •12.5.2. Пурин
- •12.5.3. Способы получения
- •12.5.4. Важнейшие представители и медико-биологическое значение
- •12.5.5. Нуклеозиды, нуклеотиды и нуклеиновые кислоты
- •12.6. Алкалоиды
- •Вопросы и упражнения
12.4.5. Хинолин и изохинолин
Хинолин и изохинолин — это конденсированные системы, состоящие из пиридинового цикла и бензольного кольца. Поэтому их названия как конденсированных систем:

хинолин изохинолин
(бензо[b]азин) (бензо[c]азин)
Хинолин и изохинолин являются азотоаналогами нафталина, и нумерация атомов в их молекулах проводится так же, как и в молекуле нафталина: в хинолине, начиная с гетероатома, а в изохинолине атом азота имеет номер 2.

Хинолин, изохинолин и их производные — это бесцветные жидкости и низкоплавкие вещества, малорастворимые в воде и имеющие своеобразный запах.
12.4.5.1. Строение
Хинолин и изохинолин, так же, как и их углеродный аналог нафталин, представляют бициклические сопряжённые системы из 10 -электронов. Присутствие атома азота значительно изменяет распределение электронной плотности. Электроноакцепторное влияние атома азота главным образом распространяется на цикл пиридина. Поэтому электронная плотность на бензольном кольце понижена в незначительной степени, а наибольший положительный заряд возникает в положении 2 молекулы хинолина и в положении 1 изохинолина:

12.4.5.2. Химические свойства
Как и пиридин, хинолин и изохинолин являются типичными основаниями с константами основности, близкими к таковым для пиридина. Образование солей протекает аналогично пиридину. Например, для хинолина:
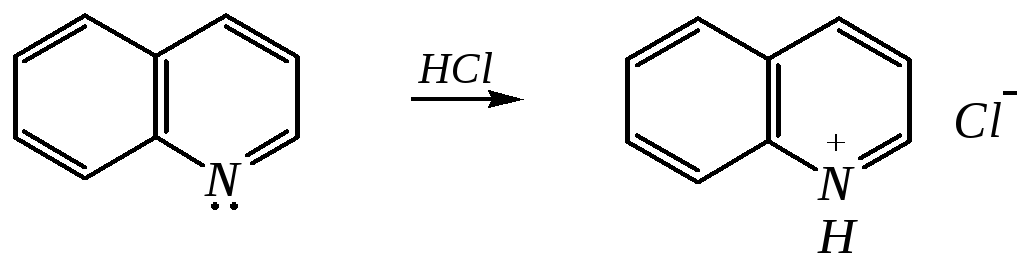
хлорид хинолиния
Реакции алкилирования и окисления по атому азота протекают в тех же условиях и при участии тех же реагентов, что и для пиридина. Например, для хинолина:
|
|
йодид N-алкилхинолиния
хинолин-N-оксид
|
Однако хинолин и изохинолин могут окисляться под действием сильных окислителей (KMnO4, HNO3) с разрушением одного цикла, обычно бензольного. Но окисление изохинолина щелочным раствором перманганата калия приводит к смеси двух кислот.
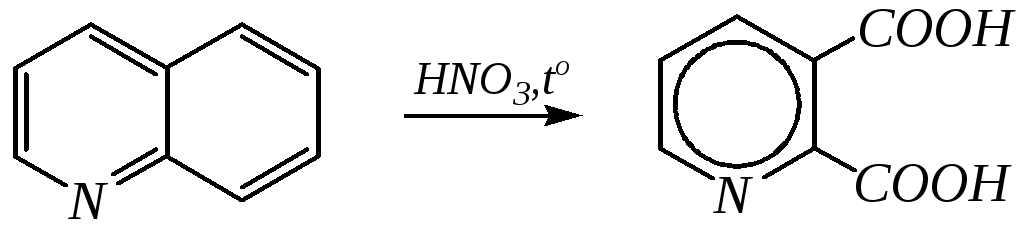
хинолиновая кислота

цинхомеровая кислота

Реакции электрофильного замещения для обоих соединений протекают по бензольному кольцу, обычно по атомам С5 и С8. Но если при нитровании хинолина образуется примерно эквимолярная смесь 5- и 8-нитрохинолинов, то нитрование изохинолина даёт преимущественно 5-нитропроизводное:
 5-нитроизохинолин 8-нитроизохинолин
5-нитроизохинолин 8-нитроизохинолин
90% 10%
Сульфирование при обычных температурах (360—500 К) также приводит к образованию 5- и 8-хинолинсульфокислот (главным образом, 8-производного), но эти изомеры при нагревании выше 530 К переходят в более термодинамически стабильную 6-сульфоновую кислоту.
Галогенирование хинолина и изохинолина в условиях реакции электрофильного замещения (в присутствии кислотных катализаторов) также приводит к 5- и 8-производным. Введение атома галогена в пиридиновое кольцо происходит в значительно более мягких условиях. Так, бромирование хинолина и изохинолина в присутствии незначительных количеств HCl даёт 3-бромхинолин и 4-бромизохинолин соответственно. Механизм процесса на примере изохинолина можно представить в следующем виде:


4-бромизохинолин
Нуклеофильное замещение атома водорода идёт наиболее легко в положение С2 хинолина и С1 изохинолина. Так, например, протекают реакция А.Е. Чичибабина и взаимодействие со щёлочью для хинолина:

хинолон-2
Для хинолина и изохинолина возможно гидрирование как пиридинового цикла, так и бензольного кольца. Восстановить пиридиновый цикл до тетрагидропиридинового можно боргидридами металлов или каталитически водородом в метаноле. Однако каталитическое гидрирование в растворе сильных кислот приводит к первоначальному селективному восстановлению бензольного кольца, а затем — к продукту исчерпывающего гидрирования — декагидропроизводному. Например, для хинолина:


