
- •Глава 12. Гетероциклические соединения
- •12.1. Классификация и номенклатура
- •12.2. Пятичленные гетероциклические
- •12.2.1. Номенклатура пиррола, фурана и тиофена и их производных
- •12.2.2. Строение пиррола, фурана и тиофена
- •12.2.3. Физические и химические свойства пиррола, фурана и тиофена
- •12.2.4. Особенности индола
- •12.2.5. Способы получения пиррола, фурана, тиофена, индола
- •12.2.6. Важнейшие представители и медико-биологическое значение
- •12.3. Пятичленные гетероциклические
- •12.3.1. Номенклатура имидазола и пиразола
- •12.3.2. Строение имидазола и пиразола
- •12.3.3. Физические и химические свойства имидазола и пиразола
- •12.3.4. Способы получения
- •12.3.5. Важнейшие представители и медико-биологическое значение
- •12.4. Шестичленные гетероциклические
- •12.4.1. Номенклатура пиридина и его производных
- •12.4.2. Строение пиридина
- •12.4.3. Химические свойства пиридина
- •Но если оба -положения заняты, то замещается водород в-положении. При нагревании с избытком амида натрия можно получить 2,6-диаминопиридин.
- •12.4.4. Особенности химического поведения пиколинов и функциональных производных пиридина
- •12.4.5. Хинолин и изохинолин
- •12.4.6. -Пиран и -пиран и их производные
- •12.4.7. Способы получения
- •Реакция аналогична получению бензола, протекает при высоких температурах, но представляет только теоретический интерес.
- •12.4.8. Важнейшие представители и медико-биологическое значение
- •12.5. Шестичленные гетероциклические
- •12.5.1. Строение и свойства диазинов
- •12.5.2. Пурин
- •12.5.3. Способы получения
- •12.5.4. Важнейшие представители и медико-биологическое значение
- •12.5.5. Нуклеозиды, нуклеотиды и нуклеиновые кислоты
- •12.6. Алкалоиды
- •Вопросы и упражнения
12.5.2. Пурин
Пурин (имидазо[4,5-d]пиримидин) представляет собой конденсированную бициклическую систему, построенную из пиримидинового и имидазольного циклов. Он имеет свою, оригинальную нумерацию атомов, которая отличается от правил нумерации конденсированных структур. Пурин существует в виде двух таутомеров — 9Н-пурина и 7Н-пурина. (Ещё две теоретически возможные таутомерные формы, 1Н-пурин и 3Н-пурин, не обнаружены.)

9Н-пурин 7Н-пурин
В кристаллическом состоянии пурин существует в виде 7Н-таутомера, однако в растворе 7Н-пурин и 9Н-пурин представлены примерно в равных количествах.
Система пурина, подобно бициклической системе индола, содержит 10--электронную систему. При этом в имидазольном кольце электронная плотность повышена, а в пиримидиновом, наоборот, понижена по сравнению с бензольным.
По кислотным свойствам пурин (рКа = 8.9) — немного более сильная кислота, чем фенол (рКа = 9.9), и значительно более сильная кислота, чем имидазол (рКа = 14.2). Такая сравнительно высокая кислотность обусловлена значительной делокализацией отрицательного заряда аниона между четырьмя атомами азота:

Основные свойства пурина выражены слабо (рКb = 11.5); в растворе существуют все три возможные протонированные формы пурина, но с преобладанием катиона, образующегося при N1-протонировании:

Алкилирование пурина протекает довольно сложно, и в нём могут участвовать нейтральная молекула или анион. С йодметаном в метаноле при 373 К образуется соль 7,9-диметилпуриния:

Возможные углеродные центры электрофильной атаки как в пиримидиновом, так и в имидазольном циклах пуриновой системы заняты, и вполне очевидно, что Se-реакции для самого пурина неизвестны. Однако замещённый пурин может галогенироваться, нитроваться и даже вступать в реакцию азосочетания, как это показано в следующих примерах.
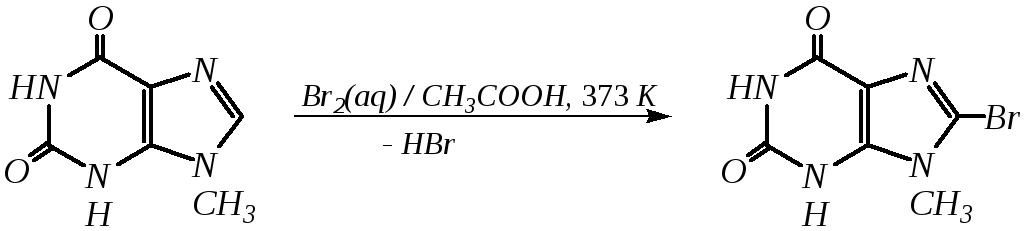


Нуклеофильное замещение наиболее характерно для галогенозамещённых пуринов. Реакции замещения для 2-, 6- или 8-галогенопуринов протекают относительно легко с такими нуклеофилами, как амины, цианиды, алкоксиды, сульфиды и др. Механизм реакции SN2аром. Например:
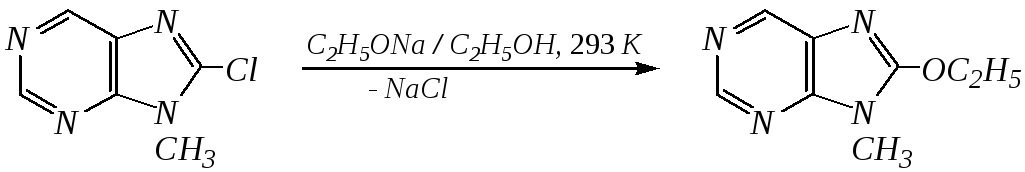
В 9-замещённых галогенопуринах наибольшей реакционной способностью обладает галоген в 8-м положении, в 9Н-галогенопуринах — галоген в 6-м положении. Изменение реакционной способности галогена в положении 8 связано с образованием аниона в пятичленном цикле 9Н-пурина, и нуклеофильная атака осуществляется по пиримидиновому кольцу. При наличии заместителя в 9-м положении пятичленный цикл протонируется растворителем, что облегчает нуклеофильную атаку по этому кольцу.


12.5.3. Способы получения
В синтетическом отношении производные диазинов оказываются более доступными, чем сами незамещённые гетероциклы.
1. Пиримидиновое кольцо получают конденсацией -дикарбонильных соединений с мочевиной или её производными. Например, барбитуровая кислота образуется из малонового эфира и мочевины:

барбитуровая кислота
Сам пиримидин может быть получен путём превращения барбитуровой кислоты в трихлорпиримидин, и последующим его восстановлением:
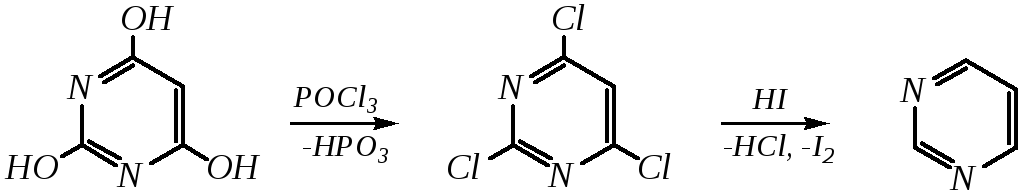
2. Пиразиновое кольцо легко образуется при самоконденсации -аминокарбонильных соединений (в том числе-аминокарбоновых кислот — гл. 6.9.2.3).

2,5-дигидротетраалкилпиразины
3. Пиридазин и его производные получают с использованием гидразина.
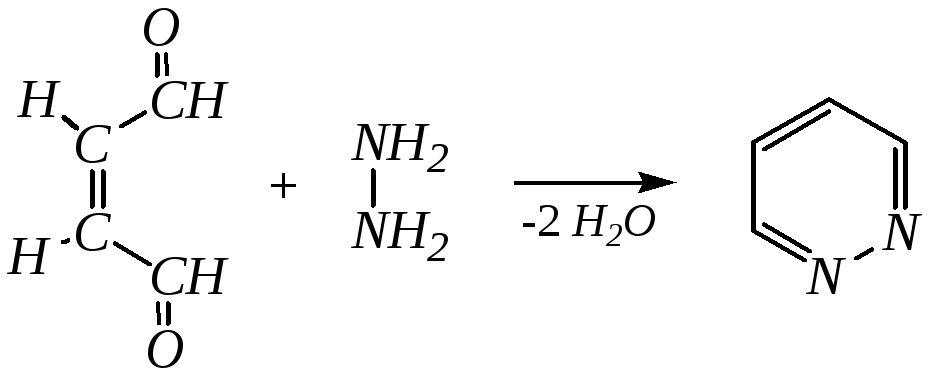
4. Для получения пурина и его производных могут использоваться 5,6-диаминопиримидины (или соответствующие гидроксильные производные). Например, аминобарбитуровая кислота при конденсации с цианатом (изоцианатом) калия образует мочевую кислоту, которая затем может быть превращена в пурин:

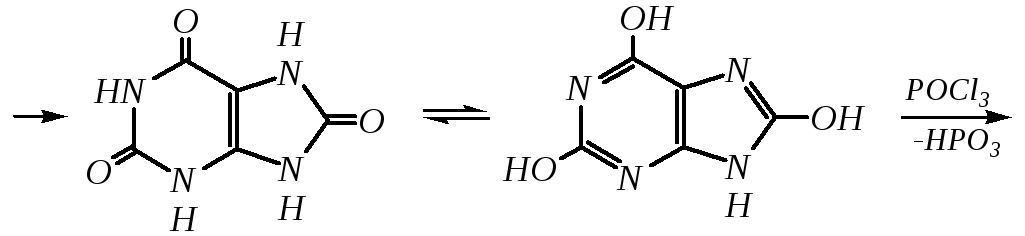
мочевая кислота

