
физика экзамен
.pdf
|
Вопрос№1 |
|
1)Понятиетермодинамическойсистемы. |
|
|
Определение: Термодинамика –наукао закономерностяхпревращенияэнергии. |
В |
|
термодинамикеширокоиспользуетсяпонятие |
термодинамическойсистемы |
. |
Определение: Термодинамической системойназываетсяовокупностьматериальных тел, взаимодействующих, какмеждусобой, таки с окружающейсредой.
2)Видытермодинамическистемх
1)Открытаятермодинамическаясистема(обмениваетсявеществоми энергиейс окр.средой
2)Закрытаятермодинамическаясистема(обмениваетсяокр.средойтольковеществом) 3)Изолированнаятермодинамическаясистема(необмениваетсяокр.средой)
3)Внутренняяэнергиятел.
Энергиюлюбойсистемыможноразделитьнадвечасти: 1)энергия, зависящаяотположениядвижениясистемы, какцелого, и 2) энергия, определяемаясостояниемвзаимодействиемчастейсистемы(вплотьдоатомов
и молекул). Вторуючастьназывают внутреннейэнергиейсистемы |
U. |
|
Изменениевнутреннейэнергиисистемы( |
U ) можетпроисходитьдвумяспособами. |
|
Во-первых, системаможетсовершитьработу( |
А) надокружающимителами. |
|
Во-вторых, энергияможетбытьполучена(илиотдана) в результатестолкновениймолекул илииспусканияпоглощенизлучения(в обыденнойжизничащевсего–инфракрасных лучей).Вэтомслучаеговорят передачетепла (Q).Положительнымсчитаетсятепло, полученноет лом.
Позаконусохраненияэнергииотсюдаследует: |
U = Q – A (1) |
Этаформуланазывается первымначаломтермодинамики . Онаявляетсяоднимиз важнейшихсоотношенийфизики техники.
4)Cвободнаяисвязаннаяэнергии.
внутренняяэнергиялюбойсистемысостоитиздвухразныхчастей:
1. Свободнаяэнергия G – этотачастьвнутреннейэнергии, которуюв принципеможно полностьюиспользоватьдлясовершенияработы
2. Связаннаяэнергия WСВЯЗ, которуюв данныхусловияхвообщенельзяпревратить
в работу . Вбольшинствеслучаевсвязаннаяэнергия–эточастьэнергиитеплового движениясоставляющихсистемучастиц.
Сказанноеможновыразитьвидеформулы: |
U = G + WСВЯЗ (2) |
|
|
5)Обратимыенеобратимыепроцессы. |
|
|
|
Процессы, прикоторых |
А = G , называются обратимыми, потомучтозатративработу |
А |
|
мыможемвернутьсистемув исходноесостояние. |
|
1 |
|
|
|
|
|

Всепроцессы, в которых А < G являются необратимыми; чтобыв этомслучаевернуть системув исходноесостояниенадозатратитьработыбольше, чембылополучено. Влюбом реальномпроцессечастьсвободнойэнергииобязательнопревращаетсятепло, тоестьв связаннуюэнергию.
6)Диссипациясвободнойэнергии.
Переходсвободнойэнергиив теплоназывают диссипациейсвободнойэнергии (слово „диссипация“по-русскизначит„рассеяние“).Однако, в некоторыхслучаях, когда диссипациянезначительна, можноусловносчитатьпроцессобратимым(как, например, мы считаемвоздухидеальнымгазом).
Вопрос№2
1)Первоеначалотермодинамикидлязакрытыхпроцессов
2)Применениеп рвогоначалатермодинамикизопроцессам.
Первоеначалотермодинамики:
приизобарномпроцессе |
Q=∆U+A=∆U+P∆V |
|
|
|
приизохорномпроцессеA=0 |
|
|
|
|
Q=∆U=(m/M)*Cv∆T |
|
|
|
|
приизотермическомпроцессе∆U=0 |
|
|
|
|
Q=A=(m/M)*RT In[V1/V2] |
|
|
|
|
Здесьm — масса газа, M — молярнаямасса газа, Cv— молярнаятеплоёмкость |
при |
|||
постоянномобъёме, p,V,T — |
давление, объём и температура газасоответственно, причём |
|||
последнееравенствовернотолькодляидеальногазао. |
|
|
|
|
3)Применениеп рвогоначалатермодинамикиживыморганизмам. |
|
|
||
. Еслисвободнуюэнергию, получаемуюприихусвоении, обозначить |
GПИЩИ, топервое |
|||
началоможнозаписатьв такомвиде: |
|
|
|
|
GПИЩИ = U + A + Q |
(3) |
|
|
|
тоестьэнергияпищиидёт: |
|
|
|
|
а) наповышениевнутреннейэнергииорганизма; |
|
|
|
|
б) насовершениеработыи |
|
|
|
|
в) натеплоотдачув окружающуюсреду (организмвсегдадолжен |
отдавать |
тепло, иначеон |
||
перегреется, чтонесовместиможизнью). |
|
|
|
|
Внутренняяэнергияорганизмав большинствеслучаевлишьколеблетсяв некоторых
2

пределах, нов среднемостаётсяпостоянной( U = 0)Тогда.
GПИЩИ = A + Q |
(4) |
Этаформуланазывается уравнениемэнергетическогобаланса.
Вопрос№3
1)Макроэрги, хрольв жизнедеятельности.
Вживыхорганизмахсвободнаяэнергия, получаемаяприусвоениипищи, почтицеликом
выделяетсяходебиологическогоокисления, происходящегонавнутреннихмембранах
митохондрий. Примерно50%этойэнергиидиссипирует(выделяетсявидетепла, которое целикомуходитв окружающуюсреду).Остальные50%тратятсянасинтезтакназываемых
макроэргов –веществ, обеспечивающихэнергиейвсеклеткиорганизма. Важнейшимиз
такихвеществявляетсяаденозинтрифосфорнаякислота (АТФ).
Работав живоморганизмепроизводитсязасчётэнергии, выделяющейсяприотщеплении отАТФконцевойфосфатнойгруппыНРО 3 (обычнобозначаемойднобуквойФ) и переносе
этойгруппынакакое-тодругоевещество, чащевсего–наводу:
АТФ-аза |
|
↓ |
|
А-Ф-Ф~Ф+Н |
2О→А-Ф-Ф+Н 3 РО4 +энергия(около30кДж/моль) |
АТФ( ) |
АДФ( ) |
РеакциякатализируетсяферментомАТФ-азой. Количествоэнергии, выделяющеесяпри переносефосфатнойгруппы, можетколебаться(в зависимостиотусловийреакции) от 26до
38килоджоулейнамоль; обычнопринимаютсреднююцифру30кДжнамоль. Другими словами, изменениехимическогопотенциалаприотщеплениифосфатнойгруппыпримерно равно30кДж/моль.
Насовершениеработыиспользуетсяоколо40%этойэнергии, или20%отисходнойэнергии пищи. Остальнаяэнергияопять-такипревращаетсятеплои уходитизорганизма. Таким образом, КПДорганизмасоставляетоколо20%.
Резюмируя, можносказать, чтоживыеорганизмыотличаютсяпреждевсеготем, что роль
промежуточногозвенамеждуисточникомсвободнойэнергииработойвнихвыполняет нетепловаяэнергия, а химическая (энергияАТФи другихмакроэргов).
Синтезмакроэрговпроисходит, основном, засчётокислениямономеров, накоторые
3

расщепляютсяв кишечникепищевыепродукты. Важнейшимизэтихмономеровявляется глюкоза. Засчётэнергии, выделяющейсяприокислении1моляглюкозы, может синтезироваться36молейАТФ. Этотакназываемый аэробный синтез; онтребуетрасхода кислорода. Крометого, 2моляАТФмогутсинтезироватьсябезучастиякислородапридругих реакциях( анаэробный синтез).Такимобразом, засчётэнергии1моляглюкозывсегоможет синтезироваться38молейАТФ. Близкиецифрыхарактерныи длядругихмакроэргов.
2)Видыработ, совершаемыхорганизме.
. Основныминаправлениямизатратыэнергииявляются:
1. Мышечнаяработа.
2.Синтезсложныхмолекул, в первуюочередь–белков.
3.Поддержаниеразницыконцентрациймногихвеществ(в первуюочередьионов) в цитоплазмев межклеточнойсреде.
4.Поддержаниеразностипотенциаловнамембранахклеток.
Рассмотримэтипроцессыподробнее.
1. Мышечнаяработа нетребуетособыхпояснений, однако, надоиметьв виду, чтопонятия работыв физике в физиологиизаметноразличаются. Простейшийпример: с точкизрения физикичеловек, стоящийпостойке«смирно» несовершаетникакойработы(путьравеннулю
2. |
Синтезмакромолекул. |
(белков) Наэтозатрачиваетсязначительнаяэнергия(от25 000кДж/ |
|
мольдо200 000кДж/мольдляразныхбелков).Этуэнергиюможноподсчитатьформуле: |
|||
Gсинт =ν·Δµ (5), где |
ν –числосинтезированныхмолей, µ –изменениехимического |
||
потенциалаприсинтезеданногобелка. |
|
||
3. |
Поддержаниеразностиконцентраций. |
Вовсехклеткахконцентрациябольшинствещества |
|
внутриклеткизаметно(частовомногораз) отличаетсяконцентрацииснаружи. Например, ионовкалияв цитоплазмегораздобольше, чемв межклеточнойжидкости, а ионовнатрия, наоборот, намногобольшеснаружи. Такаяразницаконцентрацийнеобходимадля жизнедеятельностиклеток. Ионы(и прочиевещества) поддействиемразностиконцентраций достаточнобыстропроникаютчерезмембрану(этоназывают„пассивнымтранспортом“).Для того, чтобыконцентрациивнутри снаружиневыровнялись(чтонесовместиможизнью клетки), в мембранахклетоксуществуютособыемеханизмы(ихчастоназываютнасосами),
которыепереносятвещества |
противразностиконцентраций. |
Наработутакихнасосов |
|
тратитсязаметноеколичествосвободнойэнергии, котороеможноподсчитатьформуле |
|||
GКОНЦ=v*RT*InC1/C2 |
(6) |
|
|
где ν –числомолейперенесенноговещества; С |
1 и С 2 -концентрациипооднуи другую |
||
сторонымембраны. |
|
|
|
4. Созданиеразностипотенциаловнамембранах |
. Цитоплазмавсехклетокзаряжена |
||
отрицательно поотношениюк межклеточнойжидкости. Другимисловами, намембранах |
|||
всехклетоксуществуетпостояннаяразностьпотенциалов, называемая |
потенциаломпокоя |
||
(ПП). Крометого, вомногихклеткахв ответнараздражениевозникаеткратковременная
4

разноcтьпотенциалов( |
потенциалдействия, ПД). НасозданиеППи ПД |
нужнасвободная |
|
энергия, котораяв данномслучаетратитсянапереносионовчерезмембрану |
противразности |
||
потенциалов U. Этаэнергиярассчитываетсяпоизвестнойформуле |
Gпот = q.U (7),где q – |
||
зарядперенесенныхионов, равный: |
q =ν .z.U, где ν –числомолейионов, перенесенных |
||
черезмембрану, z –валентностьиона, F =числоФарадея, тоестьзарядодногомоля одновалентныхионов(F = 96 500Кл/моль).
3)Электрохимическийпотенциал
Учитываявкладвсехтрёхтиповпроцессов(кромемышечнойработы) получимдляобщей затратысвободнойэнергии:
G=v*(∆µ+RT*In[C1/C 2]+zFT) |
(9) |
|
Величина µ ЭХ =∆µ+RT*In[C1/C 2]+zFT |
(10) |
|
называетсяизменением |
электрохимическогопотенциала |
. |
Именноизменениеэлектрохимическогопотенциалаопределяетхарактери направление многихфизико-химическихпроцессов, происходящихв клетках.
Вопрос№4
1)Тепловойбалансорганизма
Ворганизмелюбогоживогосуществанепрерывновыделяетсятепло. Этотеплодолжно отводитсяокружающуюсреду, иначеорганизмперегреетсяи погибнет. Однако, и слишком быстраяотдачатеплаопаснадляорганизма–онаприводитк переохлаждению
Основнаячастьтеплавыделяетсямышцахи внутреннихорганах, отдачажетеплаидётс поверхностиела(с кожи).Ткани организмаплохопроводяттепло, поэтомупочтивсётепло переноситсяизнутрик поверхноститокомкрови. Вкожеи подкожнойклетчаткенаходится большоеколичествокровеносныхсосудов. Проходяпоним, кровьотдаётеплонаружу.
Черезподкожнуюклетчаткуи черезодеждутеплопереноситсязасчёттеплопроводности. Теплопроводность – этопереностеплазасчётусилениямолекулярногодвижениявеществе.
Нетруднополучитьформулудляпереносатеплапутёмтеплопроводности. Пустьпоток |
х, а площадь S. |
||
теплаидётчерезслойвещества(ткань, стенуи т.д.).Толщинуслояобозначим |
|||
Слеватемпературавна |
Т1, а справа(пусть Т1 > Т 2).Очевидно, чтоколичествотепла |
Q, |
|
прошедшеечерезслойзавремя t, прямопропорциональноразноститемператур, площади времени обратнопропорциональнотолщинеслоя. Крометого, надоучестьсвойства вещества; дляэтоговводяткоэффициенттеплопроводностиК. Отсюдаследует, что количествотепла, переносимоепутёмтеплопроводности, равно:
QTП =K*(T1-T2 /X) *St
2)Основныеспособытеплообменаорганизма.
Споверхностиодеждыи с открытыхчастейтелатеплоуходитдвумяспособами: ) путём конвекции б) путёмизлучения.
Конвекцией называютпереностепла, связанныйдвижениемгазаилижидкости. 1)естественнаяконвенция - откаждогочеловекакверхуподнимаетсяпотоктёплоговоздуха, на местокоторогопритекаетсостороныхолодный.
5

2)принудительнаяконвекция , когдадвижениевоздухасоздаётсявнешнейпричиной (вентилятор, ветер)
Q = W/t ТепловойпотокQ -количествотеплотыW, ДЖ( ) проходящиезавремяТ, (С) черезданнуюповерхностьнаправлениинормалик ней
Излучение тожеиграетсущественнуютольв теплоотдаче. Вобычныхкомнатныхусловиях (в томчисле, в учебнойаудитории) людипутёмизлучениятеряютдо60%тепла. Излучение человекалежитв областинфракрасныхлучей(длиныволнв диапазоне3 – 20микрометров).
Количествотепла, теряемоетеломзасчётизлучения, вычисляетсяпоформуле: |
|
QИЗЛ =σ·( |
|
T14 – T24).S.t (14)Здесь. σ = 5,6.10 –8 (в системеСИ; запоминатьчислоненадо),Т |
1 – |
||
температураповерхностиела, Т |
2 –температураокружающихтел. Тут, однако, надо |
|
|
заметитьследующее. Воздухпочтипрозрачендляинфракрасных |
лучей, поэтомузаТ 2 надо |
||
братьнетемпературувоздуха помещении, а температурустен, а онаможетбытьзаметно нижетемпературывоздуха. Например, вполнереальнаситуация, когдалежащийнастоле
термометрпоказываетбольше20 0С (тоестьтемпературувоздуха),а людив помещении мёрзнут, потомучтостеныхолодные.
Привысокойнаружнойтемпературенапервыйпланвыступаетотдачатеплазасчёт испарения. Когданаружнаятемператураприближаетсяк температурела, все рассмотренныеранееспособытеплоотдачинеработают, потомучторазностьтемператур, от
которойзависитпереностепла, делаетсямалойилидажеможетстатьотрицательной.
Количествотепла, уносимоеизорганизмазасчётиспарения, можноподсчитатьформуле:
QИСП = L· m (15),
где m –массаиспарившейсяводы, |
L – удельнаятеплотаиспаренияводы(2,25 |
.106 Дж.кг –1; |
запоминатьчислоненадо).Учеловекаиспарение, в основном, связано потоотделением; |
|
|
крометого, заметнуюрольиграетиспарениеводыв лёгких. Надоподчеркнуть, чтоследует |
|
|
учитыватьименноколичество |
испарившейся воды, потомучтодалеконевесьпотфактически |
|
испаряется. Здесьоченьбольшоезначениеимеетвлажностьвоздухаи скоростьегодвижения.
Приумеренныхи низкихтемпературахиспарениетожеуноситчастьтепла(в основном, засчётиспаренияв лёгких),нобольшеезначениеимеютконвекцияизлучение.
3)Температурныйгомеостаз
Температурателачеловекаи многихживотныхподдерживаетсяпостояннойдостаточно высокойточностью. Этосвойстворганизманазывают температурнымгомеостазом.
4)Способытерморегуляции
Постоянствотемпературытелаобеспечиваетсявыработавшейсяходеэволюции системой терморегуляции. Различаютхимическуюфизическуютерморегуляцию.
Химическая терморегуляцияосновананаизменениискоростихарактерабиологического окисления. Например, припереохлажденииорганизмавыделяютсягормоны, ускоряющие окисление. Крометого, происходитразобщениеокислениясинтезаАТФ: насинтезАТФ идётне50%энергии, выделяющейсяприокислении, а меньше. Соответственно, б льший процентэнергиипревращаетсятепло; организмсогревается. Однако, изменениехарактера биологическогоокислениянеблагоприятносказываетсянасостоянииорганизма, поэтому, как правило, химическаятерморегуляциявключаетсялишьв экстремальныхситуациях.
Физическая терморегуляция(играющаяв большинствеслучаевосновнуюроль)
6

осуществляетсязасчётизмененияхарактеракровообращения. Припонижениитемпературы теласужаютсяартериолымелкиеартериив кожеи подкожнойклетчатке. Притокровик поверхностиелауменьшается(этопроявляетсятом, чтокожабелеет).Какследствие, уменьшаетсяпередачатеплаотвнутреннихорганови мышцк поверхностиелаи отдача теплав окружающуюсреду. Приповышениитемпературытеласосудырасширяются(кожа краснеет),с усилениемкровотокаувеличиваетсятеплоотдача. Например, в пальцах количествопротекающейкровив зависимостиоттемпературыможетменятьсяв сотнираз! Приповышениитемпературысущественноезначениеимееттакжеусиленноепотоотделение.
Вопрос№5
1)Основнойобмен
Основнойобмен —минимальноеколичествоэнергии, необходимоедляобеспечения нормальнойжизнедеятельностив условияхотносительногофизическогопсихического покоя. Этаэнергиярасходуетсянапроцессыклеточногометаболизма, кровообращение, дыхание, выделение, поддержаниет мпературытела, функционированиежизненноважных нервныхцентровмозга, постояннуюсекрециюэндокринныхжелёз.
•
Печеньпотребляет27%энергииосновногообмена;
•
Мозг— 19%;
•
Мышцы— 18%;
•
Почки— 10%;
•
Сердце— 7%;
•
Остальныеорганыи ткани— 19%.
Любаяработа —физическаяилиумственная, такжеприёмпищи, колебаниятемпературы окружающейсредыи другиевнешниеиливнутреннефакторы, изменяющиеуровень обменныхпроцессов, лекутзасобойувеличениеэнергозатрат.
Основнойобменопределяют в строгоконтролируемых, искусственноздаваемых условиях:
•
7

утром, натощак(через12–14часовпослепоследнегоприемапищи);
•
в положениилежанаспине, приполномрасслаблениимышц, в состоянииспокойного бодствования;
•
в условияхтемпературногокомфорта(18–20С°);
•
за3сутокдоисследованиязорганизмаисключаютбелковуюпищу;
Основнойобменвыражаетсяколичествомэнергозатратизрасчета1ккална1кгмассытелав час[1ккал/(кг×ч)]
Факторывлияющиенавеличинуосновногообмена:
•
возраст;
•
рост;
•
массатела;
•
полчеловека.
Самыйинтенсивныйосновнойобменотмечаетсяу детей(у новорожденных– 53ккал/кгв сутки, у детейпервогогодажизни– 42ккал/кгв сутки).
Средниевеличиныосновногообменау взрослыхздоровыхмужчинсоставляют1300–1600 ккал/сут, у женщинэтивеличинына10%ниже. Этосвязано тем, чтоу женщинменьше массаи поверхностьела.
Свозрастомвеличинаосновногообменанеуклонноснижается. Средняявеличинаосновного обменау здоровогочеловекаприблизительно1ккал/(кг×ч).
2)Понятиеметодахизмерениятеплопродукцииорганизма.
Дляизмеренияколичестватепла, выделяемогоорганизмом, существуютдваметода: прямаяи непрямаякалориметрия.
Вметоде прямойкалориметрии используются физическиекалориметры,
8

сконструированныетакимобразом, чтов нихможнопомещатьживотныхиличеловека, |
|
||
Первыйкалориметрдляизмеренийналюдяхбылв началеХХвекасозданВ.В.Пашутинымв |
|
||
Военно-Медицинскойакадемии. Наэтомприборебыливыполненыважныеисследования |
|
||
биоэнергетикив нормеи патологии. Методпрямойкалориметриидаётбогатуюи точную |
|
||
информацию, ноонтрудоёмоки требуетприменениясложнойдорогостоящейаппаратуры. |
|
||
Поэтомугораздочащеиспользуют |
непрямуюкалориметрию . Вэтомметоде собирают |
|
|
воздух, выдыхаемыйчеловекомзаопределённоевремя, и |
измеряютв нёмсодержаниеО |
2 и |
|
СО2. Поэтимданнымс помощьюспециальныхтаблицопределяюттеплопродукцию.
Непрямаякалориметриянамногопроще; важнотакже, чтоеёможноприменятьнетольков специальнойлаборатории, в любыхусловиях(у постелибольного, наобъектахвоенной техники т.п.),ноточностьеёзаметнониже.
Вопрос№6
1)Понятиеэнтропии.
ЭНТРОПИЯ, ф-циясостоянияSтермодинамич. системы, изменениек-ройdSдля бесконечномалогобратимогоизменениясостояниясистемыравноотношениюколватеплотыполученногосистемойв этомпроцессе(илиотнятоготсистемы), к абс. т- реТ:
2)Энтропиякакмерасвязаннойэнергии.
Связаннаяэнергия-тачастьвнутреннейэнергии, которуюнельзяиспользоватьдля совершенияработы. Порядупричиноказалосьудобнеевместосвязанной
энергииввестидругуювеличину, котораяназывается |
энтропия и выражаетсяформулой: |
|
||
|
S=WСВЯЗ/T |
(16) |
|
|
тоесть энтропияS –этовеличинасвязаннойэнергии, приходящаясянаединицутемпературы |
|
|||
(пошкалеКельвина).Размерностьэнтропии–Дж |
.К –1. Очевидно, что WСВЯЗ = T.S, и |
U = |
||
G + WСВЯЗ = G + T·S, откудаполучаемсвязьмеждусвободнойэнергиейэнтропией: |
G = U |
|||
– T· S |
(17). |
|
|
|
Почтивсегдаприизученииконкретныхпроцессовнасинтересуетнестолькосамаэнергия, |
|
|
||
сколькоеёизменение. Вбиологическойтермодинамикемычащевсегоимеемделос |
|
|
||
изотермическимипроцессами(температурателапостоянна).Вэтомслучае: |
G = U – T·S |
|||
(18). |
|
|
|
|
3)Вычисленизмененияэнтропиичерезколичествотепла, переданноев процессе. |
|
|
||
Рассмотримсначалаизотермическиепроцессы, наиболеехарактерныедляорганизма. Если |
|
|
||
изменениеэнтропииприпереходеизсостояния1 в состояние2 обозначить |
S 1→2 ,то |
|
||
∆S=Q/T |
(19) |
|
|
|
9
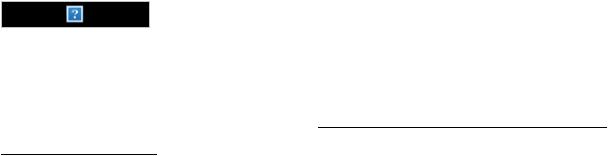
где Q1→2 - этоколичествотепла, полученногосистемойв ходе |
обратимого переходаиз |
||
первогосостояниявовторое. |
|
|
|
Например, приплавлении1кгльдапри0 |
0С в условиях, когданетпотерьтепла(и, значит, |
||
можнопроцессчитатьобратимым),надосообщитьльду335кДж(этавеличинаназывается |
|||
удельнойтеплотойплавления).Поэтомув данномпроцессеизменениеэнтропиильдаравно |
|||
,тоестьпри0 |
0С (273К) энтропия1кгводына 1,23кДж/Кбольше, |
||
чемэнтропияльда. |
|
|
|
4)Второеначалотермодинамикидляизолированныхсистем. |
|
||
Изолированными называютсистемы, которые |
необмениваютсокружающейясредойни |
||
веществом, ниэнергией . Абсолютноизолированныхсистемнебывает, новомногихслучаях
(например, длявеществахорошемтермосе) можнопрактическисчитатьсистему
изолированной.
Визолированнойсистемеобщееизменениеэнтропиивсегдаположительно |
(тоесть |
общаяэнтропияизолированнойсистемывсегдавозрастает).
Здесьважнонеопуститьслово„общее“.Вкакой-точастисистемыэнтропияможет уменьшиться, ноэтообязательнодолжнобытьскомпенсированоувеличениемэнтропиив другихчастяхсистемы.
Изформулы(18): |
G = U – T·S |
видно, чтоеслиэнтропиявозрастает( |
S > 0 ), то |
|
свободнаяэнергиясистемыуменьшается ( |
G < 0 ). Поэтомувтороеначаломожно |
|||
сформулироватьпо-другому: |
Визолированнойсистемеобщееизменениесвободной |
|
||
энергиивсегдаотрицательно |
(тоестьсвободнаяэнергияизолированнойсистемывсегда |
|
||
уменьшается) . |
|
|
|
|
Этаформулировкаболеенаглядна. Мызнаем, чтововсехреальныхпроцессахпроисходит диссипациясвободнойэнергии, тоестьчастьсвободнойэнергиипревращаетсясвязанную
(преимущественнотепловую).Еслисистемаизолированная, тоизвнесвободнаяэнергияне поступает, поэтомуобщийзапассвободнойэнергиисистемыдолженуменьшаться.
Второеначалотермодинамикив приведеннойформулировкеимееточеньбольшое практическоезначение, потомучтоонопозволяетточноустановить, какомнаправлении будетпроисходитьотилиинойпроцесс. Например, еслимыустановимприрасчёте, чтопри некоторомпроцессеобщаясвободнаяэнергияизолированнойсистемыдолжнаувеличиваться,
можнокатегорическиутверждать, чтотакойпроцессневозможен.
10
