
- •Министерство образования и науки Российской Федерации
- •Введение
- •Строение атома
- •Ядро и электронная оболочка атома
- •1.2. Строение ядра атома
- •Нуклиды, изотопы, массовое число
- •Строение электронной оболочки атома. Энергетические уровни
- •2. Квантово - механическое объяснение строения атома
- •2.1. Орбитальная модель атома
- •2.2. Орбитали с s, p , d - и f -электронами (атомные s, p , d - и f -орбитали)
- •2.3. Энергетические подуровни
- •3. Периодический закон и Периодическая система элементов
- •4. Химические соединения
- •5. Практическая часть
- •Энергетические уровни, подуровни и орбитали многоэлектронного атома
- •Задача №3
- •Задача №4 Какие величины квантовых чисел характеризуют состояние валентных электронов в атоме Eu?
- •Задача №9
- •Задача №10
- •Задача №11
- •Задача №12
- •Задача №13
- •Задача №14
- •Индивидуальные задания
- •5.1. Характеристика элемента
- •5.2. Характер химической связи
- •Приложение
- •Литература
- •Оглавление
- •Литература……………………………………………………..37
Министерство образования и науки Российской Федерации
Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования
«МАТИ Российский государственный технологический
университет имени К.Э. Циолковского»
Кафедра «Моделирование систем и информационные технологии»
ЭЛЕКТРОННАЯ СТРУКТУРА АТОМОВ
И
ПЕРИОДИЧЕСКАЯ СИСТЕМА ЭЛЕМЕНТОВ
Методические указания к практическим занятиям
по дисциплине «ХИМИЯ»
Составители:
Белова С.Б.
Белов С.П.
Гришина Н.Д.
МОСКВА 2011
Электронная структура атомов и периодическая система элементов: Методические указания к практическим занятиям по дисциплине «Химия» / сост. С.Б.Белова, С.П.Белов, .Д.Гришина ─ М.: МАТИ, 2011 ─ 40 с.
© Белова С.Б.,
Белов С.П.
Гришина Н.Д.
составление, 2011
© МАТИ, 2011
Введение
Для понимания химического характера того или иного вещества необходимо знание об электронном строении атомов, его образующих. Согласно Периодическому закону, свойства элементов и образуемых ими соединений определяются зарядом ядер их атомов. Расположение химических элементов в Периодической системе соответствует электронному строению их атомов.
Данные методические указания предназначены для изучения электронного строения атомов и приобретения навыков определения свойств элементов по их расположению в Периодической системе элементов.
Строение атома
рассматривая вопрос об электронном строении атомов, необходимо различать свободные атомы, под которыми понимают атомы настолько удаленные друг от друга, что не взаимодействуют между собой, и атомы в твердых телах, которые взаимодействуют между собой, образуя химические связи. Для того, чтобы понять характер их взаимодействия, необходимо первоначально остановиться на электроном строении свободных атомов.
Ядро и электронная оболочка атома
Каждый атом состоит из ядра и электронной оболочки (рис.1). Электронная оболочка атома – это совокупность элементарных частиц – электронов, каждому из которых присущ корпускулярно-волновой характер.
Электрон как частица обладает массой покоя. Me=9,1095·10ˉ31 кг и несет отрицательный электрический заряд, равный 1,6022·10ˉ19 Кл. Абсолютное (без учета знака) значение этого заряда является наименьшим и называется элементарным зарядом.
Атом в целом не заряжен (электрически нейтрален). Это обусловлено тем, что сумма отрицательных зарядов электронов компенсирована положительным зарядом ядра атома: в каждом атоме число элементарных отрицательных зарядов в оболочке равно числу элементарных положительных зарядов в ядре.
Между положительно заряженным ядром атома и отрицательно заряженными электронами его оболочки действуют электростатические (кулоновские) силы притяжения. Геометрический размер атома, условно записываемый диаметром его электронной оболочки, имеет порядок 10ˉ10 м, а диаметр атомного ядра – порядок 10ˉ14 м, т.е по размеру ядро в 10000 меньше, чем атом. Отсюда следует, что:
масса атома сосредоточена в его ядре.
В легчайшем атоме водорода (имеется в виду атом одного из изотопов водорода – протия, ядро которого состоит из одного протона) ядро обладает массой 1,6726·10ˉ27 кг; электрон легче ядра в 1836 раз (фактически речь идет о сравнении масс электрона и протона).
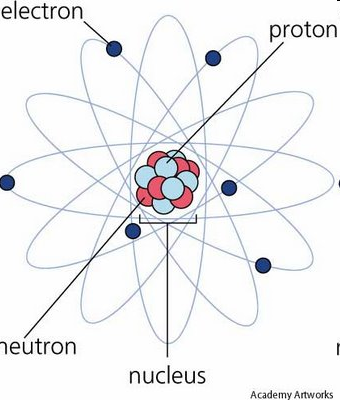
Рис. 1 Ядро и электронная оболочка
