
OVR
.pdf41
Задание 13
Составьте уравнение реакции, протекающей в водном растворе между перманганатом калия и нитритом калия в присутствии серной кислоты. Определите, протекает ли самопроизвольно данная реакция в стандартных условиях.
Алгоритм |
|
Результат |
|
||
1) Записываем реагенты в мо- |
1) KMnO4 + KNO2 + H2SO4 |
||||
лекулярном виде. |
2) K+ + MnO4– |
+ K+ + NO2– + |
|||
2) Записываем реагенты в ион- |
|||||
ном виде. KMnO4, KNO2 – |
+ 2Н+ + SO4 2– |
|
|
|
|
растворимые соли, в водном |
|
|
|
|
|
растворе находятся в виде ио- |
|
|
|
|
|
нов, H2SO4 – водном растворе |
|
|
|
|
|
сильная кислота, также образу- |
|
|
|
|
|
ет ионы |
3) MnO4- + NO2– + 2Н+ = |
|
|||
3) Определяем функции ве- |
|
||||
ществ (окислитель, восстано- |
|
|
|
|
|
витель), среду реакции. Запи- |
|
|
|
|
|
сываем ионы, участвующие в |
|
|
|
|
|
реакции. MnO4- Ок за счет |
|
|
|
|
|
Mn+VII ;NO2– – Вс за счет N+III. |
|
|
|
|
|
Среда кислотная. |
|
|
2+ |
|
|
4) Начинаем составлять полу- |
|
|
|
||
реакцию для окислителя. Нахо- |
4)MnO4 |
Mn |
|
|
|
дим Вф MnO4- в кислотной сре- |
|
|
|
|
|
де – это Mn2+ (Mn+VII Mn+II ). |
5) MnO4 + 8Н+ Mn2+ + 4Н2О |
||||
5) Уравниваем число атомов |
|||||
слева и справа. Число атомов |
|
|
|
|
|
Mn одинаково. Слева 4 атома |
|
|
|
|
|
О, а справа 0, поэтому учиты- |
|
|
|
|
|
вая среду реакции, в левую |
|
|
|
|
|
часть добавляем 8Н+, а в пра- |
|
|
|
|
|
вую – 4Н2О. |
|
|
+ |
|
2+ |
6) Уравниваем суммарные за- |
|
||||
6) MnO4 |
+ 8Н + 5е Mn + |
||||
42
ряды справа и слева. Слева |
+ 4Н2О |
|
|
|
|
сумма зарядов равна –1 + 8(+1) |
|
|
|
|
|
= +7. Справа сумма зарядов |
|
|
|
|
|
равна +2 + 0 = +2. Нужно слева |
|
|
|
|
|
прибавить 5е . Получили по- |
|
|
|
|
|
луреакцию для окислителя. |
7) NO2– NO3– |
|
|
||
7) Начинаем составлять полу- |
|
|
|||
реакцию для восстановителя. |
|
|
|
|
|
Определяем Оф восстановите- |
|
|
|
|
|
ля. Оф для NO2– будет NO3– |
|
|
|
|
|
(N+III N+V). |
8) NO2– + H2O NO3– + 2Н+ |
||||
8) Уравниваем число атомов |
|||||
слева и справа. Слева и справа |
|
|
|
|
|
одинаково число атомов N. |
|
|
|
|
|
Слева 2 атома О, а справа их 3, |
|
|
|
|
|
поэтому учитывая среду реак- |
|
|
|
|
|
ции справа добавляем 2Н+ , а |
|
|
|
|
|
слева 1 молекулу H2O. |
9) NO2– + H2O 2е NO3– + |
||||
9) Уравниваем сумму зарядов |
|||||
слева и справа. Слева сумма |
+ 2Н+ |
|
|
|
|
зарядов 1 + 0 = 1, справа 1+ |
|
|
|
|
|
+2(+1) = +1; поэтому из левой |
|
|
|
|
|
части вычитаем 2е . Получили |
|
|
|
|
|
полуреакцию для восстанови- |
|
|
|
|
|
теля. |
|
|
+ |
|
|
10) Уравниваем число принятых |
+ 8Н |
||||
10) 2 MnO4 |
+ 5е |
||||
и отданных электронов в ОВР. |
Mn2+ + 4Н2О |
|
|||
Находим дополнительные мно- |
5 NO2– + H2O 2е |
|
|||
жителидля каждойполуреакции. |
NO3– + 2Н+ |
|
|
||
11) Составляем ионное уравне- |
11) 2MnO4 +16Н+ + 5NO2– + |
||||
ние ОВР. Суммируем левые и |
+ 5H2O = 2Mn2+ + 8Н2О + |
||||
правые части полуреакций с уче- |
+ 5NO3– + 10Н+ |
|
|
||
том коэффициентов. Сокращаем |
2MnO4 + 6Н+ + 5NO2– = |
||||
подобныечленыв уравнении. |
= 2Mn2+ + 3Н2О + 5NO3– |
||||
12) Составляем уравнение ОВР |
12) 2КMnO4+ 5КNO2 + 3H2SO4 = |
||||
www.mitht.ru/e-library
43
в молекулярном виде. Исполь- |
= 2MnSO4 + 5КNO3 + К2SO4 + |
||||||
зуем ионное уравнение (п.11) и |
+ 3Н2О |
||||||
запись реагентов в молекуляр- |
|
|
|
||||
ном виде (1). |
|
|
13) MnO4 /Mn2+ |
||||
13) |
Определяем |
направление |
|||||
протекания реакции. Составля- |
|
|
|
||||
ем сопряженную Оф/Вф для |
|
|
|
||||
окислителя. |
|
|
|
о |
|
||
14) |
Выписываем |
стандартный |
14) |
= 1,24 В |
|||
|
|||||||
потенциал для Ок в кислотной |
|
|
|
||||
среде. |
|
|
15) NO3 /NO2 |
||||
15) |
Составляем |
сопряженную |
|||||
пару Оф/Вф для восстановите- |
|
|
|
||||
ля. |
|
|
|
|
о |
|
|
16) |
Выписываем |
стандартный |
16) |
= 0,838 В |
|||
|
|||||||
потенциал сопряженной пары |
|
|
|
||||
для восстановителя в кислот- |
|
|
|
||||
ной среде. |
|
|
17) о = оок овс = |
||||
17) |
Находим |
разность между |
|||||
стандартным |
потенциалом Ок |
= 1,24 0,84 = 0,402 В |
|||||
и |
стандартным |
потенциалом |
|
|
|
||
Вс. |
|
|
|
|
|
|
|
18) |
Делаем вывод о протека- |
18) 0,402 В 0,4 В реакция |
|||||
нии ОВР в стандартных усло- |
идет в прямом направлении в |
||||||
виях. |
|
|
стандартных условиях. |
||||
44
Задание 14
Составьте уравнение реакции взаимодействия алюминия с водным раствором гидроксида натрия. Определите, протекает ли самопроизвольно данная реакция в стандартных условиях.
Алгоритм |
Результат |
|
1) Записываем реагенты в мо- |
1) AI + H2O + NaOH |
|
лекулярном виде. |
|
2) AI + H2O + Na+ + OH– |
2) Записываем реагенты в ион- |
||
ном виде. NaOH хорошо рас- |
|
|
творимое сильное |
основание, |
|
находится в растворе в виде |
|
|
ионов; H2O преимуществен- |
|
|
но в виде молекул. |
|
3) AI + H2O + OH– = |
3) Определяем функции ве- |
||
ществ (окислитель, восстано- |
|
|
витель), среду реакции. Запи- |
|
|
сываем ионы, участвующие в |
|
|
реакции. H2O Ок за счет Н+; |
|
|
AI – Вс. Среда щелочная. |
|
|
4) Начинаем составлять полу- |
4) H2O Н2 |
|
реакцию для окислителя. На- |
|
|
ходим Вф H2O это Н2. |
5) Н2О + Н2О Н2 + 2ОН |
|
5) Уравниваем число атомов |
||
слева и справа. Число атомов |
2Н2О Н2 + 2ОН |
|
одинаково. Слева 1 атом О, а |
|
|
справа их нет, поэтому учиты- |
|
|
вая среду реакции, |
в левую |
|
часть добавляем Н2О, а в правую – 2ОН .
www.mitht.ru/e-library
45
6) Уравниваем суммарные за- |
6) 2Н2О + 2е Н2 + 2ОН |
|
|||||||
ряды справа и слева. Слева |
|
|
|
|
|
|
|||
сумма зарядов равна 0. Справа |
|
|
|
|
|
|
|||
сумма зарядов равна 0 + 2(–1) |
|
|
|
|
|
|
|||
= –2. Нужно слева прибавить |
|
|
|
|
|
|
|||
2е . Получили полуреакцию |
|
|
|
|
|
|
|||
для окислителя. |
|
|
|
|
|
|
|
|
|
7) Начинаем составлять полу- |
|
|
|
|
|
||||
7) AI AI(ОН)4 |
|
||||||||
реакцию для восстановителя. |
|
|
|
|
|
|
|||
Определяем Оф восстановите- |
|
|
|
|
|
|
|||
ля. Оф для AI в щелочной сре- |
|
|
|
|
|
|
|||
де |
|
(AI |
о |
|
|
|
|
|
|
будет AI(ОН)4 |
|
|
|
|
|
|
|
||
AI+III ). |
|
|
|
|
|
|
|
||
8) |
Уравниваем число |
атомов |
|
|
|
||||
8) AI + 4ОН AI(ОН)4 |
|
||||||||
слева и справа. Слева и справа |
|
|
|
|
|
|
|||
1 атом АI. Справа есть 4 атома |
|
|
|
|
|
|
|||
О и 4 атома Н (4ОН ), слева их |
|
|
|
|
|
|
|||
нет; учитывая среду реакции, |
|
|
|
|
|
|
|||
добавляем в левую часть 4 ОН |
|
|
|
|
|
|
|||
9) |
Уравниваем сумму зарядов |
9) AI + 4ОН |
|
|
|
||||
|
3е |
|
|||||||
слева и справа. Слева сумма |
|
|
|
|
|
|
|||
AI(ОН)4 |
|
|
|
||||||
равна 0 + 4( 1) = 4, справа 1; |
|
|
|
|
|
|
|||
поэтому из левой части вычи- |
|
|
|
|
|
|
|||
таем 3е . Получили полуреак- |
|
|
|
|
|
|
|||
цию для восстановителя. |
|
|
|
|
|
|
|||
10) |
Уравниваем число приня- |
|
|
|
|||||
10) 32Н2О + 2е Н2 + 2ОН |
|
||||||||
тых и отданных электронов в |
2 AI + 4ОН |
|
|
|
|||||
|
3е |
|
|||||||
ОВР. Находим дополнитель- |
|
|
|
|
|
|
|||
AI(ОН)4 |
|
|
|||||||
ные множители для каждой |
|
|
|
|
|
|
|||
полуреакции. |
|
|
11) 6Н2О + 2AI + 8ОН = |
|
|||||
11) Составляем ионное уравне- |
|
||||||||
ние ОВР. Суммируем левые и |
= 3Н2 + 6ОН |
|
|
|
|
|
|||
|
+ 2 AI(ОН)4 |
|
|||||||
правые части полуреакций с уче- |
6Н2О + 2AI + 2ОН = |
|
|||||||
том коэффициентов. Сокращаем |
=3Н2 + 2 AI(ОН)4 |
|
|||||||
|
|
|
|
|
|
|
|
|
|
подобныечленыв уравнении.
46
12) Составляем уравнение ОВР |
12) 6Н2О + 2AI + 2NaОН = |
||||||
в молекулярном виде. Исполь- |
= 3Н2 + 2Na AI(ОН)4 |
||||||
зуем ионное уравнение (п.11) и |
|
|
|
||||
запись реагентов в молекуляр- |
|
|
|
||||
ном виде (1). |
|
|
|
|
|
||
13) |
Определяем |
направление |
13) Н2О/ Н2 |
||||
протекания реакции. Составля- |
|
|
|
||||
ем сопряженную Оф/Вф для |
|
|
|
||||
окислителя. |
|
|
|
о |
|
||
14) |
Выписываем |
стандартный |
14) |
= 0,83 В |
|||
|
|||||||
потенциал для Ок в щелочной |
|
|
|
||||
среде. |
|
|
|
|
|
||
15) |
Составляем |
сопряженную |
|
|
|||
15) AI(ОН)4 /AI |
|||||||
пару Оф/Вф для восстановите- |
|
|
|
||||
ля. |
|
|
|
|
о |
|
|
16) |
Выписываем |
стандартный |
16) |
= 2,34 В |
|||
|
|||||||
потенциал сопряженной пары |
|
|
|
||||
для восстановителя в щелоч- |
|
|
|
||||
ной среде. |
|
|
17) о = оок овс = |
||||
17) |
Находим |
разность между |
|||||
стандартным |
потенциалом Ок |
= 0,83 ( 2,34) = 1,51 В |
|||||
и |
стандартным |
потенциалом |
|
|
|
||
Вс. |
|
|
|
|
|
|
|
18) |
Делаем вывод о протека- |
18) 1,51 В 0,4 В реакция идет |
|||||
нии ОВР в стандартных усло- |
в прямом направлении в стан- |
||||||
виях. |
|
|
дартных условиях. |
||||
www.mitht.ru/e-library
47
Задание 15
Составьте уравнение реакции, протекающей в водном растворе между избытком хлорной воды и иодидом калия. Определите, протекает ли самопроизвольно данная реакция в стандартных условиях.
|
Алгоритм |
|
|
Результат |
|||
1) |
Записываем реагенты в мо- |
1) |
CI2(изб) + KI |
|
|||
лекулярном виде. |
|
|
CI2(изб) + K+ + I– = |
||||
2) Записываем реагенты в ион- |
2) |
||||||
ном виде. KI –растворимая |
|
|
|
||||
соль, CI2 – в водном растворе |
|
|
|
||||
существует в виде молекул. |
|
CI2(изб) + I– = |
|
||||
3) |
Определяем |
функции ве- |
3) |
|
|||
ществ (окислитель, восстано- |
|
|
|
||||
витель), среду реакции. Запи- |
|
|
|
||||
сываем ионы, участвующие в |
|
|
|
||||
реакции. CI2 Ок за счет CIо;I– |
|
|
|
||||
– Вс. Среда нейтральная. |
|
CI2 CI |
|
||||
4) |
Начинаем составлять полу- |
4) |
|
||||
реакцию для окислителя. На- |
|
|
|
||||
ходим Вф CI2 – это CI |
(CIо |
|
|
|
|||
CI ). |
|
|
|
CI2 2CI |
|
||
5) |
Уравниваем |
число |
атомов |
5) |
|
||
слева и справа. Слева 2 атома |
|
|
|
||||
CI, а справа – 1. Умножаем |
|
|
|
||||
правую часть уравнения на 2. |
|
|
|
||||
6) |
Уравниваем суммарные за- |
6) |
|||||
CI2 + 2е 2CI |
|
||||||
ряды справа и слева. Слева сумма зарядов равна 0. Справа сумма зарядов равна 2(–1) = –2. Нужно слева прибавить 2е . Получили полуреакцию для окислителя.
48
7) Начинаем составлять полу- |
|
|
|||
7) I IО3 |
|
||||
реакцию для |
восстановителя. |
|
|
||
Определяем Оф восстановите- |
|
|
|||
ля. Оф для I |
|
|
|
|
|
|
будет IО3 |
;(I |
|
|
|
I+V ). |
|
|
|
8) I + 3H2O IО3 + 6H+ |
|
8) Уравниваем число атомов |
|||||
слева и справа. Справа 3 атома |
|
|
|||
О, слева их нет. ; поэтому, учи- |
|
|
|||
тывая среду |
|
реакции справа |
|
|
|
добавляем 6Н+, а слева 3H2O .
9) Уравниваем сумму зарядов |
9) I |
|
|
|
|
|
|
|
+ |
|
+ 3H2O 6е IО3 |
|
+ 6H |
||||||
слева и справа. Слева сумма |
|
|
|
|
|
|
|
|
|
равна 1 + 0 = 1, справа 1 +6 |
|
|
|
|
|
|
|
|
|
= +5 поэтому из левой части |
|
|
|
|
|
|
|
|
|
вычитаем 6е . Получили полу- |
|
|
|
|
|
|
|
|
|
реакцию для восстановителя. |
|
|
|
|
|
|
|
|
|
10) Уравниваем число приня- |
|
|
|
|
2CI |
|
|
||
10) 3 CI2 + 2е |
|
|
|
||||||
тых и отданных электронов в |
|
1 I |
|
|
|
|
|
|
|
|
|
+ 3H2O 6е |
|
|
|||||
ОВР. Находим дополнитель- |
|
IО3 + 6H+ |
|
|
|
||||
ные множители для каждой |
|
|
|
|
|
|
|
|
|
полуреакции. |
11) 3CI2 + I + 3H2O = |
|
|
||||||
11) Составляем ионное урав- |
|
|
|||||||
нение ОВР. Суммируем левые |
|
= 6СI + IО3 + 6H+ |
|
|
|||||
и правые части полуреакций с |
|
|
|
|
|
|
|
|
|
учетом коэффициентов. Со- |
|
|
|
|
|
|
|
|
|
кращаем подобные члены в |
|
|
|
|
|
|
|
|
|
уравнении. |
|
|
|
|
|
|
|
|
|
12) Составляем уравнение ОВР |
12) 3CI2 + КI+ 3H2O = |
|
|
||||||
в молекулярном виде. Исполь- |
|
= 6НСI + КIО3 |
|
|
|
||||
зуем ионное уравнение (п.11) и |
|
|
|
|
|
|
|
|
|
запись реагентов в молекуляр- |
|
|
|
|
|
|
|
|
|
ном виде (1). |
13) CI2/CI |
|
|
|
|
||||
13) Определяем направление |
|
|
|
|
|||||
протекания реакции. Составля- |
|
|
|
|
|
|
|
|
|
ем сопряженную Оф/Вф для |
|
|
|
|
|
|
|
|
|
окислителя. |
|
|
|
|
|
|
|
|
|
www.mitht.ru/e-library
49
14) |
Выписываем |
стандартный |
14) |
|
о |
=1,40 В |
||
|
||||||||
потенциал для Ок в нейтраль- |
|
|
|
|
||||
ной среде. |
|
|
|
IО3 /I |
||||
15) |
Составляем |
сопряженную |
15) |
|||||
пару Оф/Вф для восстановите- |
|
|
|
|
||||
ля. |
|
|
|
|
|
о |
|
|
16) |
Выписываем |
стандартный |
16) |
|
= 1,08 В |
|||
|
||||||||
потенциал сопряженной пары |
|
|
|
|
||||
для восстановителя кислотной |
|
|
|
|
||||
среде. |
|
|
|
о = оок овс = |
||||
17) |
Находим |
разность между |
17) |
|||||
стандартным |
потенциалом Ок |
= 1,40 1,08 = 0,32 В |
||||||
и |
стандартным |
потенциалом |
|
|
|
|
||
Вс. |
|
|
|
|
|
|
|
|
18) |
Делаем вывод о протека- |
18) |
0,32 В 0,4 В реакция не |
|||||
нии ОВР в стандартных усло- |
идет в прямом направлении в |
|||||||
виях. |
|
|
стандартных условиях. |
|||||
50
Задание 16
Составьте уравнение реакции, протекающей между гипохлоритом кальция (т) и концентрированным раствором хлороводородной кислоты . Определите, протекает ли самопроизвольно данная реакция в стандартных условиях.
Алгоритм |
Результат |
1) Записываем реагенты в мо- |
1) Ca(CIO)2(т) + HCI(конц) |
лекулярном виде. |
2) Ca(CIO)2 + H+ + CI = |
2) Записываем реагенты в ион- |
|
ном виде. HCI в водном рас- |
|
творе образует ионы; Ca(CIO)2 |
|
твердое вещество, участвует |
|
в реакции в виде молекул. |
3) Ca(CIO)2 + CI = |
3) Определяем функции ве- |
|
ществ (окислитель, восстано- |
|
витель), среду реакции. Запи- |
|
сываем ионы, участвующие в |
|
реакции. Ca(CIO)2 Ок за счет |
|
CI+I ; CI– Вс. Среда кислот- |
|
ная. |
4) Ca(CIO)2 Ca2+ + CI2 |
4) Начинаем составлять полу– |
|
реакцию для окислителя. На- |
|
ходим Вф Ca(CIO)2 это CI2 |
|
(CI+I CIо). |
5) Ca(CIO)2 + 4Н+ Ca2+ + |
5) Уравниваем число атомов |
|
слева и справа. Число атомов |
+ CI2 + 2Н2О |
Са одинаково. Слева 2 атома О |
|
и 2 атома CI а справа только 2 |
|
атома CI, поэтому учитывая |
|
среду реакции, в левую часть |
|
добавляем 4Н+, а в правую – |
|
2Н2О. |
|
www.mitht.ru/e-library
51
6) Уравниваем суммарные за- |
6) Ca(CIO)2 + 4Н+ + 2е |
|||||||||
ряды справа и слева. Слева |
Ca2+ + CI2 +2Н2О |
|||||||||
сумма зарядов равна 4(+1) = |
|
|
|
|
|
|||||
+4. Справа сумма зарядов рав- |
|
|
|
|
|
|||||
на +2 + 0 = +2. Нужно слева |
|
|
|
|
|
|||||
прибавить 2е . Получили по- |
|
|
|
|
|
|||||
луреакцию для окислителя. |
7) CI CI2 |
|||||||||
7) Начинаем составлять полуре- |
||||||||||
акцию для восстановителя. Оп- |
|
|
|
|
|
|||||
ределяем |
Оф восстановителя. |
|
|
|
|
|
||||
Оф для |
|
|
CI2; |
|
|
|
|
|
|
|
CI будет |
(CI |
|
|
|
|
|
||||
CIо). |
|
|
|
|
|
8) 2CI CI2 |
||||
8) Уравниваем |
число |
атомов |
||||||||
слева и справа. Слева 1 атом |
|
|
|
|
|
|||||
CI, справа 2, поэтому левую |
|
|
|
|
|
|||||
часть |
полуреакции |
умножаем |
|
|
|
|
|
|||
на 2. |
|
|
|
|
|
|
|
|
|
|
9) Уравниваем сумму зарядов |
9) 2CI |
|
|
|||||||
|
2е CI2 |
|||||||||
слева и справа. Слева сумма |
|
|
|
|
|
|||||
равна 2, справа 0 ,поэтому из |
|
|
|
|
|
|||||
левой части вычитаем 2е . По- |
|
|
|
|
|
|||||
лучили полуреакцию для вос- |
|
|
|
|
|
|||||
становителя. |
|
|
|
10) 1 Ca(CIO)2 + 4Н+ + 2е |
||||||
10) Уравниваем число приня- |
||||||||||
тых и отданных электронов в |
Ca2+ + CI2 +2Н2О |
|||||||||
ОВР. |
Находим |
дополнитель- |
1 2CI |
|
2е CI2 |
|||||
|
|
|
|
|
|
|
|
|
|
|
ные |
множители |
для |
каждой |
|
|
|
|
|
||
полуреакции. |
|
|
|
11) Ca(CIO)2 + 4Н+ + 2CI = |
||||||
11) Составляем ионное урав- |
||||||||||
нение ОВР. Суммируем левые |
= Ca2+ + CI2 +2 Н2О + CI2 |
|||||||||
и правые части полуреакций с |
Ca(CIO)2 + 4Н+ + 2CI = |
|||||||||
учетом коэффициентов. Со- |
= Ca2+ + 2CI2 + 2Н2О |
|||||||||
кращаем |
подобные |
члены в |
|
|
|
|
|
|||
уравнении.
52
12) Составляем уравнение ОВР |
12) Ca(CIO)2 + 4НCI= |
||||||
в молекулярном виде. Исполь- |
= Ca CI2 + 2CI2 + 2Н2О |
||||||
зуем ионное уравнение (п.11) и |
|
|
|
||||
запись реагентов в молекуляр- |
|
|
|
||||
ном виде (1). |
|
|
13) CIO /CI2 |
||||
13) |
Определяем |
направление |
|||||
протекания реакции. Составля- |
|
|
|
||||
ем сопряженную Оф/Вф для |
|
|
|
||||
окислителя. |
|
|
|
о |
|
||
14) |
Выписываем |
стандартный |
14) |
= 2,14 В |
|||
|
|||||||
потенциал для Ок в кислотной |
|
|
|
||||
среде. |
|
|
15) CI2 /CI |
||||
15) |
Составляем |
сопряженную |
|||||
пару Оф/Вф для восстановите- |
|
|
|
||||
ля. |
|
|
|
|
о |
|
|
16) |
Выписываем |
стандартный |
16) |
= 1,40 В |
|||
|
|||||||
потенциал сопряженной пары |
|
|
|
||||
для восстановителя в ней- |
|
|
|
||||
тральной среде. |
|
17) о = оок овс = |
|||||
17) |
Находим |
разность между |
|||||
стандартным |
потенциалом Ок |
= 2,14 1,40 = 0,74 В |
|||||
и |
стандартным |
потенциалом |
|
|
|
||
Вс. |
|
|
|
|
|
|
|
18) |
Делаем вывод о протека- |
18) 0,74 В 0,4 В реакция идет |
|||||
нии ОВР в стандартных усло- |
в прямом направлении в стан- |
||||||
виях. |
|
|
дартных условиях. |
||||
www.mitht.ru/e-library
53
Задание 17
Составьте уравнение реакции, протекающей при пропускании брома через горячий водном раствор гидроксида натрия. Определите, протекает ли самопроизвольно данная реакция в стандартных условиях.
Алгоритм |
|
Результат |
||
1) Записываем реагенты в мо- |
1) |
Br2 + NaOH |
||
лекулярном виде. |
|
|
|
Br2 + Na+ + OH = |
2) Записываем реагенты в ион- |
2) |
|||
ном виде. Br2 газ, в реакции |
|
|
||
участвует в виде молекул; |
|
|
||
NaOH хорошо растворимое |
|
|
||
сильное основание, |
находится |
|
|
|
в растворе в виде ионов. |
|
Br2 + OH = |
||
3) Определяем функции ве- |
3) |
|||
ществ (окислитель, восстано- |
|
|
||
витель), среду реакции. Запи- |
|
|
||
сываем ионы, участвующие в |
|
|
||
реакции. Br2 Ок за счет Brо; |
|
|
||
Br2 – Вс за счет Br |
о |
Среда ще- |
|
|
|
|
|
||
лочная. |
|
|
|
Br2 Br |
4) Начинаем составлять полу- |
4) |
|||
реакцию для окислителя. На- |
|
|
||
ходим Вф Br2 это Br . |
|
Br2 2Br |
||
5) Уравниваем число атомов |
5) |
|||
слева и справа. Слева 2 атома |
|
|
||
Вr, а справа только 1, поэтому удваиваем число ионов Вr справа.
54
6) Уравниваем суммарные за- |
|
|
|
|
|
|
|
|||||
6) Br2 + 2е 2Br |
|
|
|
|
|
|||||||
ряды справа и слева. Слева |
|
|
|
|
|
|
|
|
||||
сумма зарядов равна 0. Справа |
|
|
|
|
|
|
|
|
||||
сумма зарядов равна –2. Нужно |
|
|
|
|
|
|
|
|
||||
слева прибавить 2е . Получили |
|
|
|
|
|
|
|
|
||||
полуреакцию для окислителя. |
7) Br2 BrО3 |
|
|
|
|
|
|
|
||||
7) Начинаем составлять полуре- |
|
|
|
|
|
|
|
|||||
акцию для восстановителя. Оп- |
|
|
|
|
|
|
|
|
||||
ределяем |
Оф восстановителя. |
|
|
|
|
|
|
|
|
|||
Оф для Br2 будет BrО3 |
(Br0 |
|
|
|
|
|
|
|
|
|||
Br+V). Среда щелочная. |
|
8) Br2 + 12ОН 2BrО3 + |
||||||||||
8) Уравниваем |
число |
атомов |
||||||||||
слева и справа. Слева есть 2 |
+ 6Н2О |
|
|
|
|
|
|
|
||||
атома Br, справа один, уд- |
|
|
|
|
|
|
|
|
||||
ваиваем число ионов BrО3 . |
|
|
|
|
|
|
|
|
||||
Справа есть 6 атомов О, слева |
|
|
|
|
|
|
|
|
||||
их нет; учитывая среду реак- |
|
|
|
|
|
|
|
|
||||
ции, добавляем в левую часть |
|
|
|
|
|
|
|
|
||||
12ОН ,в правую 6Н2О. |
|
|
|
|
|
|
|
|
|
|||
9) Уравниваем сумму зарядов |
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|||||||
слева и справа. Слева сумма |
9) Br2 + 12ОН 10е |
|
|
|
||||||||
2BrО3 + 6Н2О |
|
|
|
|||||||||
равна 0 + 12( 1) |
= 12, справа |
|
|
|
|
|
|
|
|
|||
2( 1) + 0 |
= 2, поэтому из ле- |
|
|
|
|
|
|
|
|
|||
вой части вычитаем 10е . По- |
|
|
|
|
|
|
|
|
||||
лучили полуреакцию для вос- |
|
|
|
|
|
|
|
|
||||
становителя. |
|
|
|
|
|
|
|
|
|
|
||
10) |
Уравниваем число приня- |
|
|
|
|
|
|
|||||
10) 5 Br2 + 2е 2Br |
|
|
||||||||||
тых и отданных электронов в |
1 Br2 + 12ОН |
|
|
|
|
|
||||||
|
|
10е |
||||||||||
ОВР. Находим дополнитель- |
2BrО3 + 6Н2О |
|
|
|||||||||
ные |
множители |
для каждой |
|
|
|
|
|
|
|
|
||
полуреакции.
www.mitht.ru/e-library

55
11) |
Составляем |
ионное урав- |
11) 5Br2 + Br2 + 12ОН = |
|||||
нение ОВР. Суммируем левые |
= 10Br + 2BrО3 + 6Н2О |
|||||||
и правые части полуреакций с |
3Br2 + 6ОН = 5Br + |
|||||||
учетом коэффициентов. Со- |
+ BrО3 + 3Н2О |
|||||||
кращаем |
подобные члены в |
|
|
|
||||
уравнении. |
|
|
12) 3Br2 + 6NaОН = |
|||||
12) Составляем уравнение ОВР |
||||||||
в молекулярном виде. Исполь- |
= 5NaBr+ NaBrО3 + 3Н2О |
|||||||
зуем ионное уравнение (п.11) и |
|
|
|
|||||
запись реагентов в молекуляр- |
|
|
|
|||||
ном виде (1). |
|
|
13) Br2 / Br |
|||||
13) |
Определяем |
направление |
||||||
протекания реакции. Составля- |
|
|
|
|||||
ем сопряженную Оф/Вф для |
|
|
|
|||||
окислителя. |
|
|
|
о |
|
|||
14) |
Выписываем |
стандартный |
14) |
= 1,09 В |
||||
|
||||||||
потенциал для Ок в щелочной |
|
|
|
|||||
среде. |
|
|
|
15) BrО3 / Br2 |
||||
15) |
Составляем |
сопряженную |
||||||
пару Оф/Вф для восстановите- |
|
|
|
|||||
ля. |
|
|
|
|
|
о |
|
|
16) |
Выписываем |
стандартный |
16) |
= 0,52 В |
||||
|
||||||||
потенциал |
сопряженной пары |
|
|
|
||||
для восстановителя в щелоч- |
|
|
|
|||||
ной среде. |
|
|
|
17) о = оок овс = |
||||
17) |
Находим |
разность между |
||||||
стандартным |
потенциалом Ок |
= 1,09 0,52 = 0,47 В |
||||||
и |
стандартным |
потенциалом |
|
|
|
|||
Вс. |
|
|
|
|
|
|
|
|
18) |
Делаем вывод о протека- |
18) 0,47 В > 0,4 В реакция идет |
||||||
нии ОВР в стандартных усло- |
в прямом направлении в стан- |
|||||||
виях. |
|
|
|
дартных условиях. |
||||
56
Приложение 1
Стандартные потенциалы ( о,В) окислительновосстановительных пар (водный раствор, 25 оС)
Формульн. |
Хими- |
|
|
|
единицы в |
ческая |
Оф/Вф |
о,В |
Среда реак- |
исходном |
функ- |
|
|
ции |
растворе |
ция |
Al /Al3+ |
|
|
Al |
Вс |
1,70 |
кислотная |
|
|
Вс |
[Al(OH)4]–/Al |
2,34 |
щелочная |
Br2 |
Ок |
Br2 /Br– |
+1,09 |
кисл., щел. |
|
Вс |
BrO3– /Br2 |
+0,52 |
щелочная |
Cl2 |
Ок |
Cl2 /Cl– |
+1,40 |
кисл., щел. |
ClO– |
Ок |
ClO– /Cl2 |
+2,14 |
кислотная |
[Cr(OH)6]3– |
Вс |
CrO42–/[Cr(OH)6]3– |
0,17 |
щелочная |
Cr2O7 2– |
Ок |
Cr2O7 2–/Cr3+ |
+1,33 |
кислотная |
Fe2+ |
Вс |
Fe3+/Fe2+ |
+0,77 |
кислотная |
H2O |
Ок |
H2O /H2 |
0,83 |
щелочная |
H2O2 |
Ок |
H2O2/OH– |
+0,94 |
щелочная |
|
Ок |
H2O2/H2O |
+1,76 |
кислотная |
|
Вс |
O2/H2O2 |
+0,69 |
кислотная |
H2S |
Вс |
S /H2S |
+0,14 |
кислотная |
I– |
Вс |
I2 /I– |
+0,54 |
кисл., щел. |
|
Вс |
IО3– /I– |
+1,08 |
кислотная |
MnO4– |
Ок |
MnO4–/Mn2+ |
+1,24 |
кислотная |
|
Ок |
MnO4–/MnO2 |
+0,62 |
нейтральная |
|
Ок |
MnO4–/MnO42– |
+0,56 |
щелочная |
NO2– |
Ок |
NO2–/NO |
+1,20 |
кислотная |
|
Вс |
NO3–/NO2– |
+0,838 |
кислотная |
NO3– |
Ок |
NO3–(к)/NO2 |
+0,77 |
кислотная |
|
Ок |
NO3–(p)/NO |
+0,96 |
кислотная |
|
Ок |
NO3–(оч.p)/NH4+ |
+0,88 |
кислотная |
Р |
Вс |
Н3PO4 /P |
0,38 |
кислотная |
PbO2 |
Ок |
PbO2 /Pb2+ |
+1,46 |
кислотная |
SO2 |
Вс |
SO42–/SO2 |
+0,16 |
кислотная |
SO32– |
Вс |
SO42–/SO32– |
0,93 |
щелочная |
|
Вс |
SO42–/SO32– |
0,10 |
кислотная |
SO42–(к) |
Ок |
SO42–/H2S |
+0,31 |
кислотная |
www.mitht.ru/e-library
57 |
58 |
Учебно-методическое пособие
Приложение 2
Кудряшова Зоя Александровна
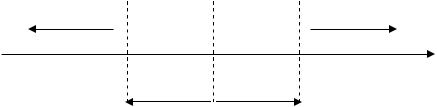
Критерий необратимого протекания ОВР
|
|
равновесие обратимо |
|
|
||
идет |
|
|
|
|
идет |
|
обратная |
|
|
|
|
прямая |
|
0,4 |
|
|
|
|
|
о,В |
|
|
0 |
|
+0,4 |
||
|
преобладает реакция |
|
||||
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
обратная |
прямая |
|
|
|
Приложение 3 |
|
Учебно-методическое пособие |
|
«Правило среды»: |
|||
Окислительно-восстановительные реакции |
|||
1. Кислотная среда: |
[O] + 2H+ = H2O |
||
|
|||
или |
H2O = [O] + 2H+ |
|
|
2. Щелочная среда: |
[O] + H2O = 2ОH– |
|
|
или |
2ОH– = [O] + H2O |
Подписано в печать ___________________ |
|
3. Нейтральная среда: |
[O] + H2O = 2ОH– |
||
Формат 60х90/16 Уч. – изд.л. |
|||
или |
H2O = [O] + 2H+ |
Гарнитура Times New Roman |
|
Тираж _________ экз. Заказ № _________
ИПЦ МИТХТ им. М.В. Ломоносова 117571, Москва, пр. Вернадского,86
www.mitht.ru/e-library
59 |
60 |
www.mitht.ru/e-library
