
Краткий курс органической химии. Часть 2
.pdf
структуры нет. Следовательно, в мета-σ-комплексе стабилизация менее эффективна, и он образуется значительно более медленно. Поэтому главным образом реакция идет через орто- и пара-σ-комплексы и приводит к соответствующим продуктам замещения.
В случае дезактивирующих заместителей, кроме галогенов, ситуация следующая: эти заместители дезактивируют все σ-комплексы, поскольку стягивают электронную плотность с положительно заряженных частиц. Однако в орто-и пара-σ-комплексах это стягивание наиболее ощутимо, т.к. в них эти заместители связаны непосредственно с атомом, на котором в одной из граничных структур локализован положительный заряд. Для мета-σ-комплекса такой граничной структуры нет, поэтому он наименее дестабилизирован электроноакцепторным влиянием и, следовательно, более устойчив, чем орто-
и пара-σ-комплексы. Например, при электрофильном замещении в молекуле нитробензола возникают три σ-комплекса, мезомерные формулы для которых приведены ниже. Из этих формул видно, что электроноакцепторное и,
следовательно, дестабилизирующее влияние нитрогруппы особенно существенно в орто- и пара-σ-комплексах.
1/3 |
NO2 |
|
NO2 |
|
NO2 |
H |
1/ |
1/3 |
1/ |
|
|
|
|
3 |
|
||
|
E |
3 |
H |
|
|
|
|
1/3 |
|
||
1/3 |
1/3 |
|
1/3 |
||
|
E |
||||
орто-σ-комплекс |
|
1/3 |
H |
E |
|
мета-σ-комплекс |
пара-σ-комплекс |
||||
Атомы галогенов, которые являются дезактивирующими заместителями,
ориентируют электрофильное замещение в орто- и пара-положения,
поскольку, дестабилизируя все σ-комплексы, эффективно делокализуют заряд в
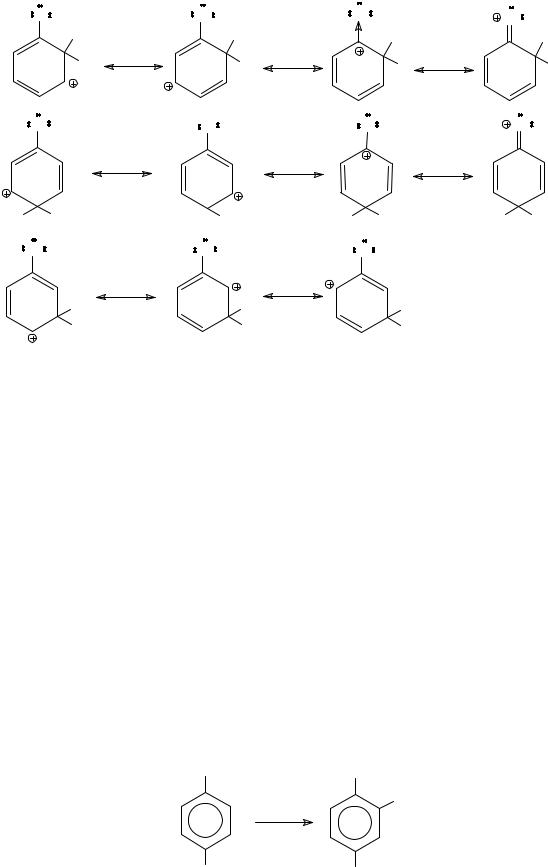
орто- и пара-σ-комплексах за счет +М-эффекта. Так, например, выглядит делокализация заряда в σ-комплексах, образующихся при электрофильном замещении в молекуле хлорбензола:
http://www.mitht.ru/e-library
Cl |
Cl |
Cl |
Cl |
H |
H |
H |
H |
E |
E |
E |
E |
Cl |
Cl |
Cl |
Cl |
E H E H E H E H
H E H E H
Cl |
Cl |
Cl |
только три |
|
|||
|
|
|
граничных структуры |
H |
H |
H |
(нет локализации |
E |
E |
E |
заряда на атоме Cl) |
|
|
|
4.7.3.Ориентация в дизамещенных производных бензола
Вмолекулах дизамещенных производных бензола электрофильное
замещение также является региоселективной реакцией. При этом могут
реализовываться две ситуации:
согласованная ориентация, когда оба заместителя направляют замещение в одно и то же положение. Например, в молекуле пара-нитрофенола гидроксильная группа как сильный электронодонор и, следовательно,
ориентант 1-го рода направляет замещение в орто-положение по отношению к себе, а нитрогруппа как ориентант 2-го рода – в мета-
положение по отношению к себе, т.е. оба заместителя направляют электрофил в одно и то же положение, поэтому при электрофильном хлорировании пара-нитрофенола образуется главным образом 4-нитро-2-
хлорфенол. OH OH
Cl
Cl2
AlCl3
NO2 NO2
несогласованная ориентация, когда два заместителя направляют замещение в разные положения. Например, в молекуле мета-нитрофенола гидроксильная группа и нитрогруппа осуществляют несогласованную
http://www.mitht.ru/e-library

ориентацию: гидроксильная группа хочет направить электрофил к атомам 2, 4 и 6 бензольного кольца, а нитрогруппа –к атому 5. При несогласованной ориентации региоселективность определяет заместитель, являющийся более сильным активатором электрофильного замещения. В
рассматриваемом примере мета-нитрофенола замещение будет направлять гидроксильная группа как активирующий заместитель, поскольку нитрогруппа является дезактивирующим заместителем, поэтому при хлорировании возможно замещение двух орто-положений и одного пара-
положения по отношению к гидроксильной группе. Однако замещение в положение 2 связано с заметными пространственными препятствиями,
поэтому, например, при электрофильном хлорировании мета-нитрфенола образуются в основном 3-нитро-4-хлорфенол и 5-нитро-2-хлорфенол.
|
OH |
|
OH |
OH |
|
6 |
2 |
Cl2 |
|
Cl |
|
+ |
|
||||
5 |
|
AlCl3 |
|
||
NO2 |
NO2 |
NO2 |
|||
|
|||||
|
4 |
|
Cl |
|
|
|
|
|
|
5. Другие реакции бензола и его гомологов
5.1. Свободно-радикальные реакции
а) При взаимодействии бензола с избытком хлора при фотохимическом инициировании происходит присоединение трех эквивалентов хлора с образованием 1,2,3,4,5,6-гексахлорцикло-гексана, или гексахлорана.
|
|
Cl |
|
|
Cl |
|
Cl |
|
|
||
3Cl2 |
|
|
|
h
Cl Cl
Cl
б) Взаимодействие толуола с хлором при фотохимическом возбуждении приводит к замещению атомов водорода в α-положении к ароматическому кольцу на атом хлора.
http://www.mitht.ru/e-library

CH3 Cl2 |
CH2Cl Cl2 |
CHCl2 Cl2 |
CCl3 |
h |
h |
h |
|
бензилхлорид бензилиденхлорид бензотрихлорид
Этот процесс происходит по свободно-радикальному механизму (SR)
через бензильный радикал, который обладает высокой устойчивостью
благодаря резонансной стабилизации.
CH2 |
CH2 |
CH2 |
CH2 |
По этой причине хлорирование на свету любых гомологов бензола,
имеющих в α-положении хотя бы один атом водорода, происходит в бензильное положение боковой цепи. Так, при хлорировании бутилбензола на свету образуется главным образом 1-фенил-1-хлорбутан.
CH2CH2CH2CH3 Cl2 |
CHCH2CH2CH3 |
h |
Cl |
Аналогично хлорированию можно осуществить и α-бромирование боковой цепи при взаимодействии таких аренов с бромом на свету.
5.2. Окисление бензола и его гомологов
Бензол может быть окислен озоном до озонида, формально соответствующего продукту взаимодействия трех двойных связей в формуле Кекуле с тремя молекулами озона. При гидролизе озонида образуются три молекулы глиоксаля (этандиаля).
O
O
3O3 |
O |
O |
H2O |
|
O |
O |
3O=CH CH=O |
|
O |
Zn |
|
|
O |
|
|
|
O |
|
|
|
озонид |
глиоксаль |
|
Гомологи бензола также подвергаются озонолизу с образованием смеси соответствующих продуктов.
http://www.mitht.ru/e-library

Кислородом воздуха на оксиде ванадия в качестве катализатора бензол окисляется до ангидрида малеиновой кислоты (малеинового ангидрида).
|
|
|
|
O |
|
||||||
|
|
|
O2 |
|
|
|
|
O |
малеиновый ангидрид |
||
|
|
|
|
|
|||||||
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
||
|
|
|
V2O5 |
|
|||||||
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
O |
|
||||||
Толуол и другие гомологи бензола при |
взаимодействии с сильными |
||||||||||
окислителями, такими как перманганат калия, окисляются до бензойной |
|
кислоты. |
COOH |
CH3 KMnO4 |
|
5.3. Восстановление бензола и его гомологов
Бензол и его гомологи могут быть восстановлены до циклогексана и его гомологов при гидрировании на платине в достаточно жестких условиях
(высокая температура и давление).
R 3H2 |
R |
Pt |
|
6. Задачи и упражнения
1.Изобразите смещение электронной плотности в следующих молекулах: а)
этилбензол; б) фенол; в) метилфенилкетон; г) метилфениловый эфир; д)
бензойная кислота.
2.Изобразите смещение электронной плотности в следующих молекулах: а)
изопропилбензол; б) бензальдегид; в) анилин; г) бензолсульфокислота; д)
цианобензол.
3.Расположите в ряд по возрастанию скорости реакции с хлором в присутствии трихлорида алюминия следующие соединения: бензол, толуол,
хлорбензол, орто-ксилол. Ответ обоснуйте. Напишите уравнения реакций.
4.Расположите в ряд по возрастанию скорости реакции с концентрированной серной кислотой следующие соединения: бензол, фенол, бензойная кислота,
http://www.mitht.ru/e-library
пара-нитробензойная кислота. Ответ обоснуйте. Напишите уравнения
реакций.
5.Расположите в ряд по возрастанию скорости реакции со смесью концентрированных серной и азотной кислот следующие соединения:
бензол, (трифторметил)бензол, толуол, орто-метилфенол. Ответ обоснуйте.
Напишите уравнения реакций.
6.Изобразите механизмы следующих реакций: а) фенол и серная кислота; б)
изопропилбензол и смесь азотной и серной кислот; в) толуол и хлорангидрид уксусной кислоты в присутствии трихлорида алюминия.
Обоснуйте ориентирующее влияние заместителя в реакции «а».
7.Изобразите механизмы следующих реакций: а) толуол и этилен в присутствии серной кислоты; б) нитробензол и хлор в присутствии трихлорида алюминия; в) бензойная кислота и серный ангидрид. Обоснуйте региоселективность реакции «в».
8.Изобразите механизмы следующих реакций: а) ацетофенон и бром в присутствии трихлорида алюминия; б) бензолсульфокислота и нитрующая смесь; в) фенилэтиловый эфир и серная кислота. Обоснуйте региоселективность реакции «а».
9.Изобразите механизмы следующих реакций: а) этилбензол и хлорангидрид бензойной кислоты; б) бензол и бензиловый спирт в присутствии серной кислоты; в) пара-хлортолуол и бром в присутствии трибромида алюминия.
Обоснуйте региоселективность реакции «а».
10.Из бензола и других необходимых реагентов получите: а) пара-нитротолуол;
б) мета-нитрохлорбензол; в) пара-нитробензойную кислоту.
11.Из бензола и других необходимых реагентов получите: а) пара-трет-
бутилацетофенон; б) мета-нитробензойную кислоту; в) пара-
хлорбензолсульфокислоту.
12.Из бензола и других необходимых реагентов получите: а) пара-
хлорбензилбромид; б) мета-хлорбензолсульфокислоту; в) пара-
толуолсульфокислоту.
http://www.mitht.ru/e-library
13.Напишите уравнения реакций пропилбензола с хлором в разных условиях: а)
в присутствии трихлорида алюминия; б) на свету.
14.Напишите уравнения реакций: а) толуол и озон; б) продукт реакции «а» и
вода; в) изопропилбензол и бром на свету; г) бензол и кислород в присутствии оксида ванадия; д) толуол и избыток водорода на платине.
15.Можно ли по продуктам озонолиза различить такие углеводороды, как: а)
толуол и орто-ксилол; б) орто-ксилол и мета-ксилол? Напишите соответствующие уравнения реакций.
http://www.mitht.ru/e-library
http://www.mitht.ru/e-library
http://www.mitht.ru/e-library
Учебное пособие
Пом ога е в Але кс а ндр Ильич
КРАТКИЙ КУРС
ОРГАНИЧЕСКОЙ ХИМИИ
Часть 2
Углеводороды
Компьютерная верстка: Березовская Ю.В.
Подписано в печать …………………. Формат 60х90/16 Отпечатано на ризографе. Уч.-изд. л.
Бумага писчая. Тираж 120 экз. Заказ №………….. Лицензия на издательскую деятельность
ИД № 03507 от 15.12.2000
119571, Москва, пр. Вернадского, 86 ИПЦ МИТХТ им. М.В. Ломоносова
http://www.mitht.ru/e-library
