
- •6. Арены
- •А.И. Кузнецов
- •Оглавление
- •6. Арены
- •Гексагон энергетические
- •Циклопентадиенил анион катион тропилия
- •6.1.1. Нитрование
- •Не очень неустойчивый
- •6.1.2. Сульфирование
- •6.1.3. Галогенирование
- •6.1.4. Алкилирование
- •6.1.5. Ацилирование
- •Пропионилхлорид пропиофенон
- •Применение реакции Фриделя-Крафтса имеет следующие ограничения:
- •6.2. Алкилбензолы
- •6.2.1. Реакции электрофильного замещения толуола
- •6.3. Реакции электрофильного замещения нафталина
- •6.4. Восстановление по Берчу
- •6.5 Окисление аренов
- •Нафталин фталевый ангидрид фталевая кислота
- •6.6. Стирол
- •Фуллерены и нанотрубки
6.1.1. Нитрование
Нитрование аренов является первой стадией в синтезе большого количества соединений. При действии на бензол концентрированной азотной кислоты, а еще лучше смеси азотной и серной кислот 1:2 (нитрующая смесь) атом водорода бензола замещается на нитрогруппу:
 (4)
(4)
Серная кислота играет роль катализатора, способствующего образованию нитроил-катиона (нитрониевого катиона).
![]()
![]()
нитроний
Механизм
1. Реакция нитрониевого катиона с системой ароматического кольца.

бензол и нитроний катион промежуточный циклогексадиенил катион
2. Потеря протона циклогексадиенил катионом.

циклогексадиенил катион нитробензол гидроний
Нитробензол путем длительного нагревания с использованием концентрированных кислот способен нитроваться до динитробензола, в основном мета.
 (5)
(5)
При присоединении нитрония в о- или п-положение к нитрогруппе возникает очень неустойчивый -комплекс, в то время как в м-положение – не очень неустойчивый:

очень неустойчивый

Не очень неустойчивый
Полинитросоединения сами по себе используются в качестве взрывчатых веществ. Нитрогруппа ароматических нитросоединений далее легко может быть восстановлена в аминогруппу, что дает возможность получать ароматические амины. Гидрированием нитробензола получают анилин.
 (6)
(6)
анилин
Его получают также восстановлением железом или оловом в кислой среде. При этом сначала образуется соль – анилинийхлорид. При действии на него щелочи высвобождается анилин.
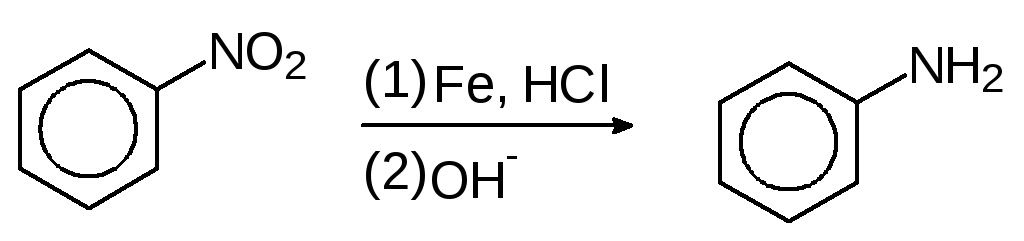 (6а)
(6а)
анилин
Гидрированием м-динитробензола получают м-фенилендиамин.
 (7)
(7)
м-динитробензол м-фенилендиамин
Использование в качестве восстановителя сероводорода позволяет восстанавливать одну из двух нитрогрупп:
 (8)
(8)
м-динитробензол м-нитроанилин
6.1.2. Сульфирование
Сульфирование - реакция электрофильного замещения, в результате которой в ароматическое ядро вводится группа - SO2R, где R = OH, Hal, Ar, R. В качестве сульфирующих агентов чаще всего используют серную кислоту различных концентраций, олеум и хлорсульфоновую кислоту.
Cульфирование бензола можно осуществлять, используя дымящуюся серную кислоту (серная кислота, содержащая триоксид серы):
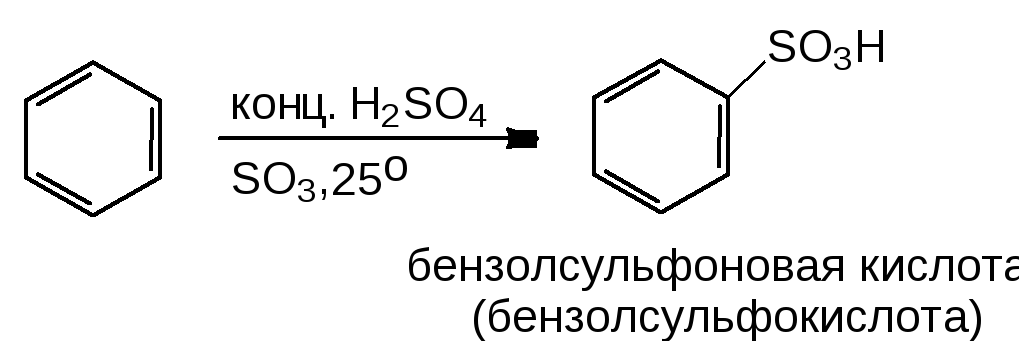 (9)
(9)
Бензол сульфируется и просто в концентрированной серной кислоте, но только медленнее. Механизм сульфирования не так хорошо изучен, как механизм нитрования. Предполагается, что непосредственно сульфирующим реагентом является оксид серы (VI). В концентрированной серной кислоте SO3 возникает в результате следующей реакции:
![]()
Механизм
1. Бензол атакуется триоксидом серы

бензол и триоксид серы циклогексадиенильный катион
2. Потеря протона циклогексадиенил катионом.
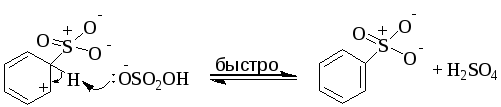
промежуточный бензолсульфонат
циклопентадиенильный катион
3. Передача протона от серной кислоты к бензолсульфонату.

бензолсульфонат бензолсульфоновая кислота
Особенностью реакции сульфирования является ее обратимость. Для осуществления обратной реакции удаления сульфогруппы через смесь бензолсульфокислоты с разбавленной серной кислотой пропускают перегретый водяной пар. Такая реакция называется десульфированием.
 (10)
(10)
Обратимость сульфирования позволяет вводить в кольцо дейтерированную метку:
 (11)
(11)
дейтеробензол
