

Чаще используется для повторного использования пиримидинов (тимидинкиназа, цитидинкиназа).
2. Синтез нуклеотидов на основе готовых азотистых оснований больше характерен для пуринов и проходит в 2 этапа:
а) образование активной формы рибозо-5-фосфата (фосфорибозилпирофосфата):
б) взаимодействие ФРПФ с азотистым основанием:
АО |
Нуклеозидмонофосфат |
НТФ |
ФРПФ |
ФФн |
|
Фосфорибозил |
|
|
трансфераза |
|
|
De novo синтез пуриновых нуклеотидов |
|
|
Особенностью синтеза пуринов de novo является то, что за основу берется рибозо-5-фосфат и на его основе формируется пуриновое кольцо. N- гликозидная связь формируется уже на ранних этапах синтеза.
Источником всех атомов азота для пуринового ядра являются аминокислоты
(глицин, глутамин, аспартат). Источники атомов углерода: СО2 и формил-ТГФК (активная форма фолиевой кислоты, В9). Общим предшественником для адениловых и гуаниловых нуклеотидов является инозинмонофосфат (ИМФ).
Рибозо-5-фосфат + АТФ |
|
Фосфорибозилпирофосфат + АМФ |
ФРПФ- |
(ФРПФ) |
|
синтетаза |
Амидотрансфераза |
|
|
|
|
Фосфорибозиламин |
||
+гли |
|
|
+глн |
+ СО2 |
|
+асп |
+ 2формил-ТГФК |
|
Инозинмонофосфат |
||
+асп |
|
+глн |
+ГТФ |
|
+АТФ |
АМФ |
|
ГМФ |
АДФ |
|
ГДФ |
74

АТФ |
ГТФ |
Ключевой фермент синтеза пуринов: амидотрансфераза. Регуляция:
1)аллостерическая: избыток конечных продуктов (АТФ, ГТФ) ингибирует ключевой фермент; избыток пиримидиновых нуклеотидов его активирует; 2)ГМФ ингибирует образование ксантиловой кислоты, а АМФ — аденилоянтарной;
3)перекрестная: для синтеза АМФ требуется ГТФ, а для синтеза ГМФ требуется АТФ; Наиболее распространенной формой нарушения обмена пуринов является подагра.
Основная причина — повышение уровня мочевой кислоты в крови (гиперурикемия) и ее отложение в почках и суставах. Причины: а) избыточный синтез пуриновых нуклеотидов (нечувствительность ферментов к регуляторам); б) дефект ферментов реутилизации пуринов; в) патология почек (недостаточное выведение). Способствует избыточное потребление пуринов с пищей. В лечении подагры используется аллопуринол — ингибитор ксантиноксидазы.
De novo синтез пиримидиновых нуклеотидов
В отличие от пуринов, при биосинтезе пиримидинов de novo вначале образуется пиримидиновое кольцо, а лишь затем к нему присоединяется рибозо-5-фосфат. Источниками атомов для пиримидинового кольца являются глутамин, аспартат и СО2. Синтез начинается с образования карбамоилфосфата:
Глутамин + СО2 + 2 АТФ ¾¾¾¾¾¾® Карбамоилфосфат + Глутамат + 2 АДФ + Фн.
Карбамоилфосфатсинтетаза II
В отличие от карбамоилфосфатсинтетазы I, фермент синтеза пиримидинов использует амидный азот глутамина (а не свободный аммиак) и локализован в цитоплазме.
Карбамоилфосфат + Аспартат ¾¾¾¾¾¾® Карбамоиласпарагиновая
Аспартаткарбамоил- кислота трансфераза
|
|
|
Оротовая к-та |
|
|
|
+ФРПФ |
ДГФК |
метилен-ТГФК |
Оротидин-5/-мономофосфат |
|
–СО2 |
|||
дТМФ |
Тимидилат- |
дУМФ |
УМФ |
|
|
|
|
дТДФ |
синтаза |
дУДФ |
УДФ |
дТТФ |
|
|
УТФ |
|
|
|
+NH2 (Глн) |
|
|
|
АТФ |
75
ЦТФ
Ключевой фермент — аспартаткарбамоилтрансфераза.
Регуляция: избыток пиримидиновых нуклеотидов ингибирует ключевой фермент, а избыток пуриновых — активирует.
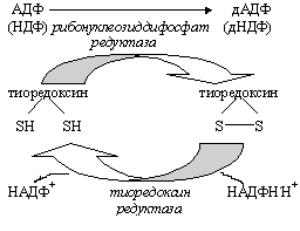
Образование дезоксирибонуклеотидов
Образование дезоксирибонуклеотидов, необходимых для биосинтеза ДНК, происходит на уровне нуклеозиддифосфатов. С участием специального белка тиоредоксина фермент редуктаза восстанавливает 2/-ОН группу в рибозе и образуется дезоксирибоза. Затем:
дНДФ ¾¾®дНТФ ¾¾® синтез ДНК.
76
