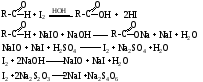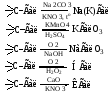ФХ. Весенний семестр 2015 / Вопросы тест- и программ-контролей / Вопросы тк (занятие 2). Каминский
.docxТест-контроль по теме «Ациклические алканы, их галогено- и кислородсодержащие соединения. Альдегиды и их производные. Лактоны ненасыщенных полиоксикарбоновых кислот»
1. Реакция окисления используется при количественном определении:
1) калия йодида;
2) глюкозы;
3) цинка оксиды;
4) кислоты аскорбиновой.
2. Формальдегид легко вступает в реакции:
1) присоединения;
2) окислительно-восстановительные;
3) замещения;
4) обмена.
3. Примеси солей аммония и параформа определяют в лекарственном средстве:
1) спирт этиловый;
2) раствор формальдегида;
3) гесаметилентетрамин;
4) глюкоза.
4. Реакцию образования йодоформа нельзя использовать для:
1) определения подлинности этанола;
2) определения подлинности лактат-иона;
3) примеси метанола в спирте этиловом.
5. Для подтверждения подлинности альдегидов используют реакции:
1) с реактивом Фелинга;
2) с реактивом Толленса;
3) с реактивом Вагнера;
4) с кислотой салициловой в присутствии кислоты серной;
5) с реактивом Несслера.
6. Белый осадок в растворе формальдегида образуется при:
1) хранении препарата при температуре выше 9С;
2) хранении при температуре ниже 9С;
3) хранении при доступе влаги;
4) хранении в посуде светлого стекла.
7. Количественное определение кислоты аскорбиновой можно проводить методами:
1) ацидиметрии;
2) алкалиметрии;
3) йодометрии;
4) йодатометрии.
8. Величина молярной массы эквивалента кислоты аскорбиновой при количественном определении методом йодатометрии составляет:
1) 1 М.м. кислоты аскорбиновой;
2) 1/2 М.м. кислоты аскорбиновой;
3) 1/3 М.м. кислоты
аскорбиновой;
4) 1/4 М.м. кислоты аскорбиновой.
9. Восстанавливающими свойствами обладают лекарственные средства:
1) калия йодид;
2) кислота аскорбиновая;
3) натрия хлорид;
4) раствор формальдегида.
10. Кислота аскорбиновая образует соль с реактивом:
1) железа (III) хлоридом;
2) серебра нитратом;
3) железа (II) сульфатом;
4) натрия гидрокарбонатом.
11. Витаминным средством является:
1) аминалон;
2) пирацетам;
3) кислота глутаминовая;
4) кислота аскорбиновая.
12. Какие из указанных соединений содержат лактонную группу?

13. Присутствие лактонной группы может быть доказана реакцией:
1) этерификации;
2) образования железа (III) гидроксаматов;
3) образования сложных эфиров;
4) образования простых эфиров;
5) реакцией электрофильного замещения.
14. Реакции характерные для спиртов:
1) присоединения;
2) этерификации;
3) нейтрализации;
4) окисление до альдегидов.
15. Лучшим из ацетилирующих агентов при анализе соединений, содержащих спиртовый гидроксил, является:
|
1) |
|
|
2) |
|
|
3) |
|
|
4) |
16. Механизм реакции этерификации заключается в:
1) реакции между спиртом и щелочью;
2) реакции между спиртом и кислотой;
3) реакции между спиртом и кислотой в присутствии H2SO4 конц.;
4) реакции между спиртом и альдегидом;
5) реакции между спиртом и третичным амином.
17. Специфической реакцией на этанол является:
1) образование хлороформа;
2) образование йодоформа;
3) реакция этерификации;
4) реакция образования комплексной соли с Cu2+.
18. При окислении соединений, содержащих спиртовый гидроксил, происходит процесс:
1) первичные спирты окисляются до альдегидов;
2) образуется эфир;
3) вторичные спирты окисляются до кетонов;
4) третичные спирты окисляются до кетонов.
19. Следующие реакции соответствуют реакциям окисления спиртов:
|
1) |
|
|
2) |
|
|
3) |
|
|
4) |
20. К многоатомным спиртам относятся:
1) глюкоза;
2) этиловый спирт;
3) фруктоза;
4) салициловая кислота;
5) глицерин.
21. Многоатомные спирты проявляют:
1) слабоосновной характер;
2) слабокислотный характер.
22. Альдегидной называется группа, в которой карбонил связан с:
1) атомом водорода и углеводородным радикалом (или атомом углерода);
2) гидроксильной группой;
3) амидной группой;
4) меркаптогруппой;
5) фенольным гидроксилом.
6) двумя углеводородными радикалами.
23. Альдегидную группу содержат:
1) камфора;
2) формальдегид;
3) глюкоза;
4) гексаметилентетрамин;
5) ацетилсалициловая кислота.
24. При гидролитическом разложении образуют формальдегид:
1) камфора;
2) стрептоцид;
3) глюкоза;
4) гексаметилентетрамин;
5) норсульфазол.
25. Лекарственные вещества, содержащие альдегидную группу, окисляются:
1) до карбоновых кислот с тем же числом атомов углерода;
2) до карбоновых кислот с меньшим числом атомов углерода;
3) до кетогруппы;
4) с разложением до СО2 и Н2О;
5) не окисляются.
26. В состав реактива Фелинга входит:
1) Cu2+;
2) Hg2+;
3) Fe3+;
4) SCN1-;
5) Ag1+.
27. Реактивами для обнаружения альдегидов являются:
1) молибденовая жидкость;
2) металлический натрий;
3) реактив Фелинга;
4) реактив Толленса;
5) реактив Драгендорфа;
6) реактив Несслера.
28. Количественное определение альдегидов проводят:
1) методом нейтрализации;
2) методом трилонометрии;
3) методом Фаянса;
4) ацидиметрией в неводных средах;
5) йодиметрическим методом.
29. Укажите последовательность и реакции, соответствующие йодометрическому методу количественного определения альдегидов:
|
1) |
|
|
2) |
|
|
3) |
|
|
4) |
|
|
5) |
30. Укажите фактор эквивалентности и расчетные формулы определения массовой доли вещества в процентах, соответствующие йодометрическому методу количественного определения альдегидов:
|
1) |
f=1
|
|
2) |
f=½ |
|
3) |
|
|
4) |
|
|
5) |
31. Для выделения альдегидов из смеси веществ можно использовать реакции:
1) реакция с сульфаниламидом;
2) реакция с фенилгидразином;
3) реакция с аммиаком;
4) реакция с фенолом;
5) реакция с натрия гидросульфитом.
32. При хранении формальдегида при температуре ниже +9С происходит процесс:
1) разложения;
2) образования окрашенного соединения хиноидной структуры;
3) выделения белого осадка параформа;
4) образования осадка гексаметилентетрамина;
5) образования осадка темно-серого цвета.
33. Реакция образования оснований Шиффа является характерной:
1) только для альдегидов;
2) только для кетонов;
3) для альдегидов и кетонов;
4) ни для альдегидов, ни для кетонов;
5) для соединений с карбонильной группой.
34. Какие из ниже перечисленных реактивов используются в реакциях образования оснований Шиффа?
1) соединения с первичной ароматической аминогруппой;
2) производные гидразина;
3) производные фенола;
4) реактив Несслера;
5) реактив Толленса.
35. Реакцией образования основания Шиффа является:
|
1) |
|
|
2) |
|
|
3) |
|
|
4) |
|
|
5) |
36. Прочность связи атома галогена с атомом углерода зависит от:
1) природы органического соединения;
2) природы галогена;
3) удаленности валентных электронов галогена от ядра.
37. Расположите соединения в порядке убывания прочности связи галогена с углеродом:
|
1) |
|
|
2) |
|
|
3) |
|
|
4) |
38. Укажите методы переведения галогенов из ковалентно-связанного в ионное состояние:
1) проба Бельштейна;
2) сплавление с натрия или калия гидроксидом;
3) нагревание с раствором серебра нитрата в азотнокислой среде;
4) метод сжигания в колбе с кислородом;
5) реакция с реактивом Драгендорфа.
39. Укажите условия проведения реакции идентификации галогенов, соответствующие пробе Бельштейна:
|
1) |
|
|
2) |
|
|
3) |
|
|
4) |
|
|
5) |
40. Следующие галогениды не дают пробы Бельштейна:
1) фториды;
2) хлориды;
3) бромиды;
4) йодиды.
41. В случае особо прочной связи галогена с углеродом, для перевода ковалентно-связанного галогена в ионное состояние используют методы:
|
1) |
|
|
2) |
|
|
3) |
42. Для перевода ковалентно-связанного галогена в галогеносодержащих соединениях в ионное состояние применяют следующие восстановительные методы:
1) взаимодействие цинка с серной кислотой;
2) взаимодействие цинка с натрия или калия гидроксидами;
3) взаимодействие металлического натрия с безводным этиловым спиртом;
4) взаимодействие цинка с уксусной кислотой;
5) взаимодействие цинка с хлороводородной кислотой.
43. Метод «сухого озоления» для переведения ковалентно-связанного галогена в галогенсодержащем соединении в ионное состояние заключается:
|
1) |
|
|
2) |
|
|
3) |
|
|
4) |
|
|
5) |
44. Возможными методами идентификации галогенов после их переведения в ионное состояние являются:
|
1) |
|
|
2) |
|
|
3) |
|
|
4) |
45. Методами количественного определения галогенидов после переведения их в ионное состояние являются:
1) метод Фольгарда;
2) метод Фаянса;
3) метод Мора;
4) метод Фольгарда в модификации Кольтгоффа;
5) меркуриметрический метод.