
- •ЛЕКЦИЯ 8
- •O, S, Se, Te, Po – халькогены
- •Природные ресурсы
- •алюмосиликаты
- •Получение
- •Свойства
- •Оксиды делят на:
- •температуры плавления (0° С) и кипения (100° С). Толстый слой воды имеет голубой
- •Химические свойства
- •Н2О2 – пероксид
- •Н2О2 проявляет окислительные и восстановительные свойства.
- •Сера
- •Природные ресурсы:
- •мирабилит
- •пирит
- •галенит
- •сфалер
- •Получение
- •Свойства
- •Известны и другие формы серы (пурпурная),получается при быстрой конденсации паров серы на поверхности,
- •Химические свойства
- •H2S сероводород
- •Вода с запахом
- •а) на воздухе H2S горит:
- •Соли называются сульфидами. Многие сульфиды ярко окрашены. В воде растворимы только сульфиды щелочных
- •BaSO4 4C BaS 4CO
- •4) Соединения S с O(SO2 2 и SO3)
- •SO2 – бесцветный газ с удушливым запахом, легко превращаемый в жидкость, t пл
- •Тиосульфаты соли.
- •Известно несколько кристаллических форм SO3. При хранении образуется β-SO3 в виде длинных блестящих,
- •При t° выше 600°С SO3 разлагается
- •Получение H2SO4
- •Получение H2SO4 из SO3 является основным методом производства H2SO4 (контактный метод). В промышленности
- •Свойства H2SO4
- •на холоду пассивирует Fe, Al, Cr.
- •медицина

Сера
Характерные степени окисления и важнейшие соединения:
– 2 (H2S и соли сульфиды, тиосульфат Na
Na2S2O3·5H2O)
+ 4 (SO2, H2SO3 –сернистая кислота и соли сульфиты)
+ 6 (H2SO4, - серная кислота и соли сульфаты, пиросерная кислота H2S2O7,
пероксодисерная кислота H2S2O8)

Природные ресурсы:
Соединение S в земной коре – 5·10–2 %, в мировом океане её – 9·10–2 %. Встречается в больших количествах самородная сера. К важнейшим природным соединениям S относятся сульфаты.
Na2SO4·10H2O – мирабилит CaSO4·2H2O – гипс
FeS2 – пирит PbS – галенит ZnS – сфалерит
FeS2, PbS, ZnS – сульфиды и полисульфиды



мирабилит

пирит

галенит

сфалер
ит
сфалерит

Получение
1) Поскольку S встречается в больших количествах в самородном виде, то получение её сводится к отделению её от пустой породы. Это достигается выплавлением её с помощью горячей воды (при > 119°С и давлении) в автоклавах.
2) S получают также из газов – H2S и SO2 (природные газы используются при обжиге сульфидных руд.)
3) Серу высокой чистоты получают перекристаллизацией из раствора серы в сероуглероде.
Свойства
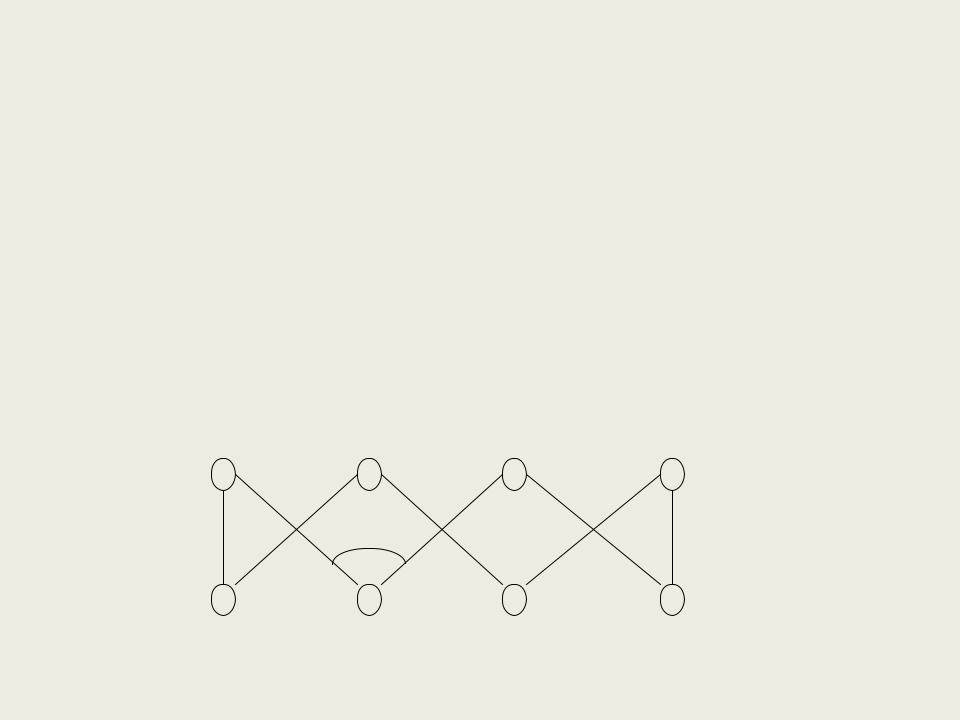
Сера существует в нескольких аллотропных формах. При комнатной температуре стабильна желтая ромбическая сера (α – сера).108˚S 8
В интервале от 95,4°С до 119,3°С (tпл) устойчива моноклинная сера (β – сера). Окраска у неё бледнее, чем у ромбической. Модификации α и β серы состоят из молекул S 8, которые имеют циклическое «зубчатое» строение.
108˚ |
S8 |
