
6.3. Понятия об электрокинетических явлениях в промывочных жидкостях
Возникновение разноименных зарядов в поверхностном слое дисперсных систем приводит к ряду интересных явлений, называемых электрокинетическими. Электрокинетические явления развиты тем сильнее, чем выше подвижной заряд диффузного слоя и пропорциональный ему потенциал границы скольжения
Если к дисперсной системе приложить электрическое напряжение, то можно наблюдать перемещение фаз относительно друг друга:
а) при электрофорезе в неподвижной дисперсионной среде движутся частицы дисперсной фазы;
б) при электроосмосе через проницаемое тело (например, фильтрационную глинистую корку) перемещается жидкая фаза к полюсу, имеющему одноименный с дисперсной фазой знак.
Если же осуществить вынужденное механическое перемещение фаз относительно друг друга, то в дисперсной системе возникает разность потенциалов:
а) потенциал оседания при движении дисперсных частиц в неподвижной жидкости;
б) потенциал течения при движении жидкости относительно неподвижной твердой поверхности.
Электрокинетические явления, обусловленные наличием электрического заряда на поверхности дисперсных частиц, играют важную роль во многих процессах, которые происходят в буровых промывочных жидкостях при приготовлении их методами предварительного гидратирования и диспергирования твердой фазы; при структурообразовании и стабилизации обработкой химическими реагентами; при фильтрации в проницаемые пласты и т.д. Поэтому результаты исследований электрокинетических характеристик промывочных жидкостей все чаще применяют для анализа этих процессов.
В поверхностном слое ДЭС возникает вследствие специфической адсорбции, поверхностной диссоциации и изоморфных замещений в кристаллической решетке.
Наличие ДЭС в глинистых минералах, особенно в монтморилонитах, может быть также обусловлено, как отмечалось ранее, изоморфными замещениями Si4+ и А13+ в тетраэдрическом и октаэдрическом слоях алюмосиликатов соответственно А13+ и Mg2+ (или другим, двух- или одновалентным катионом). При этом поглощается электрон извне и минерал приобретает отрицательный заряд
На величину поверхностного заряда существенно влияют и другие дефекты на поверхности или внутри кристаллической решетки. Причем заряд, приобретаемый за счет вакантных мест, будет отрицательным, если вакансии катионов будут в избытке и положительным при избытке вакансий анионов Вклад в величину поверхностного заряда зависит от плотности дефектов
6.4 Двойной электрический слой
Строение двойного электрического слоя
Независимо от причин образования ДЭС под действием сил электростатического притяжения образуются по крайней мере два слоя ионов, один из которых расположен на поверхности, другой - в растворе на определенном расстоянии. Потенциал в ДЭС, как и в плоском конденсаторе, будет падать круто по прямой, а поверхностный заряд ρ можно определить по формуле
где - диэлектрическая проницаемость среды; - расстояние между обкладками; - разность потенциалов между дисперсной фазой и раствором.
Теория Квинке-Гельмгольца предполагает, что один из слоев находится на твердой поверхности, а другой-в жидкости.
Плотность избыточных зарядов одного знака (в нашем случае отрицательных) возрастает сразу от 0 до определенного значения и далее при переходе в жидкость падает и изменяет знак на положительный. При дальнейшем смещении в глубь жидкости плотность избыточных зарядов внов приходит к 0. Изменение избыточного заряда аналогично падению потенциала между обкладками конденсатора (рис 11.18,в)

По теории Гуи-Чапмена ионы в жидкости под действим теплового движения стремятся распределиться равномерно в растворе.
Поэтому в результате электростатического притяжения и теплового движения создается диффузионное распределение противоионов в наружном слое (рис. II.9, а). При этом концентрация катиона Скат убывает по мере удаления от поверхности в глубь раствора, а концентрация анионов Сан — возрастает (рис. 11.9,6)
Таким образом, слой противоионов предполагается не плоским, размытым, причем плотность зарядов в нем плавно падает с увеличением расстояния от поверхности (рис. II.9, в).

Формирование этого слоя обусловлено действием противоположных процессов:
а) притяжением за счет элекростатического взаимодействия, в связи с чем концентрация противоионов у поверхности должна возрастать;
б) оттоком ионов в результате диффузии из области высоких концентраций (т.е. от поверхности) в область низших концентраций.
Положения теории Гуи—Чапмена позволяют объяснить некоторые электрокинетические явления. Плоскость скольжения А В (рис. II.9, г) при перемещении твердой и жидкой фаз относительно друг друга лежит в жидкости на некотором расстоянии Δ от межфазной границы. Разность потенциалов между поверхностью скольжения и жидкой фазой называется электрокинетическим или ζ-потенциалом. Она будет определять перемещение фаз при наложении электрического поля, т. е. обусловливать явления электрофореза или электроосмоса. Электрокинетический или ζ -потенциал является частью термодинамического потенциала φо.
Ясно, что если в систему вводить индифферентный электролит (не имеющий ионов, достраивающих кристаллическую решетку), то общий скачок потенциала φо почти не изменится, а ζ-потенциал с уменьшением толщины диффузного слоя уменьшится, так как для компенсации потенциала определенных ионов всегда требуется одно и то же эквивалентное число противоположно заряженных ионов. В таком случае, говоря, что ДЭС сжимается. Это значит, что при
С1 ≤ С2 ≤С3 получим ζ1 ≥ ζ2 ≥ ζ3.
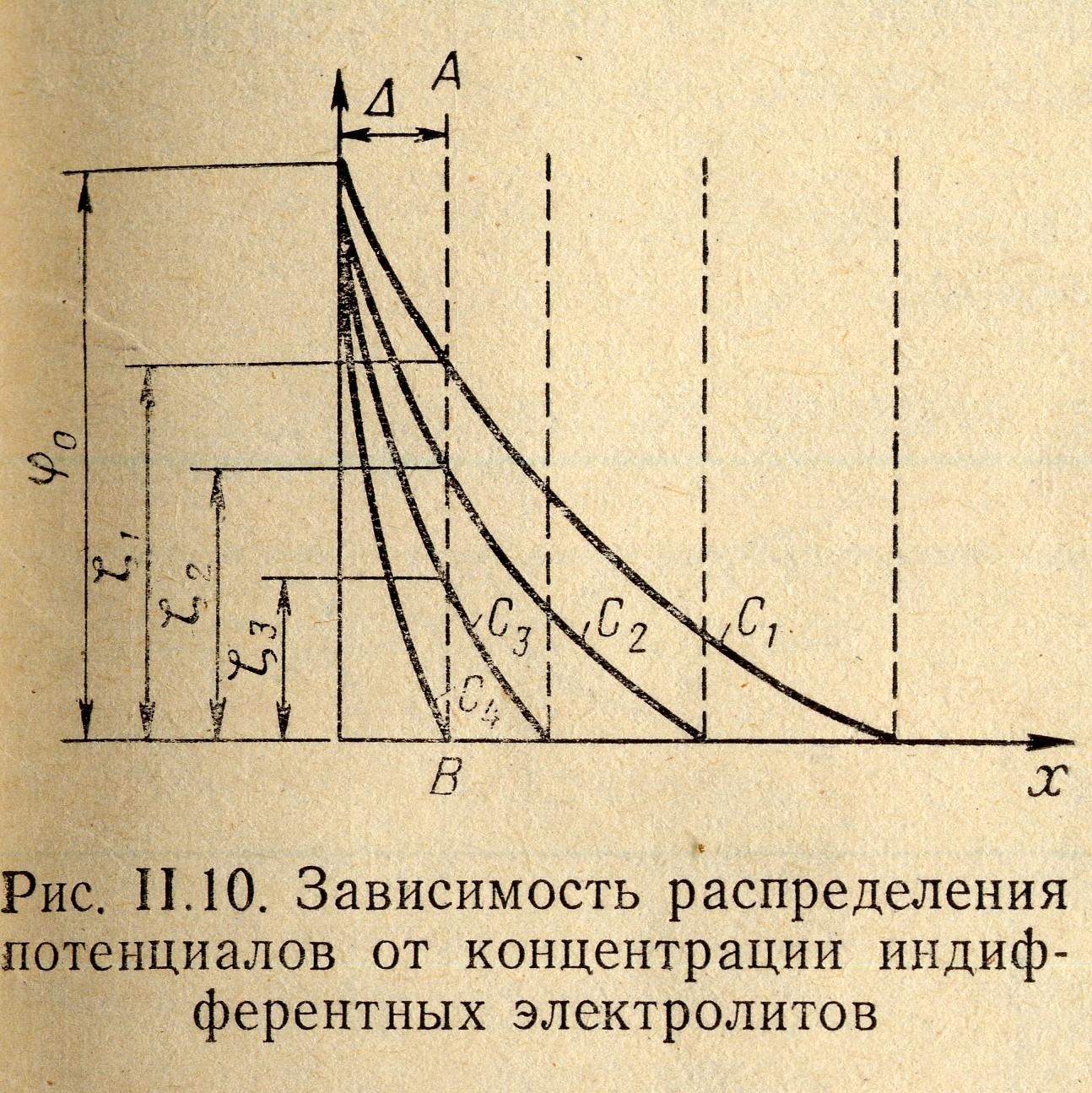
При больших концентрациях индифферентного электролита диффузный слой может сжаться до моноионного слоя и превратиться в структуру ДЭС, по теории Квинке—Гельмгольца (ζ4=0).
Теория Гуи—Чапмена имеет следующие недостатки:
в ней не принимаются во внимание размеры ионов (они рассматриваются как точечные заряды), что обусловливает высокие значения расчетных величин;
она не объясняет явление перезарядки; т. е. перемены знака ζ-потенциала при введении в систему электролита с поливалентным ионом, заряд которого противоположен заряду дисперсной фазы;
она не объясняет различного действия ионов одной и той же валентности, но отличающихся величиной ионных радиусов, например Na+ и К+.
В современной теории строения ДЭС Штерна используются следующие предпосылки:
а) формирование слоя противоионов происходит не только вследствие электростатического взаимодействия их с заряженной поверхностью, но зависит и от адсорбционных сил поверхности твердой частицы, которые действуют на коротких расстояниях и являются ответственными за формирование первого слоя противоионов в молекулярном конденсаторе;
б) как бы ни были малы противоионы, они имеют конечные размеры.
Исходя из этих условий, принимают что слой 1 противоионов (рис. 6.4, а) начинается не у самой поверхности, а на некотором расстоянии (упрощенно можно считать это расстояние равным радиусу частично гидратированного противоиона).

Рис 6.4
Соотношение между электростатическими и адсорбционными силами определяет концентрацию и заряд ионов у поверхности, если адсорбционная способность противоионов велика, то под совместным действием адсорбционных и электростатических сил возрастает концентрация ионов в слое П.
В тех случаях, когда адсорбционные силы превысят силы электростатического притяжения первый слой может состоять из ионов одноименных с потенциалопределяющими.
Теория Штерна (рис. 6.4, б) позволяет выделять адсорбционный и диффузный слои с потенциалами φх и ζ, возникающим соответственно на расстояниях б и Δ от межфазной границы. Повышение концентрации электролитов приводи к сжатию ДЭС, причем сжимаемость увеличивается с ростом валентности. Это позволило дать четкое определение понятие ζ-потенциала, представляющего собой скачок потенциала на границе адсорбционного и диффузного слоев по сравнению с объемом раствора. Такое определение означает, что под действием внешнего электрического поля перемещаются ионы диффузного слоя, а ионы адсорбционного слоя удерживаются на поверхности. Теория Штерна дает объяснение явлению перезарядки ζ-потенциала, изменению его знака при введении в систему многовалентных ионов, заряд которых противоположен знаку дисперсной фазы.
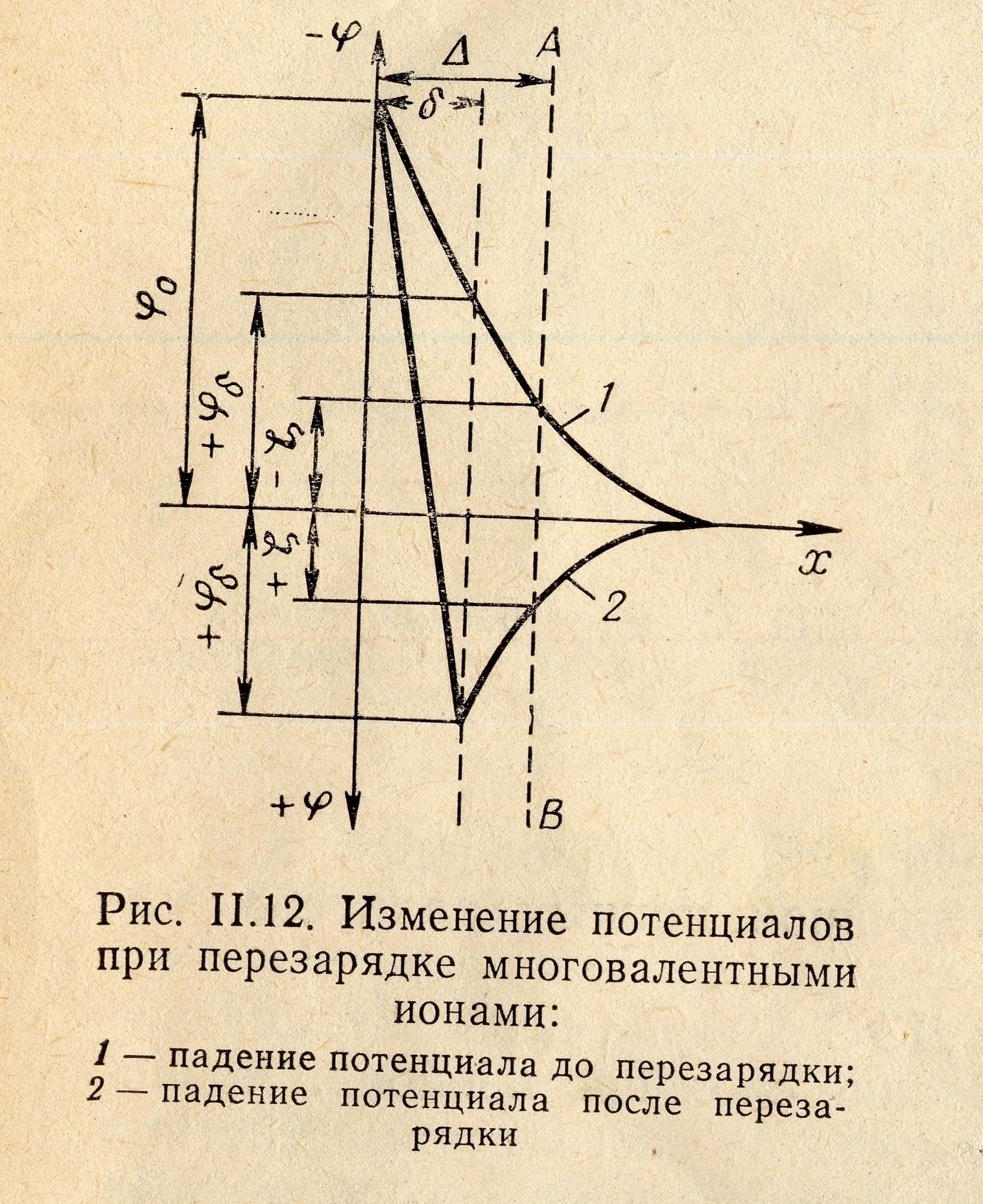
Рис. 6.5
Это связано с тем, что многовалентные ионы втягиваются в адсорбционный слой, как вследствие сильных электростатических взаимодействий, так и вследствие большой адсорбируемости (поглощаемости в соответствии с лиотропными рядами), которая связана с поляризуемостью ионов. Ионы могут адсорбироваться в таком количестве, что они не только нейтрализуют заряд твердой поверхности, но и перезаряжают частицу, т. е. φб и ζ , проходя через изоэлектрическую точку, меняют знаки (рис. 6.5). При этом термодинамический потенциал φо остается постоянным, так как чужеродные ионы не способны достраивать кристаллическую решетку твердой фазы.
Строение ДЭС, по Штерну, позволяет также объяснить структуру коллоидной мицеллы (рис. 6.6, 6.7).
