
лекция 21
.pdf
Химические свойства кислот
можно подразделить на:
1) Общие (связанные с наличием Н+):
–реакция с основными и амфотерными оксидами
CuO + 2HNO3 –t°→ Cu(NO3)2 + H2O ZnO + H2SO4 → ZnSO4 + H2O

Химические свойства кислот
можно подразделить на:
1) Общие (связанные с наличием Н+):
–реакция с солями (средними, основными, кислыми)
Na2SiO3 + 2HCl → 2NaCl + H2SiO3
H2SO4 + 2NaHCO3 → Na2SO4 + 2CO2 + 2H2O CoOHCl + HCl → CoCl2 + H2O

Химические свойства кислот
можно подразделить на:
1) Общие (связанные с наличием Н+):
– реакция с металлами с выделением водорода
Zn + H2SO4(разб) → ZnSO4 + H2↑ Fe + 2HCl → FeCl2 + H2↑
Pb + 2CH3COOH → (CH3COO)2Pb + H2↑

Химические свойства кислот
можно подразделить на:
2) Специфические (характерные для конкретных кислот):
– качественные реакции на отдельные кислоты
(на анионы)
CaCO3 + 2HCl → CaCl2 + CO2↑ + H2O
H2SO4 + BaCl2 → BaSO4↓ + 2HCl
AgNO3 + HCl → AgCl↓ + HNO3

Химические свойства кислот
можно подразделить на:
2) Специфические (характерные для конкретных кислот):
– окислительно-восстановительные реакции
Cu + 2Н2SO4(конц) → CuSO4 + SO2 + 2H2O 4Zn + 5Н2SO4(конц) → 4ZnSO4 + Н2S + 4H2O Fe + 4HNO3(разб) → Fe(NO3)3 +NO + 2H2O
4Zn + 10HNO3(разб) → 4Zn(NO3)2 + NН4NO3 + 3H2O Cu + 4HNO3(конц) → Cu(NO3)2 +2NO2 + 2H2O

Химические свойства кислот
можно подразделить на:
2) Специфические (характерные для конкретных кислот):
– окислительно-восстановительные реакции C + 2Н2SO4(конц) → CO2 + 2SO2 + 2H2O
2P + 5Н2SO4(конц) → 2Н3PO4 + 5SO2 + 2H2O S + 2HNO3(конц) → Н2SO4 +2NO
Si + 4HNO3(конц) + 12НF(конц) → 3SiF4 +4NO + 8H2O

Химические свойства кислот
можно подразделить на:
2) Специфические (характерные для конкретных кислот):
– окислительно-восстановительные реакции
2NaBr(тв.)+2H2SO4(конц.) –t°→ Na2SO4+SO2+Br2 + 2H2O 8NaI(тв.)+5H2SO4(конц.) –t°→ 4Na2SO4+H2S + 4I2 + 4H2O

Применение кислот
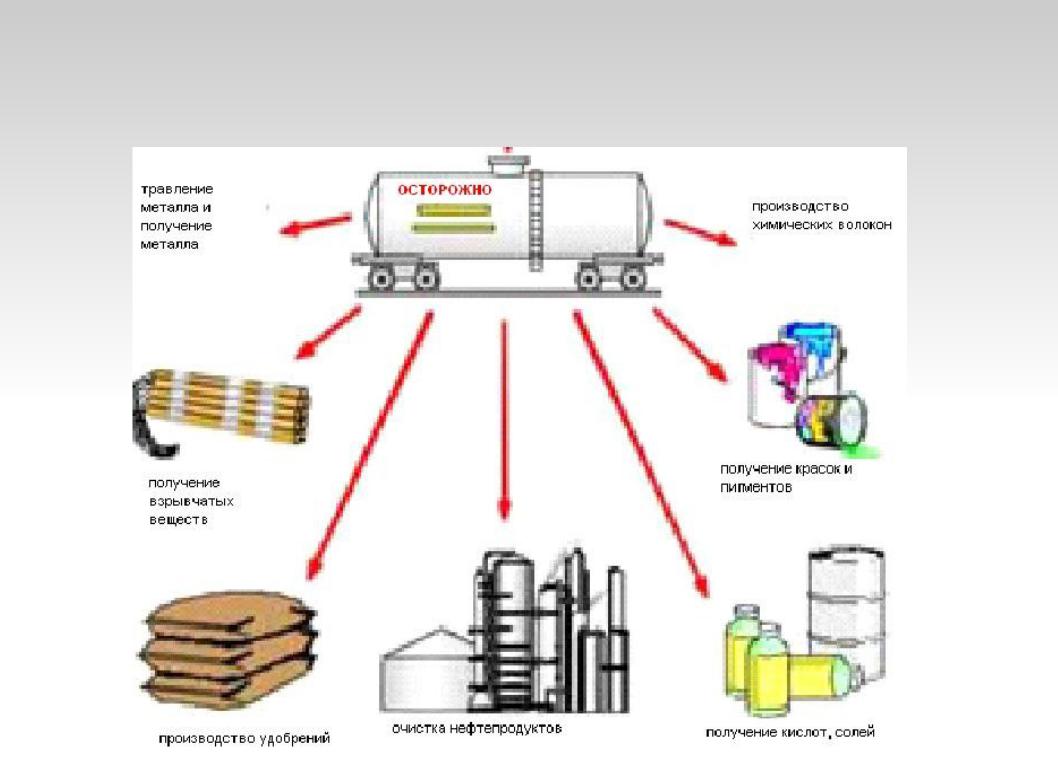
Применение кислот

Соли - сложные вещества, которые состоят из катионов металла и анионов кислотного остатка
