
- •Сборник заданий
- •Задание №1 по теме "строение вещества"
- •Варианты домашнего задания по теме «Строение вещества»
- •1.Задание по теме «строение атома»
- •ЗаданиЯ по теме «ковалентная химическая связь и строение молекулярных частиц»
- •2.1.Опишите строение предложенных в варианте задания молекул и молекулярных ионов по методу валентных связей (мвс):
- •Задания по теме «межмолекулярные взаимодействия и свойства веществ»
- •3.1. Проанализируйте влияние сил межмолекулярного взаимодействия на свойства веществ (решите задачу с указанным номером).
- •Типы межмолекулярного взаимодействия
- •Список рекомендуемой литературы
- •Задание №2 по теме: «термохимия. Направление химических реакций»
- •Примеры решения задач
- •2. Рекомендации для самостоятельной работы студентов и варианты заданий
- •3. Задачи для самостоятельного решения
- •4. Варианты заданий
- •Задание №3 по теме «химическая кинетика и равновесие»
- •Примеры решения задач
- •1.3. Вычисление константы химического равновесия
- •1.4. Вычисление равновесных концентраций
- •1.5. Направление смещения равновесия
- •Задачи для самостоятельного решения
- •Варианты заданий
- •Список рекомендуемой литературы
- •Задание № 4 по теме «Растворы»
- •Примеры решения задач
- •1.1. Процентная концентрация
- •1.3. Моляльная концентрация (моляльность) , мольная доля, титр
- •1.4. Осмотическое давление. Закон вант- гоффа
- •1.5. Давление насыщенного пара растворов. Тонометрический закон рауля
- •1.6. Температуры кипения и замерзания растворов.
- •2. Задачи для самостоятельного решения
- •3. Варианты заданий
- •Список рекомендуемой литературы
- •Задание №5 по теме: "растворы электролитов"
- •Примеры решения задач
- •1.1. Вычисление степени диссоциации слабых электролитов
- •1.3. Произведение растворимости
- •1.5. Обменные реакции в растворах электролитов
- •Варианты заданий
- •Список рекомендуемой литературы
- •Задание №6 по теме «гидролиз солей»
- •Примеры решения задач
- •Варианты заданий
- •Список рекомендуемой литературы
- •Задание № 7 по теме «Окислительно–восстановительные реакции. Электрохимия»
- •Примеры решения задач
- •2. Задания для самостоятельного решения
- •Список рекомендуемой литературы
- •Задание № 8 по теме «Классификация и свойства неорганических веществ»
- •Примеры решения задач
- •Пример 5. С какими из перечисленных веществ вступит в реакцию серная кислота: koh, CuO, Ba(oh)2, Fe2o3, Al2o3, co2, SiO2, h3po4, o2, h2o? Составьте уравнения возможных реакций.
- •Задания для самостоятельного решения
- •Варианты заданий
- •Список рекомендуемой литературы
- •Примеры решения задач
- •Задачи для самостоятельного решения
- •3.Варианты заданий
- •Задание № 10 по теме «Дисперсные системы»
- •Пример решения задачи
- •Варианты заданий
- •Список РекомендуемОй литературЫ
- •Сборник заданий для самостоятельной работы студентов по дисциплине «химия
- •450062, Республика Башкортостан, г.Уфа, ул. Космонавтов,1
1.3. Произведение растворимости
Пример 1. Растворимость гидроксида магния Mg(OH)2 при 18 оС равна
1,7∙10 –4 моль/л. Найти ПР(Mg(OH)2) при этой температуре.
Решение: При растворении каждого моля Mg(OH)2 в раствор переходит 1 моль ионов Mg+2 и 2 моль ионов ОН–.
Mg(OH)2![]() Mg2+
+
2 OH–
Mg2+
+
2 OH–
Следовательно, в насыщенном растворе Mg(OH)2
[Mg2+] = 1,7∙10-4 моль/л; [OH–] = 3,4∙10– 4 моль/л.
Отсюда
![]() .
.
Пример
2.
![]() .
Вычислить растворимость соли (в моль/л
и в г/л) при указанной температуре.
.
Вычислить растворимость соли (в моль/л
и в г/л) при указанной температуре.
Решение: Обозначим растворимость соли через s (моль/л). Тогда в насыщенном растворе PbI2 cодержится s моль/л ионов Pb2+ и 2s моль/л ионов I–.
PbI2![]() Pb+2+2I–
Pb+2+2I–
s s 2s
ПР=[Pb2+][I–]2 = 4s3
![]() ;
;
![]() .
.
Растворимость PbI2, выраженная в г/л, (m = ν∙M) составляет 1,3∙10-3∙461 = 0,6 г/л.
Пример 3. Во сколько раз растворимость CaC2O4 в 0,1 М растворе (NH4)2C2O4 меньше, чем в воде?
Решение: Вычислим растворимость CaC2O4 в воде. Пусть концентрация соли в растворе будет s (моль/л), поэтому можем записать
![]()
![]()
Отсюда
![]()
Найдем
растворимость этой соли в 0,1 М растворе
(NH4)2C2O4;
обозначим её через s′.
Концентрация ионов Ca2+
в насыщенном растворе тоже будет s′,
а концентрация [C2O42–]
составит (0,1+s′),
т.к. s′<<0,1,
то можно считать, что [C2O42–]
= 0,1моль/л. Тогда
![]() ;s′=2,6∙
10–7
моль/л. Следовательно, в присутствии
(NH4)2C2O4
растворимость СaC2O4
уменьшилась в
;s′=2,6∙
10–7
моль/л. Следовательно, в присутствии
(NH4)2C2O4
растворимость СaC2O4
уменьшилась в
![]() =620
раз.
=620
раз.
Пример 4. Смешаны равные объемы 0,02 н. растворов CaCl2 и Na2SO4; образуется ли осадок CaSO4?
Решение:
Найдем произведение концентраций ионов
Ca+2
и SO42–
и сравним его с
![]() .
Условием выпадения осадка является
[Ca2+][SO42–]
>
.
Условием выпадения осадка является
[Ca2+][SO42–]
>![]() .
.
Исходные молярные концентрации растворов CaCl2 и Na2SO4 одинаковы и равны 0,01 моль/л, т.к. при смешении исходных растворов общий объем раствора вдвое больше, то концентрация каждого из ионов уменьшается вдвое по сравнению с исходными. [Ca2+] = [SO42–] = 5∙10–3. Находим [Ca2+][SO42–] = 2,5∙10–5
![]()
2,5∙10-5 <6,1∙10-5.
Поэтому осадок не образуется.
1.4. ИОННОЕ ПРОИЗВЕДЕНИЕ ВОДЫ. ВОДОРОДНЫЙ ПОКАЗАТЕЛЬ
Пример 1. Концентрация ионов водорода в растворе равна 4∙10–3 моль/л. Определить рН раствора.
Решение: рН = -lg(4∙10–3) = -(lg4 + lg10-3)=3-0,6=2,4.
Пример 2. Определить концентрацию [H+] в растворе, рН которого равен 4,60.
Решение:
рН
= -lg[H+]
= 4,6. Перенесем знак минус lg[H+]=-рН=-4,6;
чтобы мантисса логарифма стала
положительной величиной, произведем
следующее действие
![]() следовательно, [H+]
= 2,5∙10–5
моль/л.
следовательно, [H+]
= 2,5∙10–5
моль/л.
Пример 3. Чему равна концентрация [OH–] в растворе, рН которого равен 10,80?
Решение: Из соотношения рН + рОН = 14 имеем рОН = 14 – рН = 3,20.
Отсюда
-lg[OH–]
= 3,2; lg[OH–]
= -3,20=![]() .
.
Этому значению логарифма соответствует значение
[OH–] = 6,31∙10–4 моль/л.
Пример 4. Определить концентрацию HCO3– и CO32– в 0,01М растворе H2CO3, если рН этого раствора равен 4,18.
Решение: Найдем концентрацию [H+] в растворе:
-lg[H+]
= 4,18;
![]()
[H+] = 6,61∙10–5 моль/л
H2CO3![]() H++HCO3–
диссоциация по первой ступени
H++HCO3–
диссоциация по первой ступени
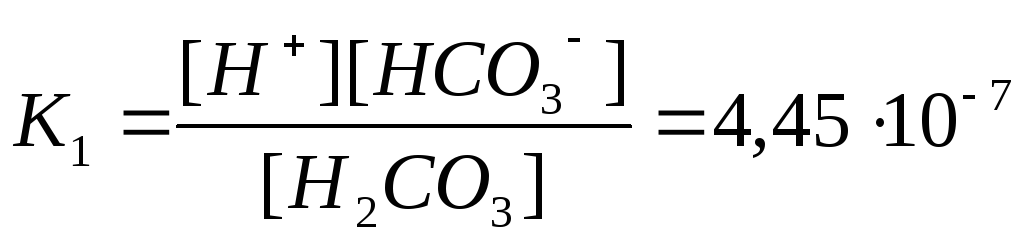
Подставляя значения [H+] и [H2CO3], находим
![]()
HCO3–![]() H++CO32–
диссоциация по второй ступени
H++CO32–
диссоциация по второй ступени
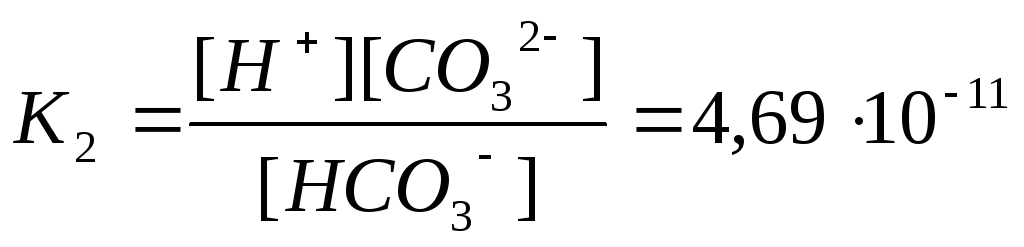
![]() .
.
