
- •1 . Химическое строение и биологическая роль холестерола. Пищевые источники холестерола. Пути и продукты метаболизма холестерола. Выведение холестерола из организма.
- •3. Характеристика нарушения обмена холестерола – желчнокаменная болезнь. Причины, последствия, основы лечения. Связь фосфолипидов с выведением холестерола. Липотропные вещества.
- •Методы лечения желчнокаменной болезни
- •4. Липопротеины крови: классификация, строение, этапы формирования. Апобелки: классификация, функции.
- •7. Локализация и роль апо-б100 рецептора. Значение рецептор-опосредованного эндоцитоза лпнп и пути метаболизма их компонентов после эндоцитоза. Роль ацил-sKoa: холестеролацилтрансферазы (ахат).
- •10. Характеристика нарушения транспорта холестерола в ткани – гиперлипопротеинемия iIа типа (семейная гиперхолестеролемия), её причины и клинические последствия.
- •12. Характеристика нарушений транспорта липидов – дислипопротинемии. Их причины и проявления.
Занятие 3. Обмен холестерола. Липопротеины. Гиперлипопротеинемии. Атеросклероз.
1 . Химическое строение и биологическая роль холестерола. Пищевые источники холестерола. Пути и продукты метаболизма холестерола. Выведение холестерола из организма.
Холестерол относится к группе соединений, имеющих в своей основе циклопентан-пергидрофенантреновое кольцо, и является ненасыщенным спиртом. Примерно 1/4 часть всего холестерола в организме этерифицирована олеиновой кислотой и полиненасыщенными жирными кислотами. В плазме крови соотношение эфиров холестерола к свободному холестеролу составляет 2:1.
Источники: Синтез холестерола в организме составляет примерно 0,5-0,8 г/сут, при этом половина образуется в печени, около 15% в кишечнике, оставшаяся часть в любых клетках, не утративших ядро. Таким образом, все клетки организма способны синтезировать холестерол. Из пищевых продуктов наиболее богаты холестеролом (в пересчете на 100 г продукта) сметана (0,002 г), сливочное масло (0,03 г), яйца (0,18 г), говяжья печень (0,44 г). В целом за сутки с обычным рационом поступает около 0,4 г.
В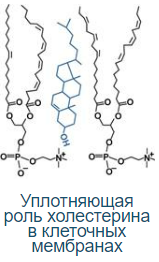 ыведение
холестерола из организма происходит
практически только через кишечник: o с
фекалиями в виде холестерола поступающего
из желчи и образованных микрофлорой
нейтральных стеролов (до 0,5 г/сут), o в
виде желчных кислот (до 0,5 г/сут),
biokhimija.ru Тимин О.А. Лекции по общей биохимии
(2020г) 263 o около 0,1 г удаляется со
слущивающимся эпителием кожи и секретом
сальных желез, o примерно 0,1 г превращается
в стероидные гормоны и после их разрушения
выводится с мочой.
ыведение
холестерола из организма происходит
практически только через кишечник: o с
фекалиями в виде холестерола поступающего
из желчи и образованных микрофлорой
нейтральных стеролов (до 0,5 г/сут), o в
виде желчных кислот (до 0,5 г/сут),
biokhimija.ru Тимин О.А. Лекции по общей биохимии
(2020г) 263 o около 0,1 г удаляется со
слущивающимся эпителием кожи и секретом
сальных желез, o примерно 0,1 г превращается
в стероидные гормоны и после их разрушения
выводится с мочой.
Функции холестерола: 1. Структурная – входит в состав мембран, повышая их вязкость и жесткость.
2. Связывание полиненасыщенных жирных кислот и их транспорт между органами и тканями в составе липопротеинов низкой и высокой плотности.
3. Является предшественником желчных кислот, стероидных гормонов (кортизола, альдостерона, половых гормонов) и витамина D.
2. Синтез холестерола. Локализация, источники углерода и водорода, этапы синтеза. Реакции синтеза мевалоновой кислоты. Схема дальнейших этапов синтеза х. Рекции синтеза х. с обменом углеводов. Регуляция синтеза. Гормональный и аллостерический механизмы регуляции. Понятие о лекарственной регуляции синтеза холестерола.
 Биосинтез
холестерола происходит в эндоплазматическом
ретикулуме. Источником всех атомов
углерода в молекуле является ацетил-SКоА,
поступающий сюда в составе цитрата, как
и при синтезе жирных кислот. При биосинтезе
холестерола затрачивается 18 молекул
АТФ и 13 молекул НАДФН. Образование
холестерола идет более чем в 30 реакциях,
которые можно сгруппировать в несколько
этапов:
Биосинтез
холестерола происходит в эндоплазматическом
ретикулуме. Источником всех атомов
углерода в молекуле является ацетил-SКоА,
поступающий сюда в составе цитрата, как
и при синтезе жирных кислот. При биосинтезе
холестерола затрачивается 18 молекул
АТФ и 13 молекул НАДФН. Образование
холестерола идет более чем в 30 реакциях,
которые можно сгруппировать в несколько
этапов:
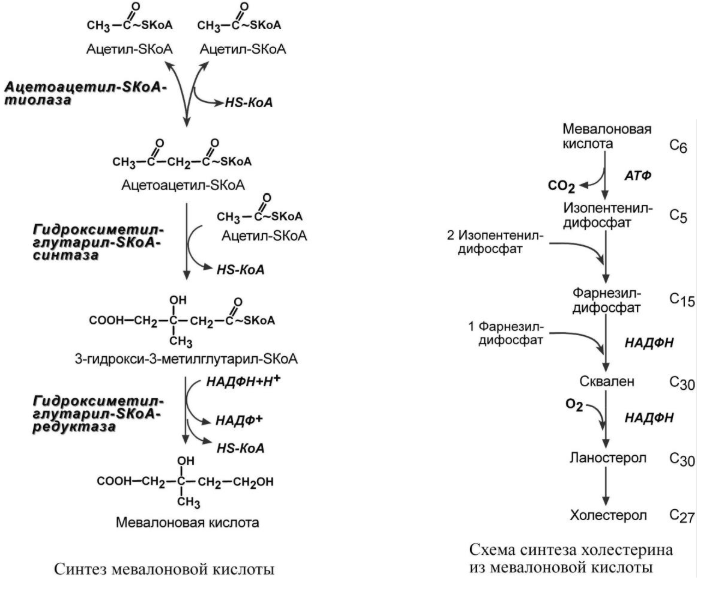
1. Синтез мевалоновой кислоты. Первые две реакции синтеза совпадают с реакциями кетогенеза, но после синтеза 3-гидрокси-3-метилглутарил-SКоА вступает в действие фермент ГМГ-SКоА-редуктаза, образующая мевалоновую кислоту.
2. Синтез изопентенилдифосфата.
3. Синтез фарнезилдифосфата.
4. Синтез сквалена.
5. Синтез ланостерола.
6. Синтез холестерола.
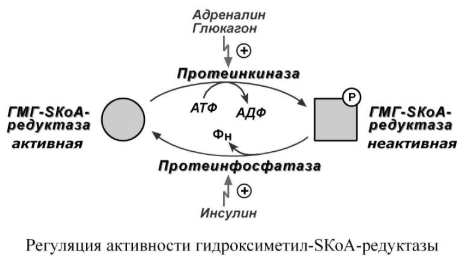 Регуляция:
Регуляторным ферментом является
гидроксиметилглутарил-SКоА-редуктаза:
Регуляция:
Регуляторным ферментом является
гидроксиметилглутарил-SКоА-редуктаза:
1. Метаболическая регуляция – по принципу обратной отрицательной связи ГМГ-SКоАредуктаза ингибируется конечным продуктом реакции – холестеролом. Строение и обмен липидов 264 2. Регуляция транскрипции гена ГМГ-SКоА-редуктазы – холестерол и желчные кислоты подавляют считывание гена и уменьшают количество фермента. 3. Ковалентная модификация при гормональной регуляции: инсулин, активируя протеинфосфатазу, способствует переходу фермента ГМГ-SКоА-редуктазы в активное состояние. Важным следствием такой регуляции является прекращение кетогенеза при наличии инсулина. Глюкагон и адреналин посредством аденилатциклазного механизма активируют протеинкиназу А, которая фосфорилирует фермент и переводит его в неактивную форму.
Изменение транскрипции гена ГМГ-КоА редуктазы (генетическая регуляция) осуществляется стерол-регулируемым элементом в ДНК (SREBP, sterol regulatory element-binding protein) с которым способны связываться белки - факторы SREBP. Эти факторы при достаточном количестве холестерина в клетке закреплены в мембране ЭПР. Когда уровень холестерина падает, факторы SREBP активируются под действием специфичных протеаз комплекса Гольджи, передвигаются в ядро, взаимодействуют на ДНК с участком SREBP и стимулируют биосинтез холестерина.
Скорость биосинтеза холестерола также зависит от концентрации специфического белка-переносчика, обеспечивающего связывание и транспорт гидрофобных промежуточных метаболитов синтеза.
