
учебник фт Подзолков
.pdf
1.2.Хроническая обструктивная болезнь легких
7.В клинической картине больных ХОБЛ преобладают жалобы на:
A.Одышку и кашель.
B.Отеки ног и сердцебиение.
C.Боли в грудной клетке.
D.Головокружение и слабость.
E.Отеки ног, снижение уровня артериального давления.
8.Внелегочным проявлением ХОБЛ является:
A.Сахарный диабет.
B.Плеврит.
C.Хроническое легочное сердце.
D.Левожелудочковая недостаточность.
E.Тромбоэмболия легочной артерии.
9.Клиническая картина ХОБЛ:
A.Кашель с выделением желтой мокроты, прогрессирующая со временем одышка у курильщика.
B.Рецидивирующие приступы удушья при контакте с аллергенами.
C.Одышка при физической нагрузке при длительном анамнезе артериальной гипертензии.
D.Острое начало болезни, кашель, высокая лихорадка.
E.В клинической картине доминируют признаки правожелудочковой сердечной недостаточности.
10.Рентгенологические изменения при ХОБЛ:
A.Инфильтративные изменения в верхушках легких.
B.«Летучие» инфильтраты в легких.
C.Расширение тени средостения.
D.Признаки эмфиземы легких.
E.Синдром диссеминации.
Ответы: 1 — А, 2 — B, 3 — C, 4 — B, 5 — D, 6 — B, 7 — A, 8 — C, 9 — A, 10 — D.
Клиническая задача 1
Больной, 52 года, обратился к врачу с жалобами на одышку при умеренной физической нагрузке, кашель с мокротой желтого цвета преимущественно в утренние часы.
Кашель стал беспокоить пациента в течение 5 последних лет, сопровождался выделением серой мокроты. На протяжении последнего года больной стал ощущать одышку при физической нагрузке, которую хорошо переносил ранее. По поводу хронического кашля и одышки ранее к врачу не обращался. В течение последней недели кашель стал более интенсивным, мокрота приобрела желтый цвет, усилилась одышка.
Пациент курит с 16 лет в среднем по 1 пачке сигарет в сутки, работает инженером, в анамнезе — хронический гастрит.
При осмотре выявлено: сознание ясное, положение активное. Телосложение нормостеническое. Акроцианоз. Отеков нет. Температура тела 37,8 °С.
ЧДД 23 в минуту. Грудная клетка расширена в поперечнике, ригидная при пальпации. Надключичные ямки сглажены. При сравнительной перкуссии —
71
Глава 1. Болезни органов дыхания
коробочный звук, снижена подвижность нижнего края легких. При аускультации — дыхание с удлиненным выдохом, умеренное количество сухих рассеянных низкотональных хрипов, количество увеличивается при форсированном выдохе.
Область сердца не изменена. При пальпации и аускультации не выявлено патологии сердечно-сосудистой системы. ЧСС 102 в минуту. АД 120/70 мм рт. ст.
Живот мягкий, безболезненный. При глубокой пальпации живота патологических изменений не выявлено. Размеры печени и селезенки в переделах нормы. Сатурация (SaO2) 91%.
При проведении лабораторно-инструментального обследования пациента выявлено:
1. Общий анализ крови: лейкоциты 10,0 u 109/л, п. 3%, н. 72%, э. 2%, м. 5%, л. 18%, гемоглобин 150 г/л, эритроциты 4,0 u1012/л, тромбоциты 320 u 109/л, СОЭ 22 мм/ч.
2.Биохимический анализ крови: общий белок 72 г/л, АЛТ 12 ЕД/л, АСТ 10 ЕД/л, холестерин 5,0 моль/л, креатинин 92 мкмоль/л, мочевина 6,0 ммоль/л, глюкоза 4,5 ммоль/л.
3.ЭКГ: синусовый ритм, ЧСС 102 в минуту, нормальное положение электрической оси сердца.
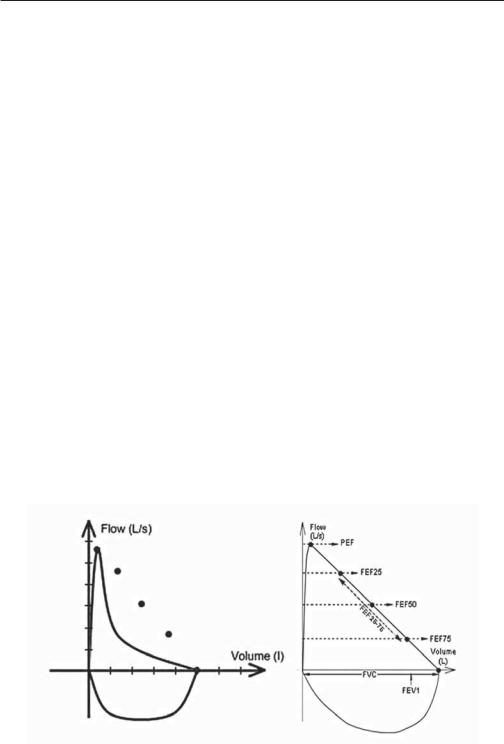
4.Показатели функции внешнего дыхания. Показатели спирометрии пациента — в табл. 1.16. Кривая «поток–объем» после ингаляции 400 мкг сальбутамола пациента и здорового человека — на рис. 1.4.
|
|
Таблица 1.16 |
|
|
Показатели спирометрии пациента |
||
|
|
|
|
Показатели |
Исходные показатели |
Показатели после ингаляции 400 мкг |
|
ФВД пациента, % |
сальбутамола, % |
||
|
|||
FEV1 (ОФВ1) |
46 |
49 |
|
FEV1% (ОФВ1/ФЖЕЛ ) |
45 |
50 |
|
PEF ( ПОС) |
68 |
68 |
|
Рис.1.4. Кривая «поток–объем» после ингаляции 400 мкг сальбутамола пациента и здорового человека
72

1.2.Хроническая обструктивная болезнь легких
5.Рентгенография органов грудной клетки: легочные поля увеличены
вразмерах, гиперпрозрачны, диафрагма уплощена, расширение ретростернального пространства, уменьшение числа и калибра легочных сосудов в периферических зонах.
6.Общий анализ мокроты: альвеолярные макрофаги 12 в поле зрения, лейкоциты 30 в поле зрения, эритроциты не выявлены, эозинофилы не выявлены, спирали Куршмана не выявлены, кристаллы Шарко–Лейдена не выявлены, микобактерии туберкулеза (МБТ) не выявлены.
Вопросы
1.Какие синдромы можно выделить у данного пациента?
2.Необходимы ли дополнительные исследования? Если да, то какие?
3.Сформулируйте диагноз.
4.Дайте рекомендации по лечению и изменению образа жизни.
Ответы
1.Синдром дыхательной недостаточности, воспаления дыхательных путей, эмфиземы легких, воспалительный синдром.
2.Необходимо выполнить анализ крови для определения уровня СРБ, определить газовый состав и кислотно-щелочное состояние артериальной крови, КТ органов грудной клетки. Требуется оценить выраженность симптомов ХОБЛ с помощью шкал CAT и MRC.
3.Хроническая обструктивная болезнь легких тяжелой степени, эмфизематозный фенотип, стадия обострения. Осложнения: дыхательная недостаточность.
4.Лечение: госпитализация, оксигенотерапия, бронхолитическая терапия в период обострения через небулайзер с применением бронхолитиков и ГКС, антибактериальная терапия, системные ГКС, мукорегуляторные препараты. После купирования обострения — базисная терапия пролонгированными бронхолитическими препаратами.
Клиническая задача 2
Больной, 65 лет, был доставлен бригадой скорой помощи в приемное отделение стационара с жалобами на одышку в покое с затруднением выдоха, кашель с трудноотделяемой, густой, вязкой мокротой желто-зеленого цвета, общую слабость.
Из анамнеза известно, что пациент курит около 50 лет в среднем по 1,5 пачки сигарет в сутки. В течение 10 последних лет пациента беспокоит хронический кашель с выделением мокроты серого цвета, одышку при физической нагрузке стал отмечать на протяжении 5 последних лет. Ранее одышка появлялась при значительной физической нагрузке больного, постепенно прогрессировала и в последние месяцы отмечается при обыденной физической нагрузке. Примерно два раза в год пациент отмечает периоды нарастания выраженности кашля, мокрота приобретает желтый цвет, становится более густой, нарастает одышка. По поводу вышеописанных жалоб пациент изредка обращался к терапевту по месту жительства, однако обследования не проходил, рекомендаций не придерживался. Настоящее ухудшение состояния отмечает на протяжении 10 последних дней перед госпитализацией после переохлаждения, когда усилился кашель, изменился характер выделяемой мокроты, наросла одышка.
73
Глава 1. Болезни органов дыхания
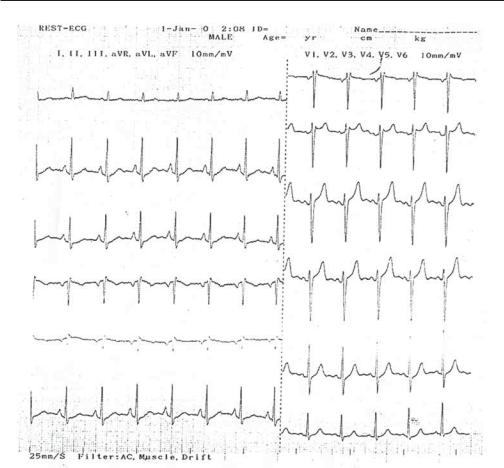
Рис. 1.5. ЭКГ больного (задача 2)
При обследовании выявлено: сознание ясное. Положение вынужденное: больной сидит, опираясь руками о край кровати. Телосложение астеническое. Дефицит массы тела. Ногти пальцев кистей рук изменены по типу часовых стекол, дистальные фаланги пальцев кистей рук расширены. Цианоз пальцев кистей рук, кожи носогубного треугольника, мочек ушей. Цианотичные пальцы теплые на ощупь. Отеков нет. Температура тела 37,7 °С.
ЧДД 25 в минуту. Грудная клетка расширена в поперечнике, ригидная при пальпации. Надключичные пространства выбухают, поля Кренига расширены. При сравнительной перкуссии выявляется коробочный звук, снижена подвижность нижнего края легких. При аускультации определяется дыхание с удлиненным выдохом, сухие рассеянные разнотональные хрипы.
Область сердца визуально не изменена. Правая граница относительной сердечной тупости находится на 2 см кнаружи от правого края грудины. Тоны сердца приглушены. Ритм сердечных сокращений правильный, ЧСС 112 в минуту, артериальное давление 110/66 мм рт. ст. Патологических шумов при аускультации сердца не выявлено.
74
1.2. Хроническая обструктивная болезнь легких
Живот мягкий, безболезненный. При глубокой пальпации живота патологических изменений не выявлено. Размеры печени и селезенки в пределах нормы.
При проведении лабораторно-инструментального обследования пациента выявлено:
1.Общий анализ крови: лейкоциты 12,0 u109/л, п. 4%, н. 75%, э. 2%, м. 5%, л. 15%, гемоглобин 160 г/л, эритроциты 5,3 u1012/л, тромбоциты 320 u109/л, СОЭ 25 мм/ч.
2.Биохимический анализ крови: общий белок 60 г/л, АЛТ 15 ЕД/л, АСТ 14 ЕД/л, холестерин 5,3 моль/л, креатинин 80 мкмоль/л, мочевина 8,0 ммоль/л, глюкоза 4,7 ммоль/л, С-реактивный белок 45 мг/л (норма — менее 0,5 мг/л).
3.ЭКГ пациента (рис. 1.5).
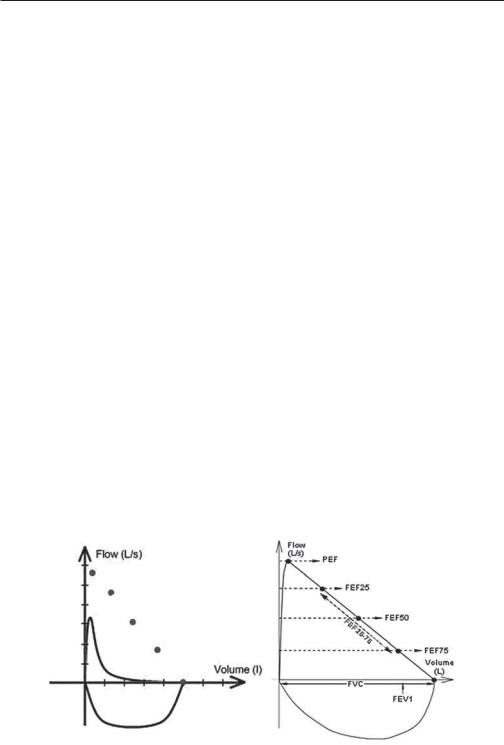
4.Показатели функции внешнего дыхания. Показатели спирометрии пациента — в табл. 1.17; кривая «поток–объем» после ингаляции 400 мкг сальбутамола пациента и здорового человека — на рис. 1.6.
5.Газовый состав артериальной крови: SaO2 86%, PaO2 55 мм рт. ст., PCO2 50 мм рт. ст.
6.Рентгенография органов грудной клетки: легочные поля увеличены в размерах, повышенной прозрачности, расширение ретростернального пространства на боковой рентгенограмме, уменьшение числа и калибра
|
|
Таблица 1.17 |
|
|
Показатели спирометрии пациента |
||
|
|
|
|
Показатели |
Исходные показатели |
Показатели после ингаляции |
|
ФВД пациента, % |
400 мкг сальбутамола, % |
||
|
|||
VC (ЖЕЛ) |
74 от должного значения |
74 |
|
FVC (ФЖЕЛ) |
78 |
78 |
|
FEV1 (ОФВ1) |
45 |
46 |
|
FEV1% (ОФВ1/ФЖЕЛ ) |
52 |
53 |
|
PEF ( ПОС) |
64 |
64 |
|
Рис. 1.6. Кривая «поток–объем» после ингаляции 400 мкг сальбутамола пациента и здорового человека
75

Глава 1. Болезни органов дыхания
легочных сосудов в периферических зонах, уплощение диафрагмы, усиление легочного рисунка в базальных отделах.
Вопросы
1.Какие синдромы можно выделить у данного пациента?
2.Необходимы ли дополнительные исследования? Если да, то какие?
3.Сформулируйте диагноз.
4.Дайте рекомендации по лечению и изменению образа жизни.
Ответы
1.Синдром дыхательной недостаточности, воспаления дыхательных путей, эмфиземы легких, хронического легочного сердца, воспалительный синдром.
2.Необходимо выполнить КТ органов грудной клетки, ЭхоКГ. Требуется оценить выраженность симптомов ХОБЛ с помощью шкал CAT и MRC.
3.Хроническая обструктивная болезнь легких тяжелого течения, эмфизематозный фенотип, стадия обострения. Осложнения: дыхательная недостаточность.
4.Лечение: госпитализация в отделение реанимации или интенсивной терапии, оксигенотерапия и неинвазивная вентиляция легких, бронхолитическая терапия в период обострения через небулайзер с применением бронхолитиков и ГКС, антибактериальная терапия, системные ГКС, мукорегуляторные препараты. После купирования обострения — базисная терапия пролонгированными бронхолитическими препаратами.
1.3.Бронхиальная астма
1.3.1.Определение. Статистика
«Астма» в переводе с греческого означает «удушье». Бронхиальная астма (БА) — это глобальная проблема здравоохранения во всем мире. По данным эпидемиологических исследований, в мире около 300 млн больных БА, и ежегодно регистрируется около 346 тыс. летальных исходов, связанных с БА [GINA, 2018]. У значительного числа пациентов заболевание диагностируется с существенным запозданием, поэтому истинная ее распространенность существенно больше. Летальность значительно выше в странах с низким социальным уровнем, что часто связано с несвоевременной диагностикой заболевания и неадекватной лечебной тактикой.
Распространенность БА начала прогрессивно увеличиваться с середины 60-х годов XX века в странах Западной Европы и Северной Америки, а начиная с середины 80-х годов — в странах Восточной Европы. В связи с ростом заболеваемости возникла необходимость объединения усилий по изучению бронхиальной астмы в глобальном мировом масштабе. В 1993 г. Национальным институтом сердца, легких и крови совместно с ВОЗ была создана рабочая группа из ведущих специалистов в области лечения БА из многих стран. С целью распространения информации о подходах к лечению и обеспечения внедрения результатов научных исследований в лечение БА экспертами была создана программа по ее диагностике, лечению и профилактике, по развитию взаимо-
76

1.3. Бронхиальная астма
действия между врачами, лечебными учреждениями и официальными инстанциями «Глобальная инициатива по бронхиальной астме» (Global Initiative for Asthma, GINA). Для укрепления международного сотрудничества в области лечения БА и распространения информации были подготовлены публикации, переведенные на разные языки. В настоящее время большинство Национальных рекомендаций по диагностике и лечению астмы, в том числе и рекомендации Российского респираторного общества, базируются на принципах GINA. Рекомендации GINA регулярно пересматриваются с учетом накопленного опыта и достижений современной медицины. В последней редакции рекомендаций GINA учтены новейшие сведения о заболевании, а также предложено новое определение, основанное на выделении наиболее характерных черт болезни, отличающих ее от других заболеваний системы дыхания.
Бронхиальная астма — гетерогенное заболевание, характеризующееся хроническим воспалением в дыхательных путях, сопровождающееся респираторными симптомами, такими как свистящие хрипы, одышка, заложенность в груди и кашель, которые меняются по времени и интенсивности и сопровождаются вариабельными нарушениями бронхиальной проходимости.
Под гетерогенностью астмы подразумеваются значительные отличия в патофизиологии, демографических и клинических характеристиках у разных больных.
1.3.2. Факторы риска
Бронхиальная астма — гетерогенное заболевание, в развитии которого играют роль внутренние (врожденные характеристики организма) факторы (определяют предрасположенность человека к развитию БА) и внешние (экологические) факторы (способствуют, увеличивают вероятность развития заболевания у предрасположенных к этому лиц) (табл. 1.18).
Генетическая предрасположенность. БА — генетически детерминированное заболевание, распространенность среди кровных родственников ее значительно выше по сравнению с общей популяцией. Однако на сегодняшний день установлено: нет единственного «гена астмы», а конкретные гены, вовлеченные
внаследственность БА, не идентифицированы. Вероятно, болезнь возникает
врезультате взаимодействия генов между собой и с окружающей средой. Поиск генов, связанных с формированием астмы, фокусируется на 4 направлениях:
1)выработка аллергенспецифических IgE-антител (генов, предрасполагающих к атопии);
2)выраженность гиперреактивности дыхательных путей (повышенная чувствительность к неспецифическим раздражителям по сравнению с нормой, т.е. состояние, при котором просвет бронхов сужается слишком легко или слишком мощно в ответ на провоцирующие факторы);
3)продукция медиаторов воспаления, таких как цитокины, хемокины и факторы роста;
4)определение соотношения между типами иммунного ответа с участием Т-лимфоцитов хелперов 1-го типа и Т-лимфоцитов хелперов 2-го типа (Th1- и Th2-лимфоцитов) в иммунном ответе.
77
|
|
|
Глава 1. Болезни органов дыхания |
|
|
|
Таблица 1.18 |
Факторы, влияющие на развитие и проявления БА |
|||
|
|
|
|
Внутренние факторы |
• |
Генетическая предрасположенность (к атопии, гиперреактивности |
|
|
|
дыхательных путей, развитию воспаления в дыхательных путях) |
|
|
• Пол (мужской в детском возрасте, женский — у взрослых) |
||
|
• |
Ожирение |
|
|
• Низкий вес при рождении |
||
Внешние факторы |
Факторы, способствующие развитию БА у предрасположенных к этому |
||
|
людей: |
||
|
• |
Домашние аллергены: |
|
|
|
домашняя пыль (клещи домашней пыли) |
|
|
|
аллергены животных (шерсть и эпидермис животных) |
|
|
|
|
аллергены тараканов |
|
|
|
грибы |
|
• |
Внешние аллергены: |
|
|
|
|
пыльца растений |
|
|
|
грибковые аллергены |
|
• Профессиональные (более 360 профессиональных сенсибилизиру- |
||
|
|
ющих веществ) |
|
|
• Курение (пассивное и активное) |
||
|
• Воздушные поллютанты (озон, диоксиды серы и азота, продукты сго- |
||
|
|
рания дизельного топлива) |
|
|
• Инфекционные агенты (преимущественно вирусные) |
||
|
• |
Паразитарные инфекции |
|
|
• |
Социально-экономический статус |
|
|
• |
Число членов семьи |
|
|
• |
Диета и лекарства (повышенное потребление продуктов высо- |
|
|
|
кой степени обработки, увеличенное поступление омега-6-поли- |
|
|
|
ненасыщенной жирной кислоты и сниженное — антиоксидантов (в |
|
|
|
виде фруктов и овощей) и омега-3-полиненасыщенной жирной кисло- |
|
|
|
ты (в составе жирных сортов рыбы)) |
|
Факторы, провоциру- |
• |
Домашние и внешние аллергены |
|
ющие обострения БА |
• |
Респираторная инфекция |
|
и/или являющиеся |
• |
Воздушные поллютанты |
|
причиной сохране- |
• |
Физическая нагрузка и гипервентиляция |
|
ния симптомов забо- |
• |
Изменение погодных условий |
|
левания (триггеры) |
• |
Двуокись серы |
|
|
• Пища, пищевые добавки, лекарства |
||
|
• |
Чрезмерные эмоциональные нагрузки |
|
|
• |
Курение |
|
|
• Ирританты (аэрозоли, запахи краски) |
||
В настоящее время идентифицировано более 100 генов, связанных с астмой. Параллельно проводится изучение генов, определяющих эффективность противоастматических препаратов. Выявлены:
•полиморфизм генов, кодирующих синтез E2-адренорецепторов;
•гены, регулирующие гиперчувствительность D-адренорецепторов (при раздражении которых повышается проницаемость капилляров и возникают отек слизистой оболочки бронхиол, гиперсекреция слизи);
78

1.3.Бронхиальная астма
•гены, регулирующие ответ пациентов на глюкокортикостероиды и антилейкотриеновые препараты.
Возможно, что факторы окружающей среды (внешние факторы) в раннем возрасте определяют, какие люди (имеющие генетическую предрасположенность) заболевают БА. В частности, рост распространенности БА за последние несколько десятилетий в развивающихся странах свидетельствует о важности взаимодействия экологических механизмов с генетической предрасположенностью.
Атопия — основной фактор риска развития астмы. Атопия генетически обусловлена и проявляется продукцией специфических IgE-антител. У лиц без атопии риск развития астмы очень низкий. Пациенты с БА обычно имеют другие атопические заболевания, в частности атопический дерматит; примерно у 80% больных БА — аллергический ринит. Наличие атопии наблюдается у 40–50% популяции в развитых странах, но только часть имеет БА. Это свидетельствует о том, что экологические или генетические факторы влияют на развитие БА у лиц с атопией. Аллергены, приводящие к сенсибилизации, являются белками, имеющими протеазную активность; наиболее распространенными из них являются аллергены клещей домашней пыли, шерсти кошки, собаки, тараканов, пыльца трав и деревьев.
Эпигенетические изменения (наследуемые изменения в экспрессии генов и фенотипе клетки, которые не затрагивают последовательности самой ДНК). Существует все больше доказательств того, что эпигенетические механизмы могут играть важную роль в развитии астмы, особенно на начальных этапах развития. Факторы окружающей среды (проживание среди курильщиков, неправильное питание) могут привести к метилированию ДНК и сбоям в функционировании генов (но не в их структуре), вовлеченных в патогенез БА. Эти сбои могут передаваться будущим поколениям. Эпигенетические изменения могут возникать у плода в результате воздействия окружающей среды на мать.
Инфекции. Несмотря на то что вирусные инфекции (особенно риновирусные) часто являются триггерами обострений астмы, до конца неясно, играют ли они определенную роль в этиологии БА. Существует взаимосвязь между респираторной синцитиальной вирусной инфекцией в младенчестве и развитием астмы, но конкретный патогенез не объясним. В настоящее время признано, что проживание во влажных домах с воздействием спор плесени является фактором риска для развития БА, и устранение этого фактора может улучшить течение астмы. Интересно отметить следующее: аллергическая сенсибилизация и астма наблюдаются реже у маленьких детей, имеющих братьев и сестер или посещающих детский сад, однако у них повышен риск развития инфекций. Для объяснения этого предложена «гигиеническая гипотеза», согласно которой «контакт» с инфекциями в раннем детстве способствует развитию иммунной системы ребенка по «неаллергическому» пути (сдвиг в сторону преобладающего защитного Th1-иммунного ответа), следствием чего является снижение риска БА и других аллергических заболеваний. Отсутствие инфекций в раннем детстве сохраняет смещение в сторону Th2-клеток, имеющихся при рождении. Этот механизм может объяснить выявленную взаимосвязь между размером семьи, порядком рождений, посещением детского сада и риском развития БА. С другой сторо-
79

Глава 1. Болезни органов дыхания
ны, «гигиеническая гипотеза» не может объяснить параллельный рост Th1обусловленных заболеваний, таких как сахарный диабет. В настоящее время изучение «гигиенической гипотезы» продолжается.
Диета. Роль диетических факторов противоречива. Ряд проведенных исследований показал, что диеты с низким содержанием антиоксидантов, таких как витамин C и витамин A, магния, селена, и омега-3-полиненасыщенных кислот (масло рыб) или высоким содержанием натрия и омега-6-полиненасыщенных кислот, связаны с повышенным риском астмы. Дефицит витамина D также может предрасполагать к развитию астмы.
Воздушные поллютанты. Воздушные поллютанты, такие как двуокись серы, озон, твердые частицы дизельного топлива, могут вызвать симптомы астмы, но роль различных загрязняющих веществ в этиологии заболевания пока не ясна.
Аллергены. Хорошо известно, что аллергены помещений и внешние аллергены могут вызывать обострения БА, однако их специфическая роль в развитии БА не вполне ясна. Проведенные исследования у детей показали, что сенсибилизация к аллергенам клеща домашней пыли, перхоти кошек и собак, к грибку рода Aspergillus является независимым фактором риска симптомов, напоминающих астматические, у детей в возрасте до 3 лет. Однако взаимосвязь между контактом с аллергеном и сенсибилизацией носит непрямой характер, зависит от вида аллергена, дозы, длительности контакта, возраста ребенка и, вероятно, генетической предрасположенности. Другим важным фактором аллергической сенсибилизации в городских домах является присутствие в доме тараканов. Что касается собак и кошек, то в некоторых эпидемиологических исследованиях отмечено, что ранний контакт с этими животными может защищать ребенка от аллергической сенсибилизации или развития БА, в других — высказывается предположение, что такие контакты могут увеличить риск аллергической сенсибилизации. Этот вопрос остается нерешенным. У детей, выросших в сельской местности, отмечается сниженная частота развития БА.
Профессиональная астма. Профессиональную БА определяют как астму, обусловленную контактом с аллергеном на рабочем месте. Профессиональную астму можно подозревать, когда проявления заболевания уменьшаются в выходные и праздничные дни. На сегодняшний день идентифицировано более 300 сенсибилизирующих агентов, способных привести к развитию профессиональной БА. К ним относятся вещества с низким молекулярным весом и высокой активностью: изоцианаты (ирританты), способные вызывать бронхиальную гиперреактивность, соли платины, сложные биологические вещества растительного и животного происхождения, стимулирующие выработку IgE. Профессиональные сенсибилизаторы служат причиной примерно каждого десятого случая БА у взрослых трудоспособного возраста. В индустриальных странах БА является самым частым профессиональным заболеванием органов дыхания, наиболее высокий риск ее развития характерен для таких областей деятельности, как сельское хозяйство, малярное дело, уборка/чистка, производство пластмасс. В большинстве случаев профессиональная БА развивается после латентного периода продолжительностью от нескольких месяцев до нескольких лет после начала контакта с аллергеном. Предполагается, что для многих профессиональных сенсибилизаторов существуют концентрации, пре-
80
