
- •1. Электропроводность металлов. Виды электропроводности.
- •2. Сложные полупроводники. Стеклообразные и аморфные полупроводники.
- •1. Типы электропроводности. Механизмы электропроводности.
- •2. Назначение оплетки кабеля.
- •1. Что такое полупроводник n-типа.
- •2. Биполярный транзистор в режиме насыщения.
- •1. Органические диэлектрики
- •2. Газообразные диэлектрики
Контрольные работы по МиЭЭТ
Студента группы АНб-21-2, Зарипова М. В.
Контрольная работа №1
Вариант №4
1. Электропроводность металлов. Виды электропроводности.
Металлы – это вещества обладающие высокой электропроводностью, теплопроводностью, прочностью, а также характерным блеском. Металлы подразделяют на металлы с высокой удельной проводимостью, благородные металлы, тугоплавкие металлы и металлы со средним значением температуры плавления.
В металлах атомы настолько плотно «упакованы», что электрон одного атома испытывает достаточно значительную силу других атомов. В результате валентная зона и зона проводимости в металлах приближаются друг к другу и могут даже перекрываться. Следовательно, получая очень небольшое количество энергии от внешнего тепла или источника электрической энергии, электроны легко поднимаются на более высокие уровни в металле. Такие электроны известны как свободные электроны. Эти свободные электроны ответственны за ток, протекающий через металл. Когда внешний электрический источник подключен к металлу, эти свободные электроны начинают течь к более высокому потенциальному выходу источника, в результате чего ток течет в металле.
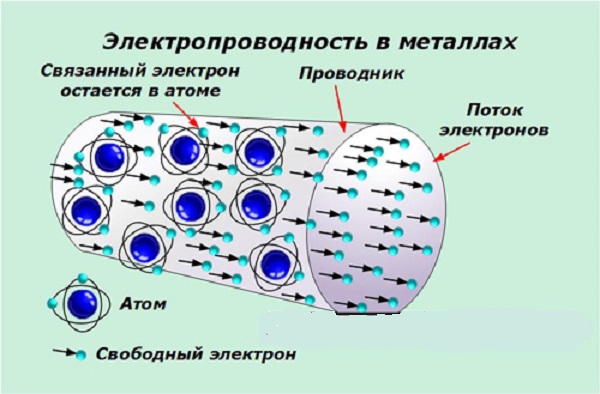
Рисунок 1 Электропроводность в металлах.
Электропроводность – способность тела, вещества или среды проводить электрический ток.
Электропроводность всех веществ связана с наличием в них носителей тока подвижных заряженных частиц.
Виды электропроводности.
Существуют различные виды электропроводности, которые происходят в материалах с разными свойствами и структурами. Рассмотрим основные виды электропроводности более подробно:
Ионная электропроводность:
Носителями заряда в водных растворах или расплавах электролитов являются положительно и отрицательно заряженные ионы. Если сосуд в раствором электролита включить в электрическую цепь, то отрицательные ионы начнут двигаться к положительному электроду – аноду, а положительные – к отрицательному – катоду. В результате установится электрический ток. Например, морская вода проводит электрический ток благодаря содержанию ионов калия, магния и натрия.
Электронную проводимость имеют полупроводниковые материалы с донорными примесями, валентность которых превышает валентность самого полупроводника. Электроны проводимости появляются в них в результате перехода электрона из валентной зоны донора в зону проводимости полупроводника. Это объясняется перекрытием валентной зоны донора и зоны проводимости полупроводника.
Дырочная проводимость получается при добавлении акцепторных примесей, валентностью меньшей, чем у полупроводника. В этом случае электрон из валентной зоны полупроводника переходит в валентную зону акцептора, а в валентной зоне полупроводника образуется вакантное место, условно названное дыркой. Движение дырок можно рассматривать как движение положительно заряженных частиц. Дырка заполняется электроном из валентной зоны соседнего атома, в которой также возникает дырка. В результате при действии внешнего электрического поля появляется электрический ток.
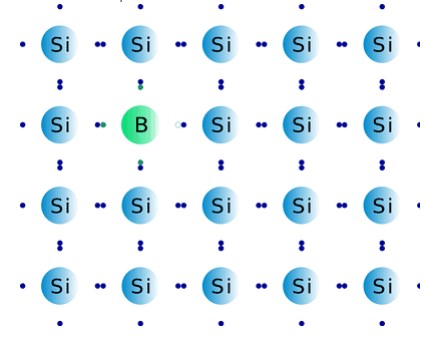
Рисунок 2 Акцепторная примесь.
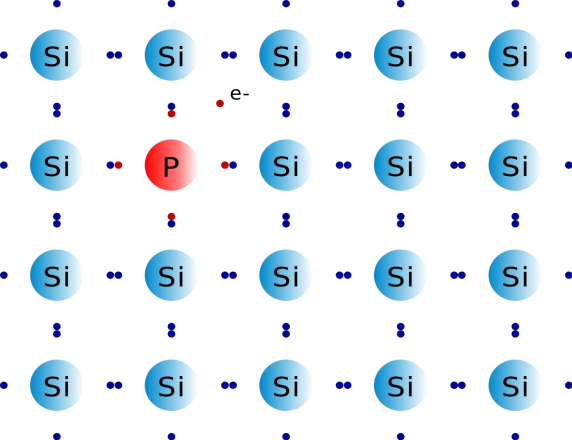
Рисунок 3 Донорная примесь.
2. Сложные полупроводники. Стеклообразные и аморфные полупроводники.
Полупроводниковыми называют материалы, являющиеся по удельной проводимости промежуточными между проводниковыми и диэлектрическими материалами и отличительным свойством которых является сильная зависимость удельной проводимости от концентрации и вида примесей или различных дефектов, а также в большинстве случаев от внешних воздействий. К полупроводникам принадлежат 12 химических элементов в средней части таблицы Менделеева – бор B, углерод C, кремний Si, фосфор P, германий Ge, мышьяк As, селен Se, олово Sn, сурьма Sb, теллур Te, йод I.
Сложными называют полупроводники, у которых структура образованна атомами различных химических элементов. Наиболее широкое применение нашли неорганические кристаллические полупроводники. Первыми из них, получившими практическое применение, были оксиды металлов. Из сложных полупроводниковых материалов в настоящее время наиболее широкое применение нашли двойные кристаллические соединения типа AmBn, где m+n=8. В этих соединениях кристаллическая решетка и среднее количество электронов на один атом такие же, как у кремния и германия, что предопределяет общность многих свойств. Полупроводниковые свойства проявляются не только в кристаллических, но и в аморфных соединениях, в частности в неорганических стеклах.
Стеклообразные полупроводники, обладают чисто электронной электропроводностью. Введение примесей незначительно изменяет свойства стеклообразных полупроводников, примесная электропроводность в них не проявляется. Полупроводниковыми свойствами обладают как кислородосодержащие стекла и бескислородные халькогенидные стекла.
Контрольная работа №2
Вариант №4
