
Лекции / Metodichka
.docx
Министерство науки и высшего образования РФ
Федеральное государственное бюджетное образовательное учреждение
высшего профессионального образования
«Уфимский государственный нефтяной технический университет»
ИХТИ ФГБОУ ВО УГНТУ в г.Стерлитамаке
Кафедра «Общей химической технологии»
МЕТОДИЧЕСКИЕ УКАЗАНИЯ
к лабораторной работе
По дисциплине «Химия и технология хлорорганического синтеза»
«Изучение влияния температуры на процесс эпоксидированияизоамиленовой фракции гидроперекисью изопропилбензола»
для обучающихся по направлению 18.04.01 «Химическая технология»,
программа магистратуры
«Химия и технология продуктов основного органического
и нефтехимического синтеза».
Составил,
к. т. н., доцент А.А. Исламутдинова
2023
Лабораторная работа № 1
«Изучение влияния температуры на процесс эпоксидирования
изоамиленовой фракции гидроперекисью изопропилбензола»
1 Цель работы: изучение влияния температуры на процесс эпоксидированияизоамиленовой фракции гидроперекисью изопропилбензола.
Оборудование, реактивы и растворы:
- Изоамиленовая фракция-20 мл (13,75 г);
- 90 % гидроперекись изопропилбензола 8 мл (10г);
- нафтенат молибдена 0,018 г;
- 0,1 н раствор тиосульфата натрия;
- 0,1 н раствор соляной кислоты в ледяной уксусной кислоте;
- 0,5 % раствор крахмала;
- 0,5 % раствор йодистого калия;
- индикатор кристаллвиолет;
- трехгорлая колба;
- холодильник обратный;
- термометр со шкалой от 0 до 100°С;
- мешалка с электроприводом;
- термостат;
- шприц с длинной иглой;
- колбы с притертой пробкой на 50 мл и 100 мл;
- микробюретка;
- магнитная мешалка.
Схема лабораторной установки представлена на рисунке 1.

1 – реактор; 2 – холодильник; 3 – термометр; 4 – гидрозатвор; 5 – делительная воронка; 6 – мешалка; 7 – контактный термометр; 8 – электроконтактное реле; 9 – электроплитка; 10 – глицериновая баня; 11 – электродвигатель; 12 – латр
Рисунок 1 – Схема установки
Теоретическая часть
Эпоксидирование – это превращение двойной связи олефинов в эпоксидное кольцо (это циклические просты эфиры, которые обладают высокой реакционной способностью в реакциях раскрытия цикла).
Эпоксидирование осуществляют, как правило, с помощью окислителей: надкислот (Прилежаева реакция), хромовой кислоты, гипохлорита натрия в пиридине, гидроперекисью изопропилбензола и др. Для эпоксидирования непредельных карбонильных соединений используют Н2О2 в щелочной среде.
Эпоксидированиеизоамилена гидроперекисями с образованием окиси изоамилена, изомеризация и дегидротация последней в изопрен – являются стадиями, получившего промышленное значение метода синтеза мономера.
Гидроперекись изопропилбензола С6Н5(СН3)2-О-ОН представляет собой бесцветную маслянистую, немного вязкую жидкость с характерным запахом, напоминающим запах озона. При попадании на кожу вызывает ожоги, подобно концентрированным растворам Н2О2.
Из известных в настоящее время промышленных способов получения изопрена очень трудно выделить наиболее экономичный. Для успешной конкуренции с натуральным каучуком себестоимость изопрена не должна превышать 250 руб/т. Поэтому до сих пор продолжают поиски новых путей синтеза изопрена.
2 Проведение опыта
В колбе на 50 мл готовится смесь изопропилбензола и изоамилена в мольном соотношении 1:2. Для этого нужно взять 8 мл (10 г) 90 % гидроперекиси изопропилбензола, 20 мл (13,75 г) изоамилена и 0,018 г катализатора MoO2R2, то есть в количестве 0,2 % от гидроперекиси. Катализатор вносится на стеклянной палочке в охлажденную смесь при перемешивании.
Приготовленную смесь необходимо перенести в реактор, в который помещен термостат,предварительно нагретый до 30°С. Включается мешалку, через 20 минут шприцом отбираются пробы, в которых анализируется содержание окиси и гидроперекиси.
C
CH3
CH3
C6H5–CH=CH2
–H2O

O
6H5–CHOOH + CH2=CH–CH3C6H5–CH–OH + H2C–CH–CH3
Конверсия (χ) определяется по формуле (1):
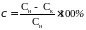 ,
(1)
,
(1)
где Сн – концентрация гидроперекиси в исходной смеси;
Ск – концентрация гидроперекиси после отбора пробы.
Селективность (S) определяется по формуле (2):
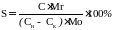 ,(2)
,(2)
гдеMr– молекулярная масса гидроперекиси;
Mo– молекулярная масса окиси;
С–концентрация окиси после отбора пробы.
3 Методика проведения эксперимента
1. Методика определения концентрации окиси
Количественное определение окиси основано на легкости присоединения амиленоксидами соляной кислоты и образования амиленхлоргидринов.
В предварительно взвешенную колбу на 100 мл (с притертой пробкой) шприцом вводится 2 мл анализируемой пробы и взвешивается. Добавляется 20 мл ледяной уксусной кислоты, 2-3 капли индикатора кристаллвиолета, опускается магнитик и оттитровывается до светло-зеленой установившейся окраски 0,1 н раствором соляной кислоты в ледяной уксусной кислоте.
2. Методика определения концентрации гидроперекиси изопропилбензола
Во взвешенную колбу на 100 мл (с притертой пробкой) шприцом вводится2 мл анализируемой пробы и взвешивается. Добавляется 10 мл уксусной кислоты, 5 мл 50 % раствора йодистого калия и ставится на 20 минут в темное место. Затем добавляется дистиллированная вода и оттитровывается 0,1 н раствором тиосульфата натрия в присутствии крахмала.
Обработка результатов:
Концентрация окиси Х (%) рассчитывается по формуле (3):
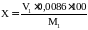 ,
(3)
,
(3)
где V1– объем соляной кислоты в уксусной кислоте, мл;
M1– навеска пробы, г;
0,0086– количество окиси, соответствующее 1 мл 0,1н раствора соляной кислоты в уксусной кислоте.
Концентрация гидроперекиси Х (%) рассчитывается по формуле (4):
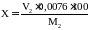 ,(4)
,(4)
где V2 – объем пробы, взятой на титрование, мл;
0,0076 – количество гидроперекиси, соответствующее 1 мл 0,1н раствора тиосульфата натрия.
Рассчитать конверсию и селективность.
